1 . 硼族元素可形成许多结构和性质特殊的化合物。回答下列问题
(1)基态Ga原子的电子排布式为__________ 。
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和________ (填化学式)。NF3和NF3BF3中F-N-F的键角大小是NF3_______ NF3BF3(填“>”、“<”或“=”)。
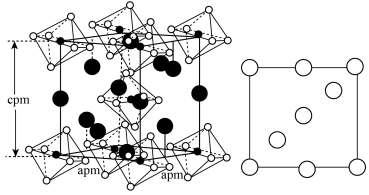
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示,晶胞参数为a pm、cpm,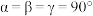 。
。__________ 。
②X晶体内含有的作用力有__________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
③晶体中有__________ 种化学环境的●原子。
(4)阿伏加德罗常数的值为NA。化合物X的密度为__________ g/cm3(用含a,c的代数式表示)。
(1)基态Ga原子的电子排布式为
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示,晶胞参数为a pm、cpm,
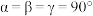 。
。
②X晶体内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
③晶体中有
(4)阿伏加德罗常数的值为NA。化合物X的密度为
您最近半年使用:0次
解题方法
2 . 下列表示不正确的是
A.HF分子中 键的形成示意图为 键的形成示意图为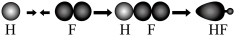 |
B.基态Cr原子的价层电子轨道表示式为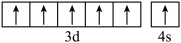 |
C. 分子的VSEPR模型: 分子的VSEPR模型: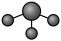 |
D.2,4,6—三硝基甲苯的结构简式: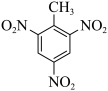 |
您最近半年使用:0次
解题方法
3 . 下列关于肼的说法正确的是
A.电子式为 | B.既含极性键,又含非极性键 |
| C.属于极性分子 | D.N原子为sp2杂化 |
您最近半年使用:0次
4 . 根据短周期元素的性质回答下列问题。
I. 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应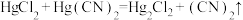 用于制备
用于制备 。
。
(1)上述反应的氧化剂是_______ 。
(2)写出 的结构简式
的结构简式_______ , 的空间构型是
的空间构型是_______ ;1mol 分子中
分子中 键为
键为_______ mol。
(3) 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式_______ 。
(4)基态N价层电子排布式为_______ 。
Ⅱ.氟化镁( )晶胞是长方体,其结构如图所示
)晶胞是长方体,其结构如图所示 晶胞示意图中○表示
晶胞示意图中○表示_______ (填离子符号)。
(6)结合离子结构示意图,解释离子半径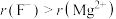 的原因
的原因_______ 。
(7) 晶胞中有
晶胞中有_______ 个 ;
;_______ 个 。
。
I.
 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应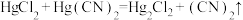 用于制备
用于制备 。
。(1)上述反应的氧化剂是
(2)写出
 的结构简式
的结构简式 的空间构型是
的空间构型是 分子中
分子中 键为
键为(3)
 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式(4)基态N价层电子排布式为
Ⅱ.氟化镁(
 )晶胞是长方体,其结构如图所示
)晶胞是长方体,其结构如图所示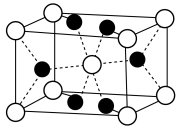
 晶胞示意图中○表示
晶胞示意图中○表示(6)结合离子结构示意图,解释离子半径
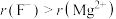 的原因
的原因(7)
 晶胞中有
晶胞中有 ;
; 。
。
您最近半年使用:0次
解题方法
5 . M、N、P、Q、R是原子序数依次增大的前四周期主族元素,组成的化合物R4N(PM4)4Q2是某种荧光粉中的成分。M的一种单质是极性分子,N基态原子核外无未成对电子,P元素存在于航空、信息和新能源等高技术领域必需的材料中,Q是一种重要的成盐元素。下列说法错误的是
| A.N、Q、R三种元素简单离子的半径:Q>R>N |
| B.N、P、Q、R四种元素的第一电离能:Q>P>N>R |
C.M元素与氢元素形成的两种微粒的键角: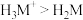 |
| D.N、P、R三种氧化物的熔点:P>R>N |
您最近半年使用:0次
6 . 氮化碳是新发现的高硬度材料,其部分结构如下图所示。下列有关其说法不 正确的是
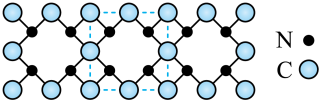
| A.氮化碳属于共价晶体 |
B.氮化碳中碳显 价,氮显 价,氮显 价 价 |
| C.氮化碳的硬度比金刚石略大 |
| D.氮化碳中C原子和N原子的最外层都满足8电子稳定结构 |
您最近半年使用:0次
7 . 化合物A是一种配合物,其化学式为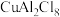 。某兴趣小组进行了如下实验:
。某兴趣小组进行了如下实验:_______ ,蓝色溶液G中含有的阳离子除了有 外,还含有
外,还含有_______ (用离子符号表示)。
(2)深蓝色溶液D中溶质的阳离子为_______ , 该离子含有的σ键的数目为
该离子含有的σ键的数目为_______ 。
(3)化合物A的一价阴离子与 具有相同的空间结构,该阴离子的电子式为
具有相同的空间结构,该阴离子的电子式为_______ 。
(4)蓝色溶液B与 作用,溶液颜色褪去,生成一种无色气体和一种白色沉淀
作用,溶液颜色褪去,生成一种无色气体和一种白色沉淀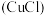 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
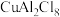 。某兴趣小组进行了如下实验:
。某兴趣小组进行了如下实验: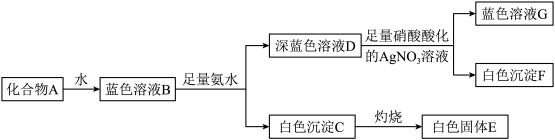
 外,还含有
外,还含有(2)深蓝色溶液D中溶质的阳离子为
 该离子含有的σ键的数目为
该离子含有的σ键的数目为(3)化合物A的一价阴离子与
 具有相同的空间结构,该阴离子的电子式为
具有相同的空间结构,该阴离子的电子式为(4)蓝色溶液B与
 作用,溶液颜色褪去,生成一种无色气体和一种白色沉淀
作用,溶液颜色褪去,生成一种无色气体和一种白色沉淀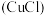 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近半年使用:0次
8 . 氯元素具有多种化合价,形成的 等离子,在一定条件下能发生相互转化。
等离子,在一定条件下能发生相互转化。 和碱反应可生成多种含氧酸盐,且温度不同,反应产物也不同。下列有关
和碱反应可生成多种含氧酸盐,且温度不同,反应产物也不同。下列有关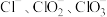 和
和 的说法正确的是
的说法正确的是
 等离子,在一定条件下能发生相互转化。
等离子,在一定条件下能发生相互转化。 和碱反应可生成多种含氧酸盐,且温度不同,反应产物也不同。下列有关
和碱反应可生成多种含氧酸盐,且温度不同,反应产物也不同。下列有关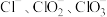 和
和 的说法正确的是
的说法正确的是A. 中心原子轨道的杂化类型为 中心原子轨道的杂化类型为 | B. 的空间构型为平面正三角形 的空间构型为平面正三角形 |
C. 与 与 的键角相等 的键角相等 | D. 提供孤电子对与 提供孤电子对与 可形成 可形成 |
您最近半年使用:0次
解题方法
9 . 下列说法正确的是
A.用电子云轮廓图表示 的 的 键形成的示意图: 键形成的示意图: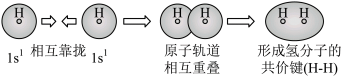 |
B. 的电子式为 的电子式为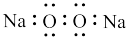 |
| C.共价键的键能越大,分子晶体的熔沸点越高 |
D.同一周期中,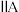 与 与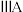 族元素原子的核电荷数都相差1 族元素原子的核电荷数都相差1 |
您最近半年使用:0次
解题方法
10 . 下列物质性质排序错误的是
A.酸性: | B.沸点: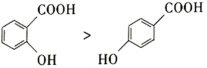 |
C.熔点: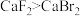 | D.稳定性: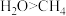 |
您最近半年使用:0次



