1 . 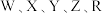 为短周期主族元素,原子序数依次增大。W的某种原子核内无中子,
为短周期主族元素,原子序数依次增大。W的某种原子核内无中子, 为同周期相邻元素,Z2是氧化性最强的单质,W的核外电子数与R的价层电子数相等,下列有关说法正确的是
为同周期相邻元素,Z2是氧化性最强的单质,W的核外电子数与R的价层电子数相等,下列有关说法正确的是
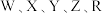 为短周期主族元素,原子序数依次增大。W的某种原子核内无中子,
为短周期主族元素,原子序数依次增大。W的某种原子核内无中子, 为同周期相邻元素,Z2是氧化性最强的单质,W的核外电子数与R的价层电子数相等,下列有关说法正确的是
为同周期相邻元素,Z2是氧化性最强的单质,W的核外电子数与R的价层电子数相等,下列有关说法正确的是| A.第一电离能:Z>Y>X |
| B.W2Y2不稳定易分解的主要原因是分子间氢键较弱 |
| C.Y和R反应生成的化合物中只含有离子键 |
| D.XW3和WZ均为极性分子 |
您最近一年使用:0次
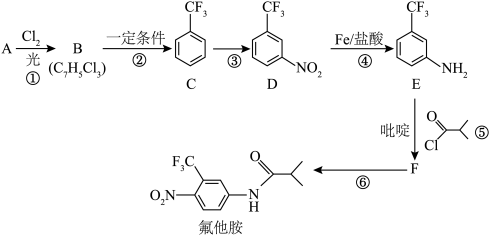
2 . 氟他胺是一种抗肿瘤药,在实验室由芳香烃A制备氟他胺的合成路线如下所示:_______ 组吸收峰。
(2)化合物E中官能团的名称为_______ 、_______ 。
(3)反应③的反应类型为_______ ,所需反应试剂和反应条件是_______ 。
(4)写出反应⑤的化学方程式_____ ;吡啶是一种有机碱,其在反应⑤中的作用是_______ 。
(5)关于氟他胺的说法中,正确的有_______。(填字母)
(6)对甲氧基乙酰苯胺(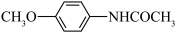 )是合成染料和药物的中间体,诸写出由苯甲醚(
)是合成染料和药物的中间体,诸写出由苯甲醚(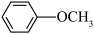 )制备对甲氧基乙酰苯胺的合成路线
)制备对甲氧基乙酰苯胺的合成路线_______ (其他试剂任选)。
(2)化合物E中官能团的名称为
(3)反应③的反应类型为
(4)写出反应⑤的化学方程式
(5)关于氟他胺的说法中,正确的有_______。(填字母)
| A.分子间可形成氢键 | B.所有碳原子一定共平面 |
C.碳原子均为 杂化 杂化 | D.分子中存在手性碳原子 |
(6)对甲氧基乙酰苯胺(
 )是合成染料和药物的中间体,诸写出由苯甲醚(
)是合成染料和药物的中间体,诸写出由苯甲醚( )制备对甲氧基乙酰苯胺的合成路线
)制备对甲氧基乙酰苯胺的合成路线
您最近一年使用:0次
名校
解题方法
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1 mol[Co(NH3)5Cl2]Cl中含配位键的数目为7NA |
| B.1 mol/LCaCl2溶液中含离子总数为3NA |
| C.标准状况下,2.24 LCO2分子中含有的σ键的数目为0.4NA |
| D.44 gCH3CHO中sp3杂化的碳原子数目为2NA |
您最近一年使用:0次
2024-09-13更新
|
69次组卷
|
2卷引用:湖南省常德市临澧县第一中学2025届高三上学期第一次阶段性考试化学试题
名校
4 . 内酯Y可以由X通过电解合成,并可在一定条件下转化为Z,转化路线如图所示。
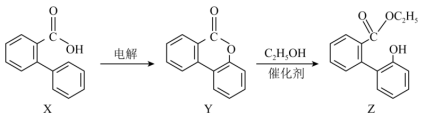
| A.Z分子中有两种杂化方式的碳原子 |
| B.Z分子中至少有13个碳原子在同一平面 |
| C.在催化剂作用下Z可与甲醛发生反应 |
D.等物质的量的X、Y、Z与足量 溶液反应,消耗的 溶液反应,消耗的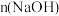 之比为 之比为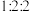 |
您最近一年使用:0次
名校
5 . 下列化学用语或化学图谱不正确的是
A. 的VSEPR模型: 的VSEPR模型: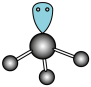 |
B.乙醚的结构简式: |
C.乙醇的核磁共振氢谱: |
D.邻羟基苯甲醛分子内氢键示意图: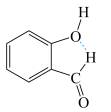 |
您最近一年使用:0次
6 . 下列说法错误的是
A.相同条件下 比 比 稳定 稳定 | B. 与 与 的空间构型相同 的空间构型相同 |
C. 中 中 键比 键比 键更易断裂 键更易断裂 | D. 中 中 键和大π键的数目不相等 键和大π键的数目不相等 |
您最近一年使用:0次
7 . 前四周期元素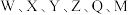 的原子序数依次增大。基态W原子核外电子的空间运动状态有4种,基态Y原子最外层电子数是内层电子数的3倍。元素Q对应的单质与酸或碱均能反应生成气体,基态
的原子序数依次增大。基态W原子核外电子的空间运动状态有4种,基态Y原子最外层电子数是内层电子数的3倍。元素Q对应的单质与酸或碱均能反应生成气体,基态 核外有5个未成对电子。基态Z原子的部分电离能数据如下:
核外有5个未成对电子。基态Z原子的部分电离能数据如下:
回答下列问题:
(1)W的元素符号为___________ 。
(2)基态Z原子最外层电子云轮廓图为___________ (填名称)。1个Q原子核外有___________ 种运动状态不同的电子。
(3)基态X原子核外电子占据___________ 个原子轨道。基态Y原子核外能量最高的能层符号是___________ 。
(4) 不稳定,易转化成
不稳定,易转化成 的原因是
的原因是___________ (从结构角度分析)。
(5) 在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为
在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为___________ 。
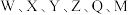 的原子序数依次增大。基态W原子核外电子的空间运动状态有4种,基态Y原子最外层电子数是内层电子数的3倍。元素Q对应的单质与酸或碱均能反应生成气体,基态
的原子序数依次增大。基态W原子核外电子的空间运动状态有4种,基态Y原子最外层电子数是内层电子数的3倍。元素Q对应的单质与酸或碱均能反应生成气体,基态 核外有5个未成对电子。基态Z原子的部分电离能数据如下:
核外有5个未成对电子。基态Z原子的部分电离能数据如下:| 元素 | 电离能 | |||
 |  |  |  | |
 | 738 | 1451 | 7733 | 10540 |
(1)W的元素符号为
(2)基态Z原子最外层电子云轮廓图为
(3)基态X原子核外电子占据
(4)
 不稳定,易转化成
不稳定,易转化成 的原因是
的原因是(5)
 在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为
在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 铁( )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)铁系元素能与 形成
形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点 ,则
,则 中含有的化学键类型包括_______。
中含有的化学键类型包括_______。
(2)以甲醇为溶剂, 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素( 、
、 、
、 、
、 )第一电离能由大到小的顺序为
)第一电离能由大到小的顺序为_______ ,色氨酮分子中 原子的杂化类型为
原子的杂化类型为_______ 。 射线衍射分析显示色胺酮钴配合物晶胞中还含有一个
射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 是通过
是通过_______ 作用与色胺酮钴配合物相结合。 、
、 、
、 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点, 、
、 、
、 明显高于
明显高于 ,其原因是
,其原因是_______ 。
(4) 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如下图所示:
的晶胞结构如下图所示: 、
、 点的原子坐标分别为(0,0,0)和(1,
点的原子坐标分别为(0,0,0)和(1, ,
, ),则
),则 点的原子坐标为
点的原子坐标为_______ ;
②立方 的晶胞参数
的晶胞参数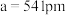 ,则其晶体密度为
,则其晶体密度为_______  。(列出计算表达式)
。(列出计算表达式)
 )、钴(
)、钴( )、镍(
)、镍( )是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。(1)铁系元素能与
 形成
形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点 ,则
,则 中含有的化学键类型包括_______。
中含有的化学键类型包括_______。| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
(2)以甲醇为溶剂,
 可与色胺酮分子配位结合形成对
可与色胺酮分子配位结合形成对 具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素(
具有切割作用的色胺酮钴配合物(合成过程如下所示)。色胺酮分子中所含元素( 、
、 、
、 、
、 )第一电离能由大到小的顺序为
)第一电离能由大到小的顺序为 原子的杂化类型为
原子的杂化类型为 射线衍射分析显示色胺酮钴配合物晶胞中还含有一个
射线衍射分析显示色胺酮钴配合物晶胞中还含有一个 分子,
分子, 是通过
是通过
 、
、 、
、 与
与 都位于第四周期且最外层电子数相同,但相应单质的熔点,
都位于第四周期且最外层电子数相同,但相应单质的熔点, 、
、 、
、 明显高于
明显高于 ,其原因是
,其原因是(4)
 是一种使用广泛的荧光材料。已知立方
是一种使用广泛的荧光材料。已知立方 的晶胞结构如下图所示:
的晶胞结构如下图所示:
 、
、 点的原子坐标分别为(0,0,0)和(1,
点的原子坐标分别为(0,0,0)和(1, ,
, ),则
),则 点的原子坐标为
点的原子坐标为②立方
 的晶胞参数
的晶胞参数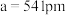 ,则其晶体密度为
,则其晶体密度为 。(列出计算表达式)
。(列出计算表达式)
您最近一年使用:0次
名校
解题方法
9 . 某种化学品的结构如图所示,已知W、X、Y、Z、M均为短周期主族元素,其中W、X、Y在同一周期,Z、M同处另一周期,M原子的最外层电子数等于其电子层数,则下列说法中正确的是
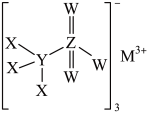
| A.在该化合物中Y和Z的杂化类型不同 |
| B.元素对应简单离子半径大小关系为:M>X>W |
| C.与W同周期的元素中,第一电离能比W大的元素有2种 |
| D.Z、W形成的简单氢化物,分子空间构型相同,分子中化学键的键角不相等 |
您最近一年使用:0次
2024-09-06更新
|
224次组卷
|
3卷引用:湖南省长沙市雅礼中学2024-2025学年高三上学期入学考试化学试题
名校
解题方法
10 . 下列化学用语或表述错误的是
A.乙烯的球棍模型: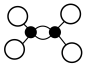 |
B.基态Al原子最高能级的电子云轮廓图: |
| C.在[Ni(NH3)6]SO4中,阴离子的VSEPR模型名称:正四面体形 |
| D.HClO的结构式为H-O-Cl |
您最近一年使用:0次



