解题方法
1 . 下列物质性质排序错误的是
A.酸性: | B.沸点: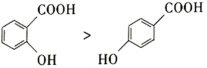 |
C.熔点: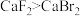 | D.稳定性: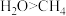 |
您最近半年使用:0次
解题方法
2 . 氮族元素包括氮(N)、磷(P)、砷( )、锑(
)、锑( )、铋(
)、铋( )和镆(
)和镆( )六种,它们的单质及其化合物在工农业生产中有着重要的用途。回答下列问题:
)六种,它们的单质及其化合物在工农业生产中有着重要的用途。回答下列问题:
(1) 基态原子核外电子排布式为
基态原子核外电子排布式为___________ , 基态原子核外有
基态原子核外有___________ 个未成对电子。
(2) 与同周期元素
与同周期元素 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为___________ 。
(3)氮气分子内存在氮氮三键,性质稳定,试从分子结构的角度解释P、 的单质化学性质比
的单质化学性质比 活泼的原因是
活泼的原因是___________ 。
(4) 离子中P的杂化类型为
离子中P的杂化类型为___________ , 分子的空间构型均为
分子的空间构型均为___________ ,其键角依次减小的原因是___________ 。
(5)氮和铜形成的一种二元化合物具有良好的电学和光学性能,其晶胞结构如图所示,则N的配位数为___________ ,该晶体密度为___________  (列出计算式,
(列出计算式, 代表阿伏加德罗常数的值)。
代表阿伏加德罗常数的值)。
 )、锑(
)、锑( )、铋(
)、铋( )和镆(
)和镆( )六种,它们的单质及其化合物在工农业生产中有着重要的用途。回答下列问题:
)六种,它们的单质及其化合物在工农业生产中有着重要的用途。回答下列问题:(1)
 基态原子核外电子排布式为
基态原子核外电子排布式为 基态原子核外有
基态原子核外有(2)
 与同周期元素
与同周期元素 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(3)氮气分子内存在氮氮三键,性质稳定,试从分子结构的角度解释P、
 的单质化学性质比
的单质化学性质比 活泼的原因是
活泼的原因是(4)
 离子中P的杂化类型为
离子中P的杂化类型为 分子的空间构型均为
分子的空间构型均为(5)氮和铜形成的一种二元化合物具有良好的电学和光学性能,其晶胞结构如图所示,则N的配位数为
 (列出计算式,
(列出计算式, 代表阿伏加德罗常数的值)。
代表阿伏加德罗常数的值)。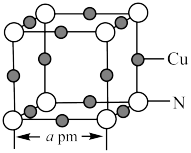
您最近半年使用:0次
解题方法
3 . 下列关于BF3和LiBF4的说法中正确的是
| A.都含有配位键 | B.F-B-F的键角相同 |
| C.B原子的杂化方式相同 | D.B元素的化合价相同 |
您最近半年使用:0次
4 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。下列有关说法正确的是

A.电负性由大到小的顺序: |
B. 中 中 的键角大于该配合物中 的键角大于该配合物中 的键角 的键角 |
| C.该物质中存在的化学键有配位键、共价键、氢键 |
| D.从分子结构的角度分析可知甘氨酸易溶于水 |
您最近半年使用:0次
5 . 我国科学家发现一种新的化合物,结构如下图所示,其中X、Y、Z和W是原子序数依次增大的短周期主族元素。下列说法错误的是

| A.原子半径:Z>W>X>Y | B.第一电离能:X>Y |
| C.X、Z、W氧化物的水化物均为强酸 | D.在右上图中HXX的键角小于180° |
您最近半年使用:0次
6 . 我国某有机所研究团队合成一种盐,其阴离子结构如图所示。短周期主族元素X、Y、Z、R的原子序数依次增大,X、Y、Z的原子序数之和为23,下列有关叙述不正确的是
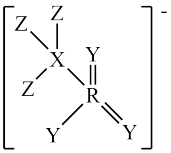
| A.电负性:Z>Y>R | B.简单氢化物的稳定性:Z>Y>X |
C.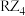 的键角和 的键角和 的键角相等 的键角相等 | D.X的单质可能是共价晶体 |
您最近半年使用:0次
解题方法
7 . 碳和硫的化合物种类繁多,应用广泛。例如 是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
Ⅰ. 曾广泛用作溶剂、灭火剂。
曾广泛用作溶剂、灭火剂。
(1)基态氯原子核外电子的空间运动状态有______ 种。基态碳原子的价电子排布是否可以表示为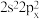 ,
,______ (填“是”或“否”),原因为______ 。
(2) 在
在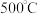 以上时可以与水反应,产生有毒的光气
以上时可以与水反应,产生有毒的光气 常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有
常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有______ (填标号)。
a. 的原子半径更大 b.
的原子半径更大 b. 键的键能更大 c.
键的键能更大 c. 键的极性更大d.
键的极性更大d. 有更多的价层轨道
有更多的价层轨道
光气分子中 的键角
的键角______ (填“大于”、“小于”或“等于”)甲醛分子中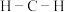 的键角,原因为
的键角,原因为______ 。
Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根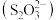 中心原子的杂化方式为
中心原子的杂化方式为______ 。硫代硫酸盐用于矿石提取银时形成 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为______ (填标号),原因为______ 。
a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。 的
的
______ 。原子 的分数坐标为
的分数坐标为 ,
, ,则原子
,则原子 的分数坐标为
的分数坐标为______ 。
 是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。
是一种优良的溶剂,也是用于制造黏胶纤维、玻璃的重要原材料。回答下列问题。Ⅰ.
 曾广泛用作溶剂、灭火剂。
曾广泛用作溶剂、灭火剂。(1)基态氯原子核外电子的空间运动状态有
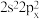 ,
,(2)
 在
在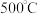 以上时可以与水反应,产生有毒的光气
以上时可以与水反应,产生有毒的光气 常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有
常温遇水水解作用很激烈,产生浑浊和气体。造成两者水解差异的因素有a.
 的原子半径更大 b.
的原子半径更大 b. 键的键能更大 c.
键的键能更大 c. 键的极性更大d.
键的极性更大d. 有更多的价层轨道
有更多的价层轨道光气分子中
 的键角
的键角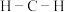 的键角,原因为
的键角,原因为Ⅱ.硫代硫酸盐可用于矿石提取银、鞣制皮革等。
(3)硫代硫酸根
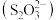 中心原子的杂化方式为
中心原子的杂化方式为 ,该配合物中提供孤电子对的原子为
,该配合物中提供孤电子对的原子为a.端基硫原子 b.中心硫原子 c.氧原子
(4)某硫代硫酸盐的晶胞结构如图。
 的
的
 的分数坐标为
的分数坐标为 ,
, ,则原子
,则原子 的分数坐标为
的分数坐标为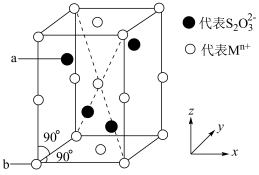
您最近半年使用:0次
8 . 下列比较正确的是
| A.离子半径:S2->Cl->K+ | B.键角:CH4<NH3<H2O |
| C.热稳定性:NH3>PH3>HF | D.酸性:HNO3<H3PO4<H2SiO3 |
您最近半年使用:0次
9 . 回答下列问题
(1)钦铝合金是制造航空航天及武器装备热端部件的理想材料。
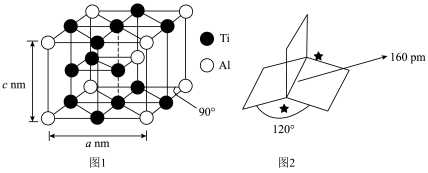
①基态 原子的价电子的轨道表示式
原子的价电子的轨道表示式__________ 。
②下列说法正确的是__________ 。
A.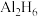 分子中既存在共价键又存在离子键
分子中既存在共价键又存在离子键
B.化学键中离子键成分的百分数: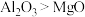
C.第一电离能:
D.测定接近沸点的水蒸气的相对分子质量,测量值偏大的理由是存在相当量的水分子因氢键而相互缔合
③该合金的化学式是__________ ,密度为__________  。
。
(2)碳和氧是构建化合物的常见元素。
某烃结构如图,结合图2所示信息,分析带星号碳的杂化方式为__________ ;带星号碳碳之间的键长比一般碳碳单键的键长要长,请从碳成键轨道的成分角度分析其原因__________ 。
(1)钦铝合金是制造航空航天及武器装备热端部件的理想材料。

①基态
 原子的价电子的轨道表示式
原子的价电子的轨道表示式②下列说法正确的是
A.
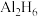 分子中既存在共价键又存在离子键
分子中既存在共价键又存在离子键B.化学键中离子键成分的百分数:
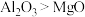
C.第一电离能:

D.测定接近沸点的水蒸气的相对分子质量,测量值偏大的理由是存在相当量的水分子因氢键而相互缔合
③该合金的化学式是
 。
。(2)碳和氧是构建化合物的常见元素。
某烃结构如图,结合图2所示信息,分析带星号碳的杂化方式为
您最近半年使用:0次
昨日更新
|
26次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
解题方法
10 . 溴代叔丁烷与乙醇的反应进程中的能量变化如图所示。下列说法正确的是
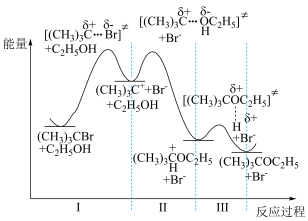
| A.溴代叔丁烷与乙醇的反应为吸热 |
| B.溴代叔丁烷和乙醇的总反应速率由反应Ⅲ决定 |
| C.氯代叔丁烷和乙醇中发生相似的反应,则反应I的活化能将增大 |
D.由该反应原理可推知,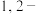 二溴乙烷和乙二醇反应可制得环丁烷 二溴乙烷和乙二醇反应可制得环丁烷 |
您最近半年使用:0次



