1 .  、
、 、
、 、
、 是生命元素。请回答:
是生命元素。请回答:
(1)下列说法正确的是___________。
(2) 键中
键中 的杂化方式
的杂化方式___________ ;画出 的结构式(用“→”表示配位键)
的结构式(用“→”表示配位键)___________ 。
(3) 、
、 、
、 与
与 能形成一种阳离子
能形成一种阳离子 ,呈轴向狭长的八面体结构(如下图所示)。
,呈轴向狭长的八面体结构(如下图所示)。 的化学式为
的化学式为___________ ,加热时 首先失去的组分是
首先失去的组分是___________ ,该组分的分子空间构型为___________ 。
②可选用___________ (填“ 射线衍射仪”或“质谱仪”)判断
射线衍射仪”或“质谱仪”)判断 中的
中的 键是否相同。
键是否相同。
③ 转化为
转化为 阳离子时,需逐级结合
阳离子时,需逐级结合 分子,各级反应的平衡常数分别为
分子,各级反应的平衡常数分别为 ,
, ,
, ,
,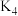 ,如
,如 。
。
请从结构角度解释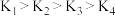 的原因
的原因___________ 。
 、
、 、
、 、
、 是生命元素。请回答:
是生命元素。请回答:(1)下列说法正确的是___________。
A.第一电离能: |
B.电负性: |
C.酸性: |
D.键角: |
(2)
 键中
键中 的杂化方式
的杂化方式 的结构式(用“→”表示配位键)
的结构式(用“→”表示配位键)(3)
 、
、 、
、 与
与 能形成一种阳离子
能形成一种阳离子 ,呈轴向狭长的八面体结构(如下图所示)。
,呈轴向狭长的八面体结构(如下图所示)。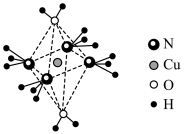
 的化学式为
的化学式为 首先失去的组分是
首先失去的组分是②可选用
 射线衍射仪”或“质谱仪”)判断
射线衍射仪”或“质谱仪”)判断 中的
中的 键是否相同。
键是否相同。③
 转化为
转化为 阳离子时,需逐级结合
阳离子时,需逐级结合 分子,各级反应的平衡常数分别为
分子,各级反应的平衡常数分别为 ,
, ,
, ,
,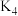 ,如
,如 。
。请从结构角度解释
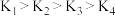 的原因
的原因
您最近半年使用:0次
2 . 砜类化合物是一类重要的有机合成中间体。一定条件下,由化合物I制取砜类化合物II的合成路线如下:

| A.化合物I和II均能使酸性高锰酸钾溶液褪色 |
| B.化合物I分子的一氯代物有5种 |
| C.化合物I分子中所有碳原子一定在同一平面内 |
| D.化合物I和II中S原子的杂化轨道类型不同 |
您最近半年使用:0次
3 . 民得维(VV116)是我国科学家研发的新冠特效药,其结构如图所示。关于该化合物下列说法不正确的是
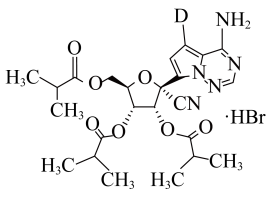
| A.该化合物是离子化合物 | B.该化合物中氮均为sp2和sp3杂化 |
| C.该化合物能与强酸或强碱反应 | D.该化合物中H和D互为同位素 |
您最近半年使用:0次
4 .  重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子的氮原子上,具体反应历程如图所示。
重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子的氮原子上,具体反应历程如图所示。
 重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子的氮原子上,具体反应历程如图所示。
重排是酮肟在一定条件下生成酰胺的反应,机理中与羟基处于反位的基团迁移到缺电子的氮原子上,具体反应历程如图所示。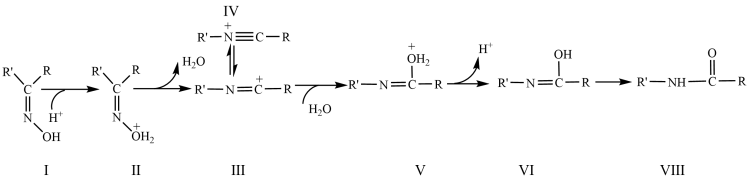
A.物质Ⅰ中碳原子和氮原子均为 杂化 杂化 | B.物质Ⅶ不能和 溶液反应 溶液反应 |
C. 在该反应过程中作催化剂 在该反应过程中作催化剂 | D.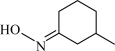 生上述反应生成 生上述反应生成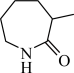 |
您最近半年使用:0次
5 . 科学家合成了一种含硼阴离子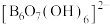 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是
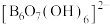 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是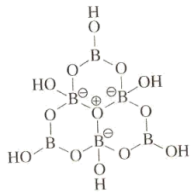
| A.基态硼原子的核外电子的空间运动状态有3种 |
| B.电负性大小为:O>B>H |
| C.该结构中硼原子的杂化方式为sp2、sp3 |
| D.该结构中共有4种不同化学环境的氧原子 |
您最近半年使用:0次
6 . 化学处处呈现美。下列说法不正确的是
A.金刚石中的碳原子采取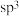 杂化轨道形成空间网状结构 杂化轨道形成空间网状结构 |
B. 溶液与 溶液与 溶液反应生成蓝色 溶液反应生成蓝色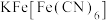 沉淀 沉淀 |
C.缺角的 晶体在饱和 晶体在饱和 溶液中变为完美立方体块,体现晶体的自范性 溶液中变为完美立方体块,体现晶体的自范性 |
| D.绚烂烟花的产生是电子由基态跃迁到激发态时,能量以光的形式释放引起的 |
您最近半年使用:0次
7 . 我国科研工作者成功合成了一种含铜(II)高效催化剂,该催化剂的部分结构如下图所示,该部分结构中的所有原子共平面。下列说法正确的是

| A.铜元素位于周期表的d区 |
| B.该催化剂中铜的配位数为3 |
| C.该部分结构中C、N原子的杂化类型相同 |
| D.基态N原子核外有7种不同空间运动状态的电子 |
您最近半年使用:0次
解题方法
8 . 金属材料对于促进生产发展、改善人类生活发挥了巨大作用。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式___________ 。涩法冶炼是以赤铜矿( )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为___ 。
(3)已知: 晶胞为立方体形,边长为
晶胞为立方体形,边长为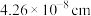 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为___________ 个。计算 晶体的密度
晶体的密度
___________  (结果保留两位小数)。
(结果保留两位小数)。
(4)基态Na原子的价层电子轨道表示式为___________ 。
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:
 ,加入
,加入 的目的是
的目的是___________ 。
(6)除去 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是___________ 。
Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7) 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是___________ 。
(8) 易与
易与 形成
形成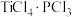 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。
(9)钛溶于盐酸制得的三氯化钛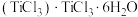 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、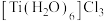 (紫色),两者配位数
(紫色),两者配位数___________ (选填“相同”或“不同”),绿色晶体中配体是___________ 。
I.钢是人类使用最早的金属之一,至今仍被广泛应用于电气、电子等领域。
(1)写出基态Cu原子的核外电子排布式
 )精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。
)精矿为主要原料,通过浸出、置换、电解等流程制备高坑度的工艺。(2)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为
(3)已知:
 晶胞为立方体形,边长为
晶胞为立方体形,边长为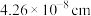 。根据图示,每个
。根据图示,每个 晶胞中含O原子的数目为
晶胞中含O原子的数目为 晶体的密度
晶体的密度
 (结果保留两位小数)。
(结果保留两位小数)。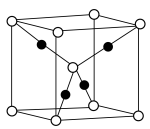
(4)基态Na原子的价层电子轨道表示式为
(5)NaCl熔点为:800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为:

 ,加入
,加入 的目的是
的目的是(6)除去
 粉末中混有的少量
粉末中混有的少量 的方法是
的方法是Ⅲ.钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(7)
 原子的价电子排布式为
原子的价电子排布式为 ,它在元素周期表中的位置是
,它在元素周期表中的位置是(8)
 易与
易与 形成
形成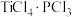 。下列关于
。下列关于 分子说法错误的是___________。
分子说法错误的是___________。| A.键角为120° | B.是极性分子 |
C.含有 键 键 | D.中心原子采取 杂化 杂化 |
(9)钛溶于盐酸制得的三氯化钛
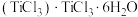 晶体有两种异构体:
晶体有两种异构体: (绿色)、
(绿色)、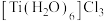 (紫色),两者配位数
(紫色),两者配位数
您最近半年使用:0次
9 . 空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉障碍的叫霾。科研人员提出了雾霾微颗粒中硫酸盐(含SO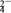 、HSO
、HSO )生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
)生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
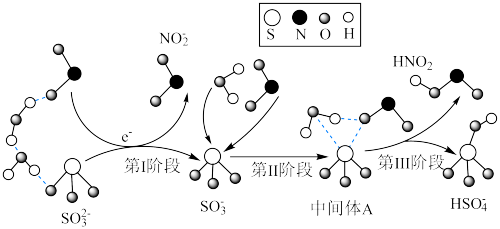
A.SO 和NO 和NO 的中心原子的杂化轨道类型分别是:sp3、sp2 的中心原子的杂化轨道类型分别是:sp3、sp2 |
| B.整个过程中有H2O参加反应,而且包含了硫氧键的断裂与形成 |
C.1molSO 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA |
D.硫酸盐转化过程中发生的总反应方程式为:SO +2NO2+H2O=HSO +2NO2+H2O=HSO +NO +NO +HNO2 +HNO2 |
您最近半年使用:0次
解题方法
10 . X、Y、Z、M为原子序数依次增大的四种短周期主族元素,X和Z基态原子L层上均有2个未成对电子,Z与M同主族;Q位于元素周期表中第四周期,基态原子有1个电子未成对且内层电子全满。 能与
能与 形成
形成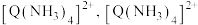 中2个
中2个 被2个
被2个 取代可得两种不同的结构。
取代可得两种不同的结构。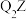 晶胞如下图所示。下列说法
晶胞如下图所示。下列说法不 正确的是
 能与
能与 形成
形成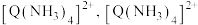 中2个
中2个 被2个
被2个 取代可得两种不同的结构。
取代可得两种不同的结构。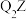 晶胞如下图所示。下列说法
晶胞如下图所示。下列说法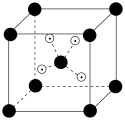
A.简单氢化物的沸点: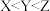 | B. 的空间构型为正四面体形 的空间构型为正四面体形 |
C.原子半径: | D.每个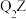 晶胞中含4个 晶胞中含4个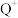 |
您最近半年使用:0次



