名校
解题方法
1 . X、Y、Z、Q、W为五种短周期主族元素,且原子序数依次增大。Z、W位于同一主族,Q、W位于同一周期且相邻。X是周期表中原子半径最小的元素,Y的同位素可用于测定文物年代,Z元素的价层电子排布为nsnnp2n。下列说法正确的是
| A.电负性:Z>Q>W | B.键角:WZ3>X2W>X2Z |
| C.YW2、X2Z2均为非极性分子 | D.Q和Z可形成原子比为2∶3、2∶5的两种分子 |
您最近半年使用:0次
解题方法
2 . 铜及其化合物在生活、生产中用途广泛。以黄铜矿为原料冶炼铜涉及多个反应,其中一个反应为
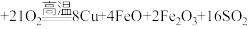 。回答下列问题:
。回答下列问题:
(1)基态铜原子的价层电子的轨道表示式(电子排布图)为______________ ,基态铜原子核外电子的空间运动状态(原子轨道)有__________ 种。
(2)高温下CuO能转化为 的原因是
的原因是_____________ (从原子结构角度分析)。
(3) 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是___________ ,属于极性分子的是___________ , 、
、 、
、 、
、 四种含硫微粒的空间结构分别为
四种含硫微粒的空间结构分别为____________ 、____________ 、____________ 、____________ 。
(4) 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是_______________ ,1360℃是__________ 的熔点。
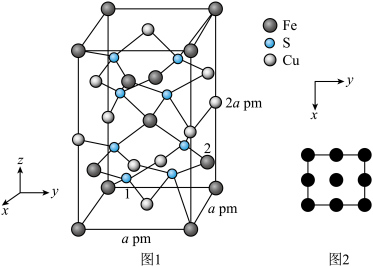
(5) 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为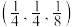 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为____________ 。晶胞参数分别为a pm,a pm、2a pm, 晶体的密度为
晶体的密度为___________  (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。

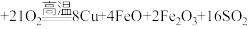 。回答下列问题:
。回答下列问题:(1)基态铜原子的价层电子的轨道表示式(电子排布图)为
(2)高温下CuO能转化为
 的原因是
的原因是(3)
 、
、 、
、 、
、 四种含硫微粒中,中心原子为
四种含硫微粒中,中心原子为 杂化的是
杂化的是 、
、 、
、 、
、 四种含硫微粒的空间结构分别为
四种含硫微粒的空间结构分别为(4)
 、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。
、FeO的熔点是下列两个数值中的一个:1360℃、1565℃。 、FeO两种氧化物的晶体类型都是
、FeO两种氧化物的晶体类型都是(5)
 晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为
晶体的晶胞结构如图1所示。晶胞中Fe的投影位置如图2所示。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图1中原子1(硫原子)的分数坐标为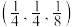 ,则原子2(铁原子)的分数坐标为
,则原子2(铁原子)的分数坐标为 晶体的密度为
晶体的密度为 (列出计算表达式,设阿伏加德罗常数的值为
(列出计算表达式,设阿伏加德罗常数的值为 )。
)。
您最近半年使用:0次
解题方法
3 . 科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近半年使用:0次
名校
解题方法
4 . 根据要求回答下列问题:
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中阴离子的空间构型是___________ ,中心原子的杂化类型为___________ 。
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。SO2的VSEPR模型为___________ ;SO3的中心原子的杂化类型为___________ ;N2O与CO2互为等电子体,且N2O中O只与一个N相连,分子中的σ键和π键数目之比是___________ 。
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。___________ 能沿着其中的金属原子链流动。
(1)LiAlH4是有机合成中常用的还原剂,LiAlH4中阴离子的空间构型是
(2)碳氧化物、氨氧化物、二氧化硫的处理和应用是世界各国研究的热点问题。SO2的VSEPR模型为
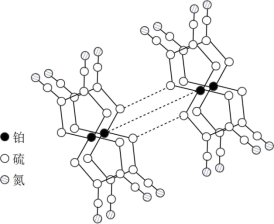
(3)某研究小组将平面形的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
您最近半年使用:0次
名校
解题方法
5 . 下列有关说法中正确的是
A.如图所示,HCl分子由H原子的1s轨道和Cl原子的3p轨道重叠形成 |
| B.ZnCO3入药可用于治疗皮肤炎症,ZnCO3中阴离子空间结构为四面体形 |
| C.基态As原子的电子排布式和价电子排布式分别为[Ar]3d104s24p3和4s24p3 |
| D.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸的高的主要原因 |
您最近半年使用:0次
名校
解题方法
6 . 下列图示或化学用语错误 的是
A.羟基的电子式: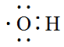 |
B.H2O的VSEPR模型: |
C.Mn2+的价电子的轨道表示式: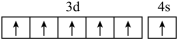 |
D.顺-2-丁烯的球棍模型为 |
您最近半年使用:0次
名校
7 . H与O可以形成H2O和H2O2两种化合物其中H2O2的分子结构如图所示,H+可与H2O形成H3O+。下列说法错误的是

A. 分子中两个 分子中两个 原子均采取 原子均采取 杂化轨道成键 杂化轨道成键 |
B.相同条件下, 在水中的溶解度大于在 在水中的溶解度大于在 中的溶解度 中的溶解度 |
C.液态水中的作用力由强到弱的顺序是:氢键 范德华力 范德华力 |
D. 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近半年使用:0次
名校
解题方法
8 . 化合物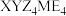 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
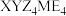 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是| A.简单离子半径:Y>E>Z | B.简单氢化物沸点: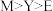 |
C.第一电离能: | D.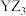 和 和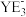 空间结构均为三角锥形 空间结构均为三角锥形 |
您最近半年使用:0次
名校
9 . 利用离子液体 可电沉积还原金属Ge,其中
可电沉积还原金属Ge,其中 的结构如图所示。下列有关说法错误的是
的结构如图所示。下列有关说法错误的是
 可电沉积还原金属Ge,其中
可电沉积还原金属Ge,其中 的结构如图所示。下列有关说法错误的是
的结构如图所示。下列有关说法错误的是
| A.该离子液体能导电 | B. 的空间构型为正四面体形 的空间构型为正四面体形 |
C.该物质中碳原子的杂化类型为 | D.电解沉积金属时,金属在阴极析出 |
您最近半年使用:0次
昨日更新
|
135次组卷
|
2卷引用:安徽省池州市2024届高三教学质量统一监测(二模)化学试题
解题方法
10 . 已知反应 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 。设
。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A. 的空间构型为直线形 的空间构型为直线形 | B.电负性: |
C. 在熔融状态下均可导电 在熔融状态下均可导电 | D. 冰中含有氢键数目为 冰中含有氢键数目为 |
您最近半年使用:0次



