解题方法
1 . 近年来,光催化剂的研究是材料领域的热点方向。一种Ru配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法正确的是
转化为HCOOH。下列说法正确的是
 转化为HCOOH。下列说法正确的是
转化为HCOOH。下列说法正确的是
A.该Ru配合物中第二周期元素的第一电离能由大到小的顺序为 |
B.该Ru配合物中C原子、N原子的杂化方式均为 |
| C.该配合物中Ru的配体分别是有机物、一氧化碳和氯原子 |
D.HCOOH的沸点比 高,主要原因是HCOOH分子间存在范德华力和氢键,而 高,主要原因是HCOOH分子间存在范德华力和氢键,而 分子间只有范德华力 分子间只有范德华力 |
您最近半年使用:0次
名校
解题方法
2 . 烟气脱硝技术是烟气治理的发展方向和研究热点。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
则该反应的ΔH=___________ kJ/mol。
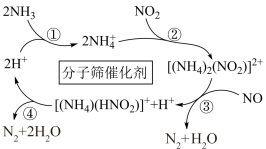
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。___________ 。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为___________ 。
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为___________ (用“→”标出其中的配位键)
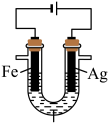
(4)以连二硫酸根(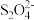 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:___________ 。
②NO吸收转化后的主要产物为 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为___________ mL。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
| 化学键 | NO中的氮氧键 | N-H | N≡N | O-H |
| 键能(kJ/mol) | a | b | c | d |
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为
(4)以连二硫酸根(
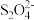 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示: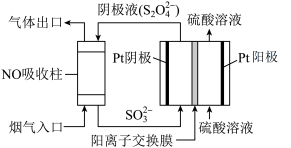
②NO吸收转化后的主要产物为
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
您最近半年使用:0次
解题方法
3 . 下列实验方案不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明 | 向盛有浓度均为 的 的 和 和 混合溶液的试管中滴加几滴 混合溶液的试管中滴加几滴 溶液,振荡,观察沉淀颜色 溶液,振荡,观察沉淀颜色 |
| B | 制备 晶体 晶体 | 向 溶液中加入95%的乙醇 溶液中加入95%的乙醇 |
| C | 比较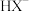 的电离程度与水解程度的大小 的电离程度与水解程度的大小 | 室温下,用 计测量一定浓度某弱酸盐 计测量一定浓度某弱酸盐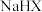 溶液的 溶液的 |
| D | 氧化性: | 向 溶液中通入少量氯气,然后再加入少量苯萃取上层为橙红色 溶液中通入少量氯气,然后再加入少量苯萃取上层为橙红色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 某兴趣小组探究电镀银实验。回答下列问题:
I.实验准备。
(1)用 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是___________ (填字母)。___________ 。
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与 浓度有关。
浓度有关。
【查阅资料】
络合反应: ,
, 。
。
【设计实验】
【问题讨论】
(3)实验a中,溶液变红色的可能原因是 和
和___________ (用离子方程式表示,已知氧化性: )。
)。
(4)①实验a、b的阴极都伴随有气泡,其原因是___________ (写电极反应式)。
②实验b比实验a产生的镀层光亮、致密,其原理是___________ 。
③一段时间后,实验b中 平衡不移动,其原因是
平衡不移动,其原因是___________ 。
【实验结论】
其他条件不变, 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。
Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与
 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。
表2:其他条件不变,温度对镀层外观的影响。
(5)表1中 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是___________ ;
表2中温度为 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是___________ 。
Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。
(6)使用新配方可以达到同样的目的,其原理是___________ 。已知: 。
。
I.实验准备。
(1)用
 固体配制
固体配制 溶液,不需要使用的仪器是
溶液,不需要使用的仪器是A. B.
B.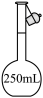 C.
C. D.
D. E.
E.
Ⅱ.探究银离子对镀层的影响。
【提出猜想】
镀层外观与
 浓度有关。
浓度有关。【查阅资料】
络合反应:
 ,
, 。
。【设计实验】
| 实验 | 装置 | 现象 |
| a |
 的 的 溶液(含少量 溶液(含少量 ) ) | 阴极表面有疏松的黑色物质生成并伴随有无色气泡,一段时间后,取阴极区电解质溶液于试管,滴加 溶液,溶液变为红色。 溶液,溶液变为红色。 |
| b |
 的 的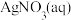 与过量 与过量 混合(含少量 混合(含少量 ) ) | 阴极表面有光亮、致密的银白色物质生成,仍然有少量无色气泡。一段时间后,取少量阴极区溶液于试管,滴加 溶液,溶液不变红。 溶液,溶液不变红。 |
(3)实验a中,溶液变红色的可能原因是
 和
和 )。
)。(4)①实验a、b的阴极都伴随有气泡,其原因是
②实验b比实验a产生的镀层光亮、致密,其原理是
③一段时间后,实验b中
 平衡不移动,其原因是
平衡不移动,其原因是【实验结论】
其他条件不变,
 浓度很小时,银镀层光亮、致密。
浓度很小时,银镀层光亮、致密。Ⅲ.探究温度、含量对镀层的影响。
表1:其他条件不变,与

 溶液等体积混合的溶液中含量对镀层外观的影响。
溶液等体积混合的溶液中含量对镀层外观的影响。 含量( 含量( ) ) | 镀层外观表象 |
| 10 | 镀层模糊,无光泽 |
| 25 | 镀层呈雾状,光泽不足 |
| 50 | 镀层光亮、致密 |
温度/ | 镀层外观表象 |
| 25 | 光亮 |
| 35 | 光亮 |
| 40 | 光亮 |
| 55 | 光亮不均匀 |
(5)表1中
 含量为
含量为 时,镀层模糊、无光泽的原因是
时,镀层模糊、无光泽的原因是表2中温度为
 时镀层光亮不均匀的主要原因是
时镀层光亮不均匀的主要原因是Ⅳ.探究新配方电镀银。
由于电镀液使用氰化钾,在电镀过程中会产生有毒气体,以及废液含剧毒的氰化物,不符合环境要求。由
 溶液和
溶液和 溶液组成电镀液也可以得到光亮、致密的镀层。
溶液组成电镀液也可以得到光亮、致密的镀层。(6)使用新配方可以达到同样的目的,其原理是
 。
。
您最近半年使用:0次
5 . 氨是最基本的化工原料,常用于制液氮、氨水、硝酸、铵盐和胺类等。
(1)工业合成氨是人类科学技术的一项重大突破,其反应如下: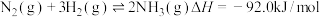
根据下列键能数据,结合上述反应数据,计算 的键能是
的键能是___________  。
。
(2)合成氨工业中,原料气( 及少量
及少量 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中 ,其反应为:
,其反应为: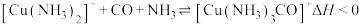 。
。
①配离子 的中心离子是
的中心离子是___________ ,配位数是___________ 。
②铜氨溶液吸收 适宜的生产条件:
适宜的生产条件:___________ 温、___________ 压。(填“高”“低”)
(3)恒温恒压条件下,向容器中通入 和
和 ,合成氨反应用摩尔分数表示的平衡常数
,合成氨反应用摩尔分数表示的平衡常数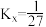 ,达到平衡时
,达到平衡时 的转化率为
的转化率为___________ (保留3位有效数字)。(已知反应的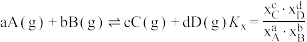 ,物质ⅰ的摩尔分数
,物质ⅰ的摩尔分数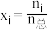 ,
,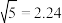 )。
)。
(4)制备 时所需的
时所需的 可以通过反应合成,但缺
可以通过反应合成,但缺 。有学者倡议:常温下,把石膏矿中
。有学者倡议:常温下,把石膏矿中 (Ⅱ)转化为难溶的
(Ⅱ)转化为难溶的 ,留下的
,留下的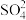 和
和 形成
形成 ,反应方程式如下:
,反应方程式如下:  ,化学平衡常数为
,化学平衡常数为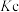 ,用下列相关
,用下列相关 的符号来表示
的符号来表示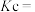
___________ 。通过计算反应的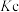 判断以上倡议
判断以上倡议___________ (填“可行”或“不可行”)。
(已知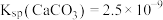 、
、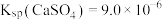 、
、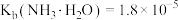 、
、 的
的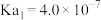 、
、 、
、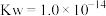 )
)
(5) 与镓
与镓 在高温下生成
在高温下生成 ,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被
,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被 原子代替,顶点和面心的碳原子被
原子代替,顶点和面心的碳原子被 原子代替。
原子代替。 原子坐标为
原子坐标为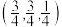 ,则
,则 原子坐标为
原子坐标为___________ 。
②若 为阿伏伽德罗常数的值,
为阿伏伽德罗常数的值, 晶胞中
晶胞中 原子与
原子与 原子之间最短的核间距离是
原子之间最短的核间距离是 ,则
,则 晶体的密度为
晶体的密度为___________  (只列计算式)。
(只列计算式)。
(1)工业合成氨是人类科学技术的一项重大突破,其反应如下:
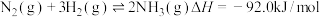
根据下列键能数据,结合上述反应数据,计算
 的键能是
的键能是 。
。| 化学键 |  |  |
键能 | 946 | 436 |
(2)合成氨工业中,原料气(
 及少量
及少量 的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中
的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中 ,其反应为:
,其反应为: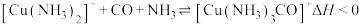 。
。①配离子
 的中心离子是
的中心离子是②铜氨溶液吸收
 适宜的生产条件:
适宜的生产条件:(3)恒温恒压条件下,向容器中通入
 和
和 ,合成氨反应用摩尔分数表示的平衡常数
,合成氨反应用摩尔分数表示的平衡常数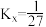 ,达到平衡时
,达到平衡时 的转化率为
的转化率为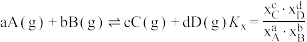 ,物质ⅰ的摩尔分数
,物质ⅰ的摩尔分数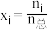 ,
,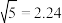 )。
)。(4)制备
 时所需的
时所需的 可以通过反应合成,但缺
可以通过反应合成,但缺 。有学者倡议:常温下,把石膏矿中
。有学者倡议:常温下,把石膏矿中 (Ⅱ)转化为难溶的
(Ⅱ)转化为难溶的 ,留下的
,留下的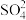 和
和 形成
形成 ,反应方程式如下:
,反应方程式如下:  ,化学平衡常数为
,化学平衡常数为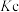 ,用下列相关
,用下列相关 的符号来表示
的符号来表示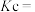
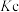 判断以上倡议
判断以上倡议(已知
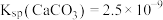 、
、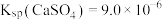 、
、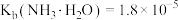 、
、 的
的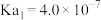 、
、 、
、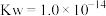 )
)(5)
 与镓
与镓 在高温下生成
在高温下生成 ,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被
,氮化镓晶胞结构可看作金刚石晶胞内部的碳原子被 原子代替,顶点和面心的碳原子被
原子代替,顶点和面心的碳原子被 原子代替。
原子代替。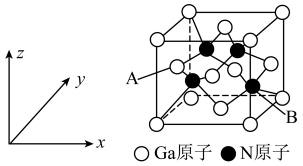
 原子坐标为
原子坐标为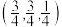 ,则
,则 原子坐标为
原子坐标为②若
 为阿伏伽德罗常数的值,
为阿伏伽德罗常数的值, 晶胞中
晶胞中 原子与
原子与 原子之间最短的核间距离是
原子之间最短的核间距离是 ,则
,则 晶体的密度为
晶体的密度为 (只列计算式)。
(只列计算式)。
您最近半年使用:0次
6 . 席夫碱A和含席夫碱A的红光铂配合物的分子结构如图所示。

A.元素的电负性大小为: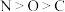 |
B.席夫碱A分子内可以形成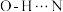 氢键 氢键 |
C.红光铂配合物分子中 的化合价为 的化合价为 |
D.红光铂配合物分子中 键的类型为离子键 键的类型为离子键 |
您最近半年使用:0次
7日内更新
|
53次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题
7 . 下列各组离子在指定条件下可能大量共存的是
A.含有 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.能使甲基橙变红的溶液中: 、 、 、 、 、 、 |
C.水电离出的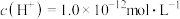 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.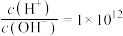 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
解题方法
8 . 下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
 | 向某钠盐粉末上滴加浓盐酸,将产生的气体通入品红溶液 | 溶液褪色 | 气体一定是 |
 | 向 溶液中滴加盐酸 溶液中滴加盐酸 | 产生浑浊 |  的非金属性比 的非金属性比 强 强 |
| C | 将SO3、SO2混合气体通入 溶液中 溶液中 | 生成白色沉淀 | 沉淀是BaSO3、BaSO4 |
| D | 向硫酸铜溶液中依次加入足量氨水和适量乙醇 | 最终析出深蓝色晶体 | 乙醇降低硫酸四氨合铜晶体的溶解度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为___ 。
(2)有下列实验:___ 。深蓝色晶体的化学式为___ 。
②写出蓝色沉淀溶解成深蓝色溶液的离子方程式___ 。
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角___ (填“大”或“小”)。[Cu(NH3)4]SO4中存在的化学键类型有___ (填标号)。
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___ (填标号)。
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:___ (用“→”或“—”将配位键表示出来)。
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为
(2)有下列实验:

②写出蓝色沉淀溶解成深蓝色溶液的离子方程式
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:
您最近半年使用:0次
解题方法
10 . 科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近半年使用:0次