1 . 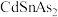 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:
(1) 、
、 、
、 键角由大到小的顺序为
键角由大到小的顺序为___________ 。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有
配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有___________ mol,该螯合物中N的杂化方式有___________ 种。 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
___________ 个Sn,找出距离 最近的Sn
最近的Sn___________ (用分数坐标表示)。 晶体中与单个Sn键合的As有
晶体中与单个Sn键合的As有___________ 个。
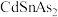 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:(1)
 、
、 、
、 键角由大到小的顺序为
键角由大到小的顺序为(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有
配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有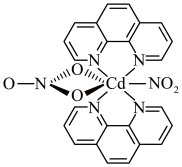
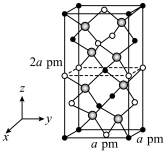
 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。| 坐标原子 | X | y | Z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |
 最近的Sn
最近的Sn 晶体中与单个Sn键合的As有
晶体中与单个Sn键合的As有
您最近半年使用:0次
2 . 磷酸亚铁锂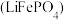 和锰酸锂
和锰酸锂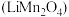 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性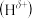 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性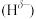 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: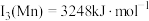 ,
,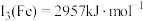 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
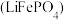 和锰酸锂
和锰酸锂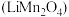 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性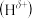 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性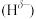 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
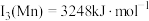 ,
,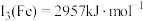 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近半年使用:0次
3 . Cu可形成多种配合物,某同学在探究配合物的形成时做了以下实验,根据下列信息回答问题:
(1)将无水硫酸铜溶解于水中,溶液呈蓝色,向其中加入浓氨水,产生蓝色沉淀的离子反应方程式___________ ,继续加入浓氨水,沉淀消失,沉淀溶解的离子反应方程式___________ 。
(2)根据以上实验过程,判断 和
和 与
与 的配位能力:
的配位能力:
___________ (填“>”“=”或“<”) 。
。
(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为___________ 。
(4)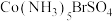 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。
溶液时,则无明显现象。
则第一种配合物的结构式可表示为___________ 。(提示: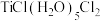 这种配合物的结构可表示为
这种配合物的结构可表示为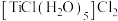 );若
);若 均为配体,则在第二种配合物的溶液中滴加
均为配体,则在第二种配合物的溶液中滴加 溶液,产生的现象是
溶液,产生的现象是___________ 。
(1)将无水硫酸铜溶解于水中,溶液呈蓝色,向其中加入浓氨水,产生蓝色沉淀的离子反应方程式
(2)根据以上实验过程,判断
 和
和 与
与 的配位能力:
的配位能力:
 。
。(3)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为
(4)
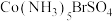 可形成两种钴的配合物。已知
可形成两种钴的配合物。已知 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加 溶液时,则无明显现象。
溶液时,则无明显现象。则第一种配合物的结构式可表示为
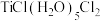 这种配合物的结构可表示为
这种配合物的结构可表示为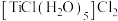 );若
);若 均为配体,则在第二种配合物的溶液中滴加
均为配体,则在第二种配合物的溶液中滴加 溶液,产生的现象是
溶液,产生的现象是
您最近半年使用:0次
4 . 元素周期表中,第四周期元素单质及其化合物在化工生产和研究中有重要的应用。
(1)钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
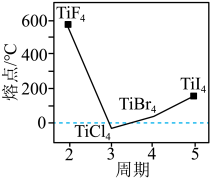
①钛能与卤素单质发生反应,生成用途多样的卤化钛。钛的不同四卤化物熔点如图所示,利用晶体知识解释它们熔点变化的原因_____ 。 ),可作为聚丙烯生产过程中的催化剂。
),可作为聚丙烯生产过程中的催化剂。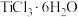 晶体有两种异构体:
晶体有两种异构体: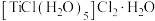 (绿色)、
(绿色)、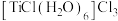 (紫色),两者配位数
(紫色),两者配位数_____ (选填“相同”或“不同”),绿色晶体中配体是_____ 。
(2)在ZnO催化作用下,呋喃(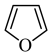 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯(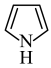 ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大π键的原子数,n代表大π键中的电子数,则吡咯中大π键可以表示为
表示,其中m表示参与形成大π键的原子数,n代表大π键中的电子数,则吡咯中大π键可以表示为_____ 。呋喃的熔、沸点低于吡咯的原因是_____ 。
(3) 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角_____  中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。
(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的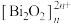 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为_____ 。晶胞棱边夹角均为90°,则晶体密度的计算式为_____  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
①钛能与卤素单质发生反应,生成用途多样的卤化钛。钛的不同四卤化物熔点如图所示,利用晶体知识解释它们熔点变化的原因
 ),可作为聚丙烯生产过程中的催化剂。
),可作为聚丙烯生产过程中的催化剂。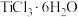 晶体有两种异构体:
晶体有两种异构体: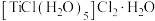 (绿色)、
(绿色)、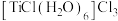 (紫色),两者配位数
(紫色),两者配位数(2)在ZnO催化作用下,呋喃(
 )可与氨反应,转化为吡咯(
)可与氨反应,转化为吡咯( ),吡咯分子中所有原子共平面,已知大π键可以用
),吡咯分子中所有原子共平面,已知大π键可以用 表示,其中m表示参与形成大π键的原子数,n代表大π键中的电子数,则吡咯中大π键可以表示为
表示,其中m表示参与形成大π键的原子数,n代表大π键中的电子数,则吡咯中大π键可以表示为(3)
 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为 。
。 中
中 键角
键角 中
中 键角(填“大于”“小于”或“等于”)。
键角(填“大于”“小于”或“等于”)。(4)硒氧化铋是一类:全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
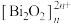 层与带负电的
层与带负电的 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。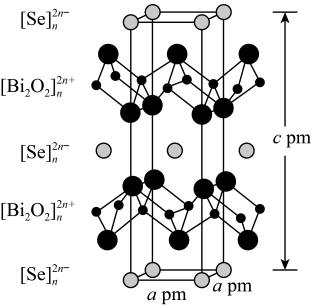
您最近半年使用:0次
名校
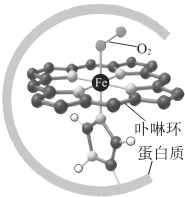
5 . 已知:血红蛋白可与 结合,血红蛋白更易与CO配位,血红蛋白与
结合,血红蛋白更易与CO配位,血红蛋白与 配位示意如图所示,血红蛋白(Hb)与
配位示意如图所示,血红蛋白(Hb)与 、CO结合的反应可表示为①
、CO结合的反应可表示为①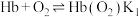
 ;②
;②
 。
。
 结合,血红蛋白更易与CO配位,血红蛋白与
结合,血红蛋白更易与CO配位,血红蛋白与 配位示意如图所示,血红蛋白(Hb)与
配位示意如图所示,血红蛋白(Hb)与 、CO结合的反应可表示为①
、CO结合的反应可表示为①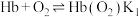
 ;②
;②
 。
。
A.相同温度下,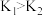 |
B.血红蛋白结合 后Fe的配位数为6 后Fe的配位数为6 |
C.已知反应 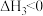 ,则 ,则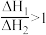 |
| D.高压氧舱可治疗CO中毒 |
您最近半年使用:0次
今日更新
|
71次组卷
|
2卷引用:河北省衡水市第十三中学2023-2024学年高三上学期测评三 化学试卷
6 . N元素能形成多种化合物,它们之间可以发生相互转化,如: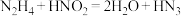 。请回答下列问题:
。请回答下列问题:
(1)N与O的第一电离能较小的是___________ 。
(2)N的基态原子的电子排布中,有___________ 个运动状态不同的未成对电子。
(3)叠氮酸 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是___________ 。
(4) 中N原子的杂化类型是
中N原子的杂化类型是___________ 。
(5)① 是一种很好的配体,则能提供孤电子对的
是一种很好的配体,则能提供孤电子对的___________ (填字母)。
A.仅有氧原子
B.仅有氮原子
C.是氧原子或氮原子
② 与钴盐通过配位键形成的
与钴盐通过配位键形成的 能与
能与 结合生成黄色
结合生成黄色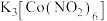 沉淀,此方法可用于检验溶液中的
沉淀,此方法可用于检验溶液中的 ,写出该配合物中钴离子的电子排布式:
,写出该配合物中钴离子的电子排布式:___________ 。
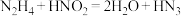 。请回答下列问题:
。请回答下列问题:(1)N与O的第一电离能较小的是
(2)N的基态原子的电子排布中,有
(3)叠氮酸
 在常温下是液体,沸点相对较高,为308.8K,主要原因是
在常温下是液体,沸点相对较高,为308.8K,主要原因是(4)
 中N原子的杂化类型是
中N原子的杂化类型是(5)①
 是一种很好的配体,则能提供孤电子对的
是一种很好的配体,则能提供孤电子对的A.仅有氧原子
B.仅有氮原子
C.是氧原子或氮原子
②
 与钴盐通过配位键形成的
与钴盐通过配位键形成的 能与
能与 结合生成黄色
结合生成黄色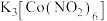 沉淀,此方法可用于检验溶液中的
沉淀,此方法可用于检验溶液中的 ,写出该配合物中钴离子的电子排布式:
,写出该配合物中钴离子的电子排布式:
您最近半年使用:0次
名校
解题方法
7 . 含金的配合物在工业生产中有重要用途。一种金的配合物的晶体结构如图所示,下列说法错误的是

| A.该化合物的化学式为CsAuCl3 |
| B.Cs+的配位数为12 |
| C.Au是第ⅠB族的过渡金属 |
| D.1mol/L该配合物水溶液的电阻率较高 |
您最近半年使用:0次
解题方法
8 . 催化丙烯制醛的反应机理如图所示,下列说法正确的是
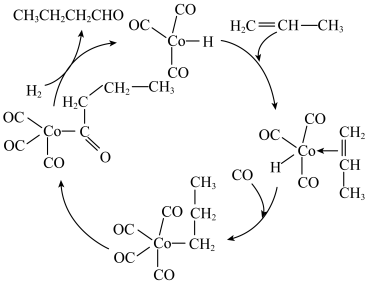
A.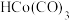 是该反应的中间产物 是该反应的中间产物 |
B.上述循环过程中, 的配位数没有发生变化 的配位数没有发生变化 |
C.若反应物为乙烯,产物为 |
D.总反应式为 |
您最近半年使用:0次
名校
解题方法
9 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是_______ 。
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:_______ ;在元素周期表中,该元素在_______ (填“s”“p”“d”“f”或“ds”)区。
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式_______ ,该阴离子中存在的化学键有_______ (填字母代号)
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
您最近半年使用:0次
昨日更新
|
65次组卷
|
2卷引用:江西省南昌市第十中学2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
10 . 含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为___________ ;
(2)已知 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为___________ ; 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有___________ 个。
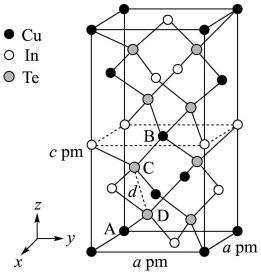
(3)一种由 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为___________ ,晶胞中 、
、 间距离
间距离
___________  。
。 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。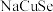 晶胞中0价
晶胞中0价 原子个数为
原子个数为___________ ,每个 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为___________ 。
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为(2)已知
 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有(3)一种由
 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为 、
、 间距离
间距离
 。
。
 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。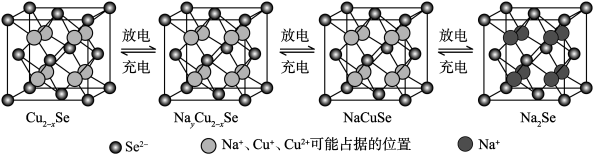
 晶胞中0价
晶胞中0价 原子个数为
原子个数为 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为
您最近半年使用:0次



