解题方法
1 . 近年来,光催化剂的研究是材料领域的热点方向。一种Ru配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法正确的是
转化为HCOOH。下列说法正确的是
 转化为HCOOH。下列说法正确的是
转化为HCOOH。下列说法正确的是
A.该Ru配合物中第二周期元素的第一电离能由大到小的顺序为 |
B.该Ru配合物中C原子、N原子的杂化方式均为 |
| C.该配合物中Ru的配体分别是有机物、一氧化碳和氯原子 |
D.HCOOH的沸点比 高,主要原因是HCOOH分子间存在范德华力和氢键,而 高,主要原因是HCOOH分子间存在范德华力和氢键,而 分子间只有范德华力 分子间只有范德华力 |
您最近半年使用:0次
2 . 一种亲电试剂的结构如图,其中W、X、Y、Z均为短周期元素且同周期,阳离子中所有原子共平面。下列说法正确的是
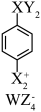
A.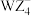 中W为 中W为 杂化 杂化 | B.第一电离能:Z>X>Y |
| C.最简单氢化物的沸点:X<Y<Z | D.1mol W的最高价含氧酸最多能与3mol NaOH反应 |
您最近半年使用:0次
名校
解题方法
3 . Ⅰ.现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)由表格可知,A组物质熔点普遍偏高,A组属于_______ 晶体,硅晶体的熔点低于金刚石,是由于_______ 。
(2)C组中HF相对分子质量小于 但熔点却高于
但熔点却高于 ,是由于
,是由于_______ 。
(3)D组晶体中 、
、 、
、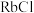 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为_______ 。
Ⅱ.下图表示一些常见晶体的微观结构: 的是
的是_______ (填字母);在干冰晶体中,每个 分子周围紧邻的
分子周围紧邻的 分子有
分子有_______ 个。
(5) 晶体在
晶体在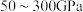 的高压下和
的高压下和 反应生成如下图所示的晶胞结构,则该晶体的化学式为
反应生成如下图所示的晶胞结构,则该晶体的化学式为_______ 。 的晶胞如下图所示,密度为
的晶胞如下图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为_______ 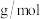 (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF: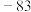 |  |
| 硅晶体:1410 | Na:98 |  : :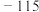 |  |
| 硼晶体:2300 | K:64 |  : :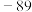 | 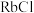 |
| 二氧化硅:1732 | Rb:39 | HI: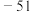 |  |
(1)由表格可知,A组物质熔点普遍偏高,A组属于
(2)C组中HF相对分子质量小于
 但熔点却高于
但熔点却高于 ,是由于
,是由于(3)D组晶体中
 、
、 、
、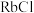 、
、 的熔点由高到低的顺序为
的熔点由高到低的顺序为Ⅱ.下图表示一些常见晶体的微观结构:
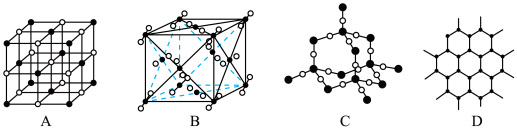
 的是
的是 分子周围紧邻的
分子周围紧邻的 分子有
分子有(5)
 晶体在
晶体在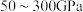 的高压下和
的高压下和 反应生成如下图所示的晶胞结构,则该晶体的化学式为
反应生成如下图所示的晶胞结构,则该晶体的化学式为
 的晶胞如下图所示,密度为
的晶胞如下图所示,密度为 ,相邻的两个
,相邻的两个 的最近核间距为anm,则
的最近核间距为anm,则 的摩尔质量为
的摩尔质量为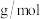 (列出代数式,设
(列出代数式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。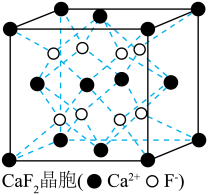
您最近半年使用:0次
名校
解题方法
4 . 有机物是一类重要的化合物,不仅种类繁多,而且与我们的日常生活密切相关。
Ⅰ.下列有机物:_______ 、⑦_______ 。
(2)⑧被酸性高锰酸钾氧化的产物为_______ 。
(3)所有原子一定共面的是_______ (填序号,下同)。
(4)⑨的二氯代物有_______ 种同分异构体。
(5)水溶性最好的是_______ ,原因_______ 。
Ⅱ.烷烃主要来源是石油和天然气,是重要的化工原料和能源物资。
(6)表中烷烃的氢原子的化学环境只有一种,分析下表中各项的排布规律,按此规律排布第6项X应为_______ (选填编号)。
a.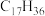 b.
b.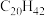 c.
c.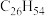 d.
d.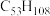
Ⅰ.下列有机物:
① ;②
;②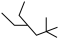 ;③
;③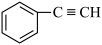 ;④
;④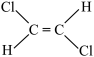 ;⑤
;⑤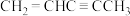 ;
;
⑥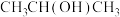 ;⑦
;⑦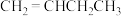 ;⑧
;⑧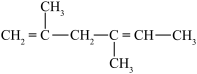 ;⑨
;⑨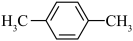 ;
;
(2)⑧被酸性高锰酸钾氧化的产物为
(3)所有原子一定共面的是
(4)⑨的二氯代物有
(5)水溶性最好的是
Ⅱ.烷烃主要来源是石油和天然气,是重要的化工原料和能源物资。
(6)表中烷烃的氢原子的化学环境只有一种,分析下表中各项的排布规律,按此规律排布第6项X应为
| 1 | 2 | 3 | 4 | 5 | 6 | … |
 |  | 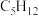 | 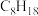 | X |
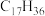 b.
b.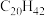 c.
c.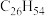 d.
d.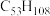
您最近半年使用:0次
2024·北京·模拟预测
名校
解题方法
5 . 下列叙述中,事实与对应解释不正确 的是
| 事实 | 解释 | |
| A | 酸性:HCOOH > CH3COOH | H3C–是推电子基团,使羧基中羟基的极性减小 |
| B | 在CS2中的溶解度:H2O < CCl4 | H2O为极性分子,CS2和CCl4是非极性分子 |
| C | 硬度:金刚石>石墨 | 金刚石属于共价晶体只含共价键,石墨属于混合型晶体,既存在共价键又存在范德华力 |
| D | 热稳定性:H2O > H2S | 水分子间存在氢键作用 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 物质的结构决定其性质。下列实例与解释不相符的是
选项 | 实例 | 解释 |
A | NH3比PH3易液化 | NH3分子间能形成氢键 |
B | 三氟乙酸的酸性大于三氯乙酸 | 三氯乙酸分子间作用力较大 |
C | Al的硬度大于Mg | Al原子价电子数多,半径小 |
D | Br2在CCl4中的溶解度大于在H2O中的 | Br2、CCl4为非极性分子,H2O为极性分 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . X、Y、Z、M为原子序数依次增大的四种短周期主族元素,X和Z基态原子L层上均有2个未成对电子,Z与M同主族;Q位于元素周期表中第四周期,基态原子有1个电子未成对且内层电子全满。 能与
能与 形成
形成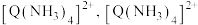 中2个
中2个 被2个
被2个 取代可得两种不同的结构。
取代可得两种不同的结构。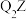 晶胞如下图所示。下列说法
晶胞如下图所示。下列说法不 正确的是
 能与
能与 形成
形成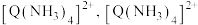 中2个
中2个 被2个
被2个 取代可得两种不同的结构。
取代可得两种不同的结构。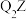 晶胞如下图所示。下列说法
晶胞如下图所示。下列说法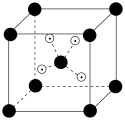
A.简单氢化物的沸点: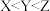 | B. 的空间构型为正四面体形 的空间构型为正四面体形 |
C.原子半径: | D.每个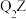 晶胞中含4个 晶胞中含4个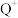 |
您最近半年使用:0次
解题方法
8 . 下列物质性质排序错误的是
A.酸性: | B.沸点: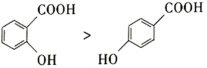 |
C.熔点: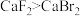 | D.稳定性: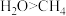 |
您最近半年使用:0次
9 . 二氯草酸硼酸锂[LiBF2(C2O4)]是新型锂离子电池电解质,乙酸锰可用于制造离子电池的负极材料,他们的合成方法如下:
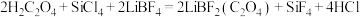

(1)基态 核外电子排布式为
核外电子排布式为___________ ,C、N、O第一电离能由小到大的顺序是___________ 。
(2)草酸(HOOCCOOH)分子中碳原子的杂化轨道类型是___________ , 草酸分子中含有σ键与
草酸分子中含有σ键与 键的数目之比为
键的数目之比为___________ 。
(3)与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为___________ 。
(4) 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为___________ 。
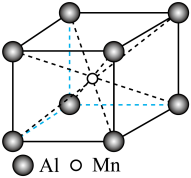
(5)镧锰合金的晶胞如图所示,锰原子除了1个在体心外,其余都在面心上。该合金中锰原子和镧原子的个数比为___________ 。 代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为
代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为___________  。
。
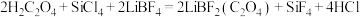

(1)基态
 核外电子排布式为
核外电子排布式为(2)草酸(HOOCCOOH)分子中碳原子的杂化轨道类型是
 草酸分子中含有σ键与
草酸分子中含有σ键与 键的数目之比为
键的数目之比为(3)与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)
 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为(5)镧锰合金的晶胞如图所示,锰原子除了1个在体心外,其余都在面心上。该合金中锰原子和镧原子的个数比为
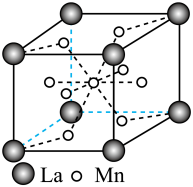
 代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为
代表阿伏加德罗常数的数值,则铝、锰的最短核间距(d)为 。
。
您最近半年使用:0次
10 . N2H4的沸点(113.5℃)比NH3的沸点(-33.4℃)高,原因是_____________ 。
您最近半年使用:0次



