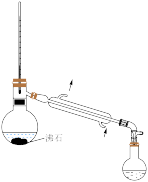
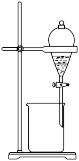
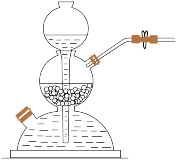
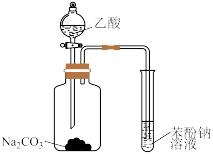
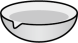
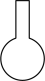
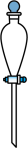
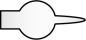
1 . 下列装置(部分加热、夹持等仪器未画出)可以用于相应实验的是
|
|
| A.分离二氯甲烷和四氯甲烷 | B.提纯含有少量氯化钠和泥沙的苯甲酸 |
|
|
| C.用电石与水反应制取乙炔 | D.比较乙酸、碳酸和苯酚的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 化学创造美好生活。下列生产活动与对应化学原理解释不正确的是
| 选项 | 生产活动 | 化学原理 |
| A | 用氢氧化铝治疗胃酸过多 | 氢氧化铝有弱碱性 |
| B | 用ClO2作饮用水杀菌消毒剂 | ClO2具有强氧化性 |
| C | 凡酸坏之酒,皆可蒸烧 | 物质的溶解性不同 |
| D | 用Fe3O4作录音磁带 | Fe3O4具有磁性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . 溴乙烷是一种重要的有机合成中间体,沸点为38.4℃,密度为1.44g/cm3。实验室制备少量溴乙烷主要步骤如下:
步骤Ⅱ:向仪器A中依次加入搅拌磁子、9.2 g乙醇及18 mL水,冰水冷却下缓慢加入28 mL 18 mol/L H2SO4,冷却至室温,搅拌下加入24g NaBr。缓慢加热至无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得溴乙烷13.5 g。
已知:
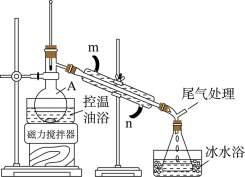
(1)仪器A的名称是________ ,冷凝管中冷却水进水口为________ (填“m”或“n”)。
(2)反应生成的主要副产物有乙烯,写出生成乙烯的化学反应方程式________ 。
(3)步骤2中需向锥形瓶内加入少量冰水并置于冰水浴中的目的是________ 。
(4)溴乙烷在水中的溶解性_______ (填“大于”、“小于”或“等于”)乙醇在水中的溶解性,其原因是________ 。
(5)为进一步制得纯净的溴乙烷,将粗品溴乙烷________ 。(写出实验步骤,实验中须使用的试剂:蒸馏水、无水CaCl2固体)
(6)计算本实验中溴乙烷的产率________ 。(保留三位有效数字)
步骤Ⅱ:向仪器A中依次加入搅拌磁子、9.2 g乙醇及18 mL水,冰水冷却下缓慢加入28 mL 18 mol/L H2SO4,冷却至室温,搅拌下加入24g NaBr。缓慢加热至无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得溴乙烷13.5 g。
已知:
(1)仪器A的名称是
(2)反应生成的主要副产物有乙烯,写出生成乙烯的化学反应方程式
(3)步骤2中需向锥形瓶内加入少量冰水并置于冰水浴中的目的是
(4)溴乙烷在水中的溶解性
(5)为进一步制得纯净的溴乙烷,将粗品溴乙烷
(6)计算本实验中溴乙烷的产率
您最近半年使用:0次
解题方法
4 . 下列有关仪器的名称、示意图与用途或使用操作的叙述均正确的是
| 选项 | A | B | C | D |
| 名称 | 坩埚 | 蒸馏烧瓶 | 分液漏斗 | 球形干燥管 |
| 示意图 |
|
|
|
|
| 用途或使用操作 | 可用于对固体进行高温加热 | 可用于制备蒸馏水 | 分液时将磨口瓶塞上的凹槽对准漏斗口颈上的小孔 | 洗气除杂实验中将气体从小口通入 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
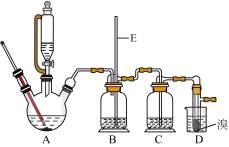
5 . 实验室用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置(加热、夹持装置已略去)如图所示:
回答下列问题:
(1)装置D中发生的主要反应的化学方程式为__________ 。
(2)装置B中长玻璃管E的作用是__________ 。
(3)在装置C中应加入氢氧化钠溶液 ,其目的是吸收反应可能生成_____________ 的气体。
(4)反应过程中应用冷水冷却装置D,其主要目的是______________ ;但又不能过度冷却(如用冰水),其原因是__________ ;将1,2-二溴乙烷粗产品置于分液漏斗中,加水,振荡后静置,产物应在_______ 层(填“上”或“下”)。
(5)若产物中有少量副产物乙醚,最好用_________ 方法除去。
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 常温下状态 | 无色液体 | 无色液体 | 无色液体 |
密度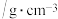 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)装置D中发生的主要反应的化学方程式为
(2)装置B中长玻璃管E的作用是
(3)在装置C中应加入氢氧化钠溶液 ,其目的是吸收反应可能生成
(4)反应过程中应用冷水冷却装置D,其主要目的是
(5)若产物中有少量副产物乙醚,最好用
您最近半年使用:0次
6 . 古代文献记载很多与化学相关的内容。下列解释错误的是
| A.《肘后备急方》载:“青蒿一握,以水二升渍,绞取汁”,“绞取汁”涉及到过滤分离方法 |
| B.“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”,“气”指乙烯 |
| C.《本草纲目》“烧酒”写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也”,这种方法是蒸馏 |
| D.《本草衍义》中对精制砒霜过程描述如下:“将生砒就置火上,以器覆之,令砒烟上飞,着覆器”中的操作方法是萃取 |
您最近半年使用:0次
7 . 浩瀚的海洋中蕴藏着丰富的资源,其中海水提溴工艺流程如下所示:不正确 的是
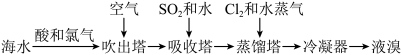
| A.吹出塔中利用了溴单质的挥发性将溴分离出来 |
| B.吸收塔中Br2与SO2发生反应以达到富集目的 |
| C.蒸馏塔中利用物质沸点不同进行分离 |
| D.吸收时可用Fe2(SO4)3溶液代替SO2和水 |
您最近半年使用:0次
名校
解题方法
8 . 两种有机化合物A和B可以互溶,有关性质如表:
(1)若要除去A和B的混合物中少量的B,采用___________(填序号)方法即可得到A。
(2)将有机化合物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),已知有机化合物A的核磁共振氢谱、质谱如图所示,则A的结构简式为___________ 。________ ___________ ;官能团的名称为___________ 。
②写出该有机物的同分异构体中能与Na反应产生H2的所有可能的同分异构体的结构简式:___________ 。
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3℃ | 78.5℃ | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |
(1)若要除去A和B的混合物中少量的B,采用___________(填序号)方法即可得到A。
| A.重结晶 | B.蒸馏 | C.萃取 | D.加水充分振荡,分液 |
(2)将有机化合物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),已知有机化合物A的核磁共振氢谱、质谱如图所示,则A的结构简式为
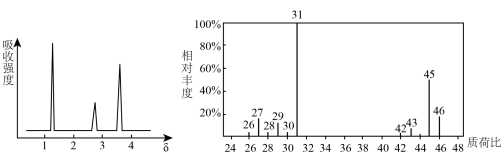

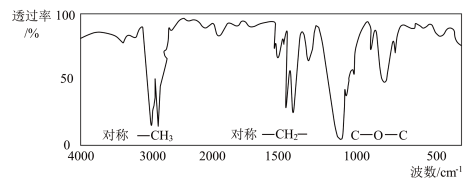
②写出该有机物的同分异构体中能与Na反应产生H2的所有可能的同分异构体的结构简式:
您最近半年使用:0次
名校
解题方法
9 . 下列每个选项中各有2组物质,它们都能用分液漏斗分离的是
| A.植物油和水、酒精和水 | B.溴乙烷和水、硝基苯和苯 |
| C.甘油和水、乙醛和水 | D.苯和水、己烷和水 |
您最近半年使用:0次
名校
解题方法
10 . 某化学兴趣小组设计实验利用苯甲酸(沸点249℃)和异丙醇(沸点82℃)制备苯甲酸异丙酯(沸点218℃),实验装置如图:
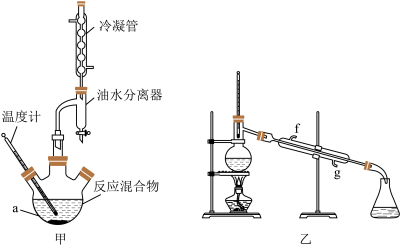
| A.在仪器a中加入三种试剂的先后顺序是:浓硫酸、异丙醇、苯甲酸 |
| B.实验采用水浴加热,若温度过高会使产率减小 |
| C.加入的苯甲酸和异丙醇中,需过量的是苯甲酸 |
| D.步骤③操作时应收集218℃的馏分,如果温度计水银球偏下,则收集的精制产品中可能混有的杂质为苯甲酸 |
您最近半年使用:0次