1 . 下列图示装置能达到实验目的的是
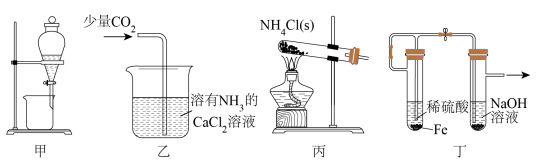
A.装置甲用甘油分离溴水中的 | B.装置乙制取少量 |
C.装置丙实验室制备少量 | D.装置丁制备少量 |
您最近半年使用:0次
2 . 下列有关物质应用的说法错误的是
A. 可用作食品添加剂 可用作食品添加剂 |
B. 可用于鉴别溴水和碘水 可用于鉴别溴水和碘水 |
C.室温时,可用 溶液来清洗试管壁的硫黄 溶液来清洗试管壁的硫黄 |
D. 可除去污水中的 可除去污水中的 |
您最近半年使用:0次
3 . 利用废旧锂电池可回收金属元素。已知废旧锂离子电池的主要成分为 以及
以及 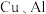 等单质,回收工艺流程如图:
等单质,回收工艺流程如图:
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
(2)“生化反应”后溶液中存在的主要阳离子有 、
、_______ 。“生化反应”最初使用的是 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为_______ ,使用细菌的优点是_______ 。
(3) 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因:_______ 。_______ 。
(5) (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 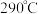 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 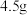 ,所得固体成分为
,所得固体成分为_______ (填化学式)。
(6)金属铜的晶胞如图所示,此晶胞的边长为 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ=_______ g∙cm-3 (用含  的代数式表示)。
的代数式表示)。
 以及
以及 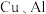 等单质,回收工艺流程如图:
等单质,回收工艺流程如图: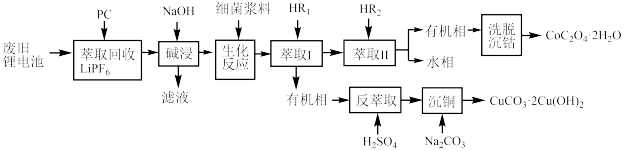
(1)“反萃取”中主要用到的玻璃仪器是_______(填字母)。
| A.漏斗 | B.胶头滴管 | C.分液漏斗 | D.蒸馏烧瓶 |
(2)“生化反应”后溶液中存在的主要阳离子有
 、
、 和
和  ,该过程中反应的
,该过程中反应的  与还原剂的物质的量之比为
与还原剂的物质的量之比为(3)
 萃取率随温度变化如图所示,请解释变化的原因:
萃取率随温度变化如图所示,请解释变化的原因: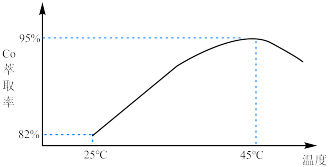
(5)
 (相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到
(相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,加热到 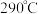 过程中,若生成两种气体,剩余固体的质量为
过程中,若生成两种气体,剩余固体的质量为 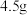 ,所得固体成分为
,所得固体成分为(6)金属铜的晶胞如图所示,此晶胞的边长为
 ,设
,设  为阿伏加德罗常数的值,则铜晶胞的密度ρ=
为阿伏加德罗常数的值,则铜晶胞的密度ρ= 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
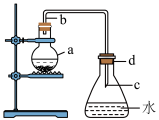
4 . 中学实验室用下图所示装置制取少量溴苯,请填写下列空白:___________ 的作用。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的___________ 遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有___________ 生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有棕色不溶于水的液体,这是溶解了___________ 的粗产品溴苯。
(5)写出烧瓶a中发生反应的化学方程式:___________ 。
(6)提纯粗溴苯的方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,发生的化学反应方程式是___________ ,待静置分层后,用___________ 分离出下层液体,即为溴苯。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有棕色不溶于水的液体,这是溶解了
(5)写出烧瓶a中发生反应的化学方程式:
(6)提纯粗溴苯的方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,发生的化学反应方程式是
您最近半年使用:0次
名校
解题方法
5 . 下列各项操作错误的有
| A.用乙醇萃取溴水中的溴单质的操作可选用分液漏斗 |
| B.进行分液时,分液漏斗中的下层液体从下口放出,上层液体则从上口倒出 |
| C.萃取、分液前需对分液漏斗检漏 |
| D.为保证分液漏斗内的液体顺利流出,需将上口的塞子拿下 |
您最近半年使用:0次
名校
解题方法
6 . 海水提碘实验中,得到碘的四氯化碳溶液后可用“反萃取法”萃取、富集碘单质,实验步骤如下(已知:3I2+6NaOH=5NaI+NaIO3+3H2O)。下列说法错误的是
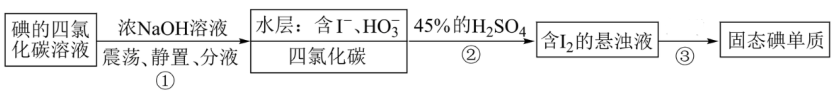
| A.步骤①还可以用酒精做萃取剂 |
| B.分液时水层从分液漏斗上口放出 |
C.步骤②中发生反应的离子方程式为6H++5I-+ =3I2↓+3H2O =3I2↓+3H2O |
| D.步骤③操作中需要的玻璃仪器为漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
7日内更新
|
78次组卷
|
2卷引用:福建省福安市第一中学2023-2024学年高一下学期3月月考化学试题
7 . 实验室以一种工业废渣(主要成分为 、
、 和少量Fe、Al的氧化物)为原料制备重要化工原料
和少量Fe、Al的氧化物)为原料制备重要化工原料 的工艺流程如下。下列说法错误的是
的工艺流程如下。下列说法错误的是
 、
、 和少量Fe、Al的氧化物)为原料制备重要化工原料
和少量Fe、Al的氧化物)为原料制备重要化工原料 的工艺流程如下。下列说法错误的是
的工艺流程如下。下列说法错误的是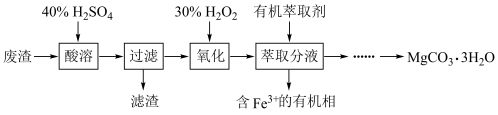
| A.滤渣中除不溶性杂质外还有硅酸 |
B.氧化过程中主要发生反应的离子方程式为: |
| C.萃取分液后分液漏斗的液体全部由下口放出到两个不同烧杯中以便分离漏 |
| D.萃取后得到的水溶液可以边搅拌边加入MgO以调节pH |
您最近半年使用:0次
名校
解题方法
8 . 下列实验装置或操作能达到实验目的的是
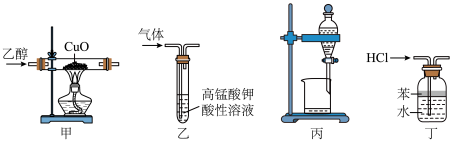
| A.装置甲:检验乙醇具有还原性 | B.装置乙:除去甲烷中的乙烯 |
C.装置丙:提取 的 的 溶液中的 溶液中的 | D.装置丁:吸收 气体,并防止液体倒吸 气体,并防止液体倒吸 |
您最近半年使用:0次
解题方法
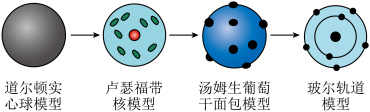
9 . 下列说法不正确的是
| A.侯德榜是我国著名化工专家,发明了侯氏制碱法 |
| B.舍勒发现了一种黄绿色气体,戴维确认该气体为氯气 |
| C.屠呦呦——从青蒿中提取青蒿素 |
| D.原子结构模型演变历史可以表示为如图 |
您最近半年使用:0次
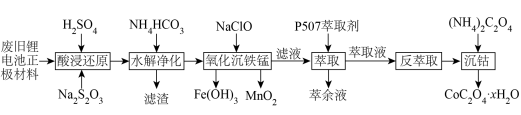
10 . 近年来,废旧锂离子电池的回收成为目前新能源产业重要的发展方向。某锂离子二次电池的正极材料主要为LiCoO2,还含有少量Al、Fe、Mn、Ni的化合物。通过如图所示的流程利用废旧锂离子电池制备草酸钴晶体(CoC2O4·xH2O),回答下列问题:
(1)LiCoO2中Co的化合价为___________ ,“酸浸还原”中LiCoO2转化为(Co2+,氧化产物是SO2,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“水解净化”的滤渣主要成分为___________ (填化学式)。
(3)“氧化沉铁锰”的操作为控制体系的pH在4~5,加入NaClO溶液。其中Mn2+转化为MnO2的离子方程式为___________ ;实际生产中,随着反应时间的延长,锰和铁的沉淀率逐渐增大,但钴的损失量也随之增大,可能的原因是___________ 。
(4)利用“P507萃取剂”从“滤液”中分离Co2+萃取时,Co、Ni的萃取率和Co/Ni分离因素与水相pH的关系如图所示。
(5)“沉钴”时反应的化学方程式为___________ 。
| 离子 | Co2+ | Fe3+ | Fe2+ | Al3+ | Mn2+ | Ni2+ |
| pH | 9.3 | 3.2 | 9.0 | 4.7 | 10.1 | 8.9 |
(1)LiCoO2中Co的化合价为
(2)“水解净化”的滤渣主要成分为
(3)“氧化沉铁锰”的操作为控制体系的pH在4~5,加入NaClO溶液。其中Mn2+转化为MnO2的离子方程式为
(4)利用“P507萃取剂”从“滤液”中分离Co2+萃取时,Co、Ni的萃取率和Co/Ni分离因素与水相pH的关系如图所示。
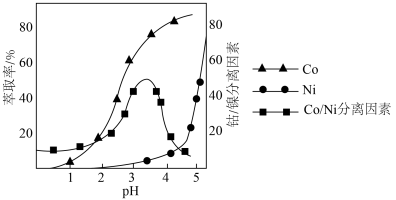
| A.2.5 | B.3.0 | C.3.5 | D.4.0 |
(5)“沉钴”时反应的化学方程式为
您最近半年使用:0次



