解题方法
1 .  气体在1834年首次被发现并确定为一种浅橙黄色气体,常用作木浆的有效漂白剂等。实验室用如图1所示装置(加热装置和夹持仪器已省略)制备少量
气体在1834年首次被发现并确定为一种浅橙黄色气体,常用作木浆的有效漂白剂等。实验室用如图1所示装置(加热装置和夹持仪器已省略)制备少量 。
。
已知:①常压下, 沸点
沸点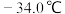 ,熔点
,熔点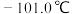 ;
; 沸点
沸点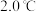 ,熔点
,熔点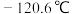 。
。
② 热稳定性差,常温下即可分解,与氧气等混合时易发生爆炸。
热稳定性差,常温下即可分解,与氧气等混合时易发生爆炸。
③ 在
在 中的溶解度远大于在水中的溶解度。
中的溶解度远大于在水中的溶解度。 的目的是
的目的是_______ 。
(2)用装置C吸收 制备
制备 ,C中磷酸钠对应的产物为磷酸氢钠,写出该反应的离子方程式
,C中磷酸钠对应的产物为磷酸氢钠,写出该反应的离子方程式_______ 。
(3)装置E的作用是_______ 。
(4) 常用于制取高纯度
常用于制取高纯度 溶液。将
溶液。将 与
与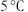 的蒸馏水充分混合反应后,从水溶液中分离出
的蒸馏水充分混合反应后,从水溶液中分离出 的实验操作为
的实验操作为_______ 。
(5)近日,北京师范大学研究团队提出了一种新的 形成机理。其反应机理如题图2所示,写出反应①的离子方程式:
形成机理。其反应机理如题图2所示,写出反应①的离子方程式:_______ 。 可被
可被 等物质还原。取某
等物质还原。取某 的稀释液
的稀释液 于锥形瓶中,并加入
于锥形瓶中,并加入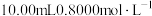 的
的 溶液,充分反应后,用
溶液,充分反应后,用 的酸性
的酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 ,则原
,则原 的稀释液的物质的量浓度为
的稀释液的物质的量浓度为_______ (不考虑 参与反应,写出计算过程。)
参与反应,写出计算过程。)
 气体在1834年首次被发现并确定为一种浅橙黄色气体,常用作木浆的有效漂白剂等。实验室用如图1所示装置(加热装置和夹持仪器已省略)制备少量
气体在1834年首次被发现并确定为一种浅橙黄色气体,常用作木浆的有效漂白剂等。实验室用如图1所示装置(加热装置和夹持仪器已省略)制备少量 。
。已知:①常压下,
 沸点
沸点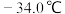 ,熔点
,熔点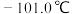 ;
; 沸点
沸点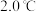 ,熔点
,熔点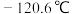 。
。②
 热稳定性差,常温下即可分解,与氧气等混合时易发生爆炸。
热稳定性差,常温下即可分解,与氧气等混合时易发生爆炸。③
 在
在 中的溶解度远大于在水中的溶解度。
中的溶解度远大于在水中的溶解度。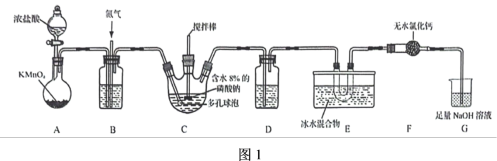
 的目的是
的目的是(2)用装置C吸收
 制备
制备 ,C中磷酸钠对应的产物为磷酸氢钠,写出该反应的离子方程式
,C中磷酸钠对应的产物为磷酸氢钠,写出该反应的离子方程式(3)装置E的作用是
(4)
 常用于制取高纯度
常用于制取高纯度 溶液。将
溶液。将 与
与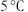 的蒸馏水充分混合反应后,从水溶液中分离出
的蒸馏水充分混合反应后,从水溶液中分离出 的实验操作为
的实验操作为(5)近日,北京师范大学研究团队提出了一种新的
 形成机理。其反应机理如题图2所示,写出反应①的离子方程式:
形成机理。其反应机理如题图2所示,写出反应①的离子方程式: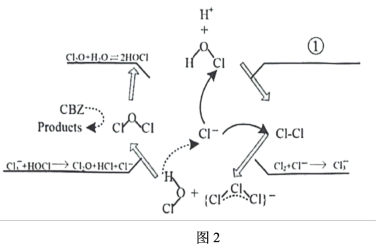
 可被
可被 等物质还原。取某
等物质还原。取某 的稀释液
的稀释液 于锥形瓶中,并加入
于锥形瓶中,并加入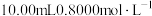 的
的 溶液,充分反应后,用
溶液,充分反应后,用 的酸性
的酸性 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 ,则原
,则原 的稀释液的物质的量浓度为
的稀释液的物质的量浓度为 参与反应,写出计算过程。)
参与反应,写出计算过程。)
您最近半年使用:0次
解题方法
2 . “消洗灵”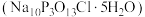 是一种高效低毒的消毒洗涤剂,其消毒原理与“84消毒液”相似,实验室中制备“消洗灵”的装置如图所示(夹持装置略)。
是一种高效低毒的消毒洗涤剂,其消毒原理与“84消毒液”相似,实验室中制备“消洗灵”的装置如图所示(夹持装置略)。
(1)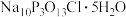 中氯元素的化合价为
中氯元素的化合价为___________ ;使用仪器___________ (填“a”或“b”)时需取下玻璃塞或玻璃塞凹槽与磨口小孔相对。
(2)装置A中发生反应的氧化剂与氧化产物的物质的量之比为___________ 。
(3)装置B中盛装的试剂为___________ ;装置D的作用为___________ 。
(4)实验操作步骤如下:
①打开仪器a的活塞及活塞K,制备NaClO碱性溶液;
②关闭仪器a的活塞及活塞K,打开仪器b的活塞;
③一段时间后,装置C中溶液经一系列操作得到粗产品。
装置C中Na3PO4与Na2HPO4的物质的量之比为1:2,则步骤②中生成 的化学方程式为
的化学方程式为___________ 。
(5)利用滴定法测定产品的纯度(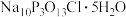 的摩尔质量为
的摩尔质量为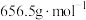 ),
),
实验方案如下:
①取2.000g产品试样溶于蒸馏水中配成100mL溶液;
②量取25.00mL待测液于锥形瓶中,加入10mL H2SO4溶液、25mL
H2SO4溶液、25mL KI溶液(过量),暗处静置5min;
KI溶液(过量),暗处静置5min;
③滴加3滴淀粉溶液,用 Na2S2O3标准溶液滴定,发生反应:
Na2S2O3标准溶液滴定,发生反应: 。平行滴定三次,平均消耗20.00mL标准溶液。判断达到滴定终点的现象为
。平行滴定三次,平均消耗20.00mL标准溶液。判断达到滴定终点的现象为___________ ;产品的纯度为___________ %(保留三位有效数字);步骤②中若静置时间过长,产品纯度的测定值将___________ (填“偏大”“偏小”或“不变”)。
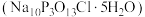 是一种高效低毒的消毒洗涤剂,其消毒原理与“84消毒液”相似,实验室中制备“消洗灵”的装置如图所示(夹持装置略)。
是一种高效低毒的消毒洗涤剂,其消毒原理与“84消毒液”相似,实验室中制备“消洗灵”的装置如图所示(夹持装置略)。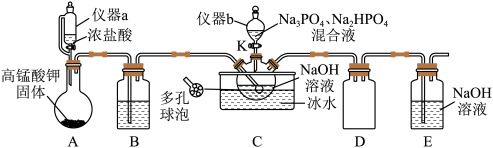
(1)
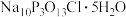 中氯元素的化合价为
中氯元素的化合价为(2)装置A中发生反应的氧化剂与氧化产物的物质的量之比为
(3)装置B中盛装的试剂为
(4)实验操作步骤如下:
①打开仪器a的活塞及活塞K,制备NaClO碱性溶液;
②关闭仪器a的活塞及活塞K,打开仪器b的活塞;
③一段时间后,装置C中溶液经一系列操作得到粗产品。
装置C中Na3PO4与Na2HPO4的物质的量之比为1:2,则步骤②中生成
 的化学方程式为
的化学方程式为(5)利用滴定法测定产品的纯度(
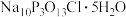 的摩尔质量为
的摩尔质量为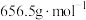 ),
),实验方案如下:
①取2.000g产品试样溶于蒸馏水中配成100mL溶液;
②量取25.00mL待测液于锥形瓶中,加入10mL
 H2SO4溶液、25mL
H2SO4溶液、25mL KI溶液(过量),暗处静置5min;
KI溶液(过量),暗处静置5min;③滴加3滴淀粉溶液,用
 Na2S2O3标准溶液滴定,发生反应:
Na2S2O3标准溶液滴定,发生反应: 。平行滴定三次,平均消耗20.00mL标准溶液。判断达到滴定终点的现象为
。平行滴定三次,平均消耗20.00mL标准溶液。判断达到滴定终点的现象为
您最近半年使用:0次
名校
解题方法
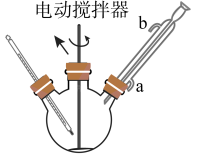
3 . 纯净苯甲酸是无色针状晶体,100℃开始升华,常用作食品防腐剂。实验室用甲苯和高锰酸钾制备苯甲酸(放热反应),反应方程式如下:
苯甲酸、氯化钾在100g水中的溶解度如表所示:
实验室用甲苯和高锰酸钾制备苯甲酸的步骤如下:
第二步(分离获得苯甲酸粗产品):①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤得到粗产品。
第三步(粗产品苯甲酸的提纯):①沸水溶解→②活性炭脱色→③趁热过滤→④→⑤过滤→⑥洗涤→⑦干燥
请回答下列有关问题:
(1)实验中准确量取5.29mL甲苯所需仪器为___________;
(2)可以作为判断反应已完成的现象是___________;
(3)第三步粗产品苯甲酸的提纯中“③趁热过滤”的目的是___________ ;“④”的操作名称是___________ ;“⑥洗涤”采用的试剂可以是___________ (填乙醇或水),判断洗涤干净的方法是___________ ;
(4)第二步粗产品苯甲酸中含有的杂质主要是氯化钾。将氯化钾与苯甲酸分离,可用下列哪种操作___________;
(5)干燥后称量得苯甲酸4.27g,则苯甲酸的产率为___________ 。
 +2KMnO4
+2KMnO4
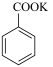 (苯甲酸钾)
(苯甲酸钾) ;
;
 +HCl→
+HCl→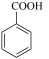 (苯甲酸)
(苯甲酸)
| 化合物 | 相对分子质量 | 密度( ) ) | 沸点(℃) | 水中溶解性 | 乙醇中溶解性 |
| 甲苯 | 92 | 0.87 | 110.0 | 不溶于水 | 互溶 |
| 苯甲酸钾 | 160 | — | — | 易溶于水 | |
| 苯甲酸 | 122 | 1.26 | 248.0 | 微溶于水 | 易溶 |
| 温度/℃ | 4℃ | 18℃ | 25℃ | 50℃ | 75℃ |
| 苯甲酸溶解度/g | 0.18g | 0.27g | 0.34 | 0.85 | 2.2g |
| 氯化钾溶解度/g | 31 | 34.2 | 38 | 42 | 48 |
第二步(分离获得苯甲酸粗产品):①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤得到粗产品。
第三步(粗产品苯甲酸的提纯):①沸水溶解→②活性炭脱色→③趁热过滤→④→⑤过滤→⑥洗涤→⑦干燥
请回答下列有关问题:
(1)实验中准确量取5.29mL甲苯所需仪器为___________;
| A.量筒 | B.酸式滴定管 | C.烧杯 | D.碱式滴定管 |
(2)可以作为判断反应已完成的现象是___________;
| A.冷凝管回流液中不再出现油状液滴 |
| B.反应液的紫红色变浅或消失 |
| C.反应液没有出现明显的分层现象 |
| D.反应液中的浑浊程度不再变化 |
(3)第三步粗产品苯甲酸的提纯中“③趁热过滤”的目的是
(4)第二步粗产品苯甲酸中含有的杂质主要是氯化钾。将氯化钾与苯甲酸分离,可用下列哪种操作___________;
| A.萃取分液 | B.重结晶 | C.蒸馏 | D.升华 |
(5)干燥后称量得苯甲酸4.27g,则苯甲酸的产率为
您最近半年使用:0次
4 . 锌、铋(Bi)、锗(Ge)的单质及其化合物用途较广。利用某冶锌工业废料(主要含ZnO,还含有氧化铋、氧化锗)回收其金属化合物的流程如下(已知:Ge4+易水解,单宁酸为一种弱酸)。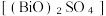 中铋的化合价为
中铋的化合价为_______ ,基态锌原子的价层电子排布式为_______ 。
(2)锌的第二电离能小于铜的第二电离能,原因是_______ 。
(3)提高“酸浸1”浸取率的措施有_______ (写出两条即可)。
(4)“酸浸2”时,Bi2O3发生反应的离子方程式为_______ 。
(5)“沉锗”操作中需调节pH值约为2.5,不能过低,也不能过高,原因是_______ 。
(6)由“浸液1”得到ZnSO4∙7H2O的操作是_______ 、_______ 、过滤、洗涤、干燥。
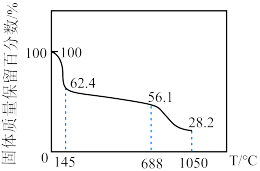
(7)加热ZnSO4∙7H2O,固体质量保留百分数与温度的关系如下图所示。688℃时所得固体的化学式为_______ 。
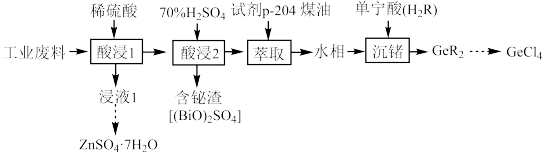
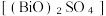 中铋的化合价为
中铋的化合价为(2)锌的第二电离能小于铜的第二电离能,原因是
(3)提高“酸浸1”浸取率的措施有
(4)“酸浸2”时,Bi2O3发生反应的离子方程式为
(5)“沉锗”操作中需调节pH值约为2.5,不能过低,也不能过高,原因是
(6)由“浸液1”得到ZnSO4∙7H2O的操作是
(7)加热ZnSO4∙7H2O,固体质量保留百分数与温度的关系如下图所示。688℃时所得固体的化学式为
您最近半年使用:0次
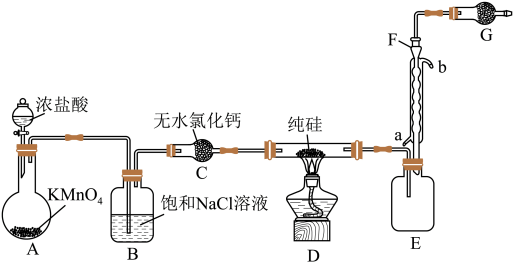
5 . 2023年9月华为推出了举世瞩目的“中国芯”——麒麟芯。“中国芯”的发展离不开单晶硅,四氯化硅是制备高纯硅的原料。某小组拟在实验室用下列装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
,
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为―70.0℃、57.7℃。
的熔点、沸点分别为―70.0℃、57.7℃。
③电负性Cl>H>Si, 的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
请回答下列问题:
(1)写出A中发生反应的离子方程式:______ 。
(2)装置B的作用是______ 。
(3)仪器F的名称是______ ,冷却水应从______ (填“a”或“b”)口通入。
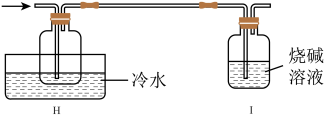
(4)有同学设计如图装置H、I替代上述E、G装置;______ 。
(5)测定产品纯度。取mg 产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用
产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用 标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为
标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为______ %(用含m、c和V的代数式表示)。若产品中溶有少量 ,则测定结果
,则测定结果______ (填“偏高”、“偏低”或“无影响”)
(6) 也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为______ 。
①
 ,
,
②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为―70.0℃、57.7℃。
的熔点、沸点分别为―70.0℃、57.7℃。③电负性Cl>H>Si,
 的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。
的沸点为31.8℃,熔点为―126.5℃,在空气中易自燃,遇水会剧烈反应。请回答下列问题:
(1)写出A中发生反应的离子方程式:
(2)装置B的作用是
(3)仪器F的名称是
(4)有同学设计如图装置H、I替代上述E、G装置;
(5)测定产品纯度。取mg
 产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用
产品溶于足量蒸馏水中(生成的HCl全部被水吸收),将混合物转入锥形瓶中,滴加甲基橙溶液,用 标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为
标准NaOH溶液滴定至终点(终点时硅酸未参加反应),消耗滴定液VmL。则产品的纯度为 ,则测定结果
,则测定结果(6)
 也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
也是制备高纯硅的重要原料,将其通入浓NaOH溶液中,发生反应的化学方程式为
您最近半年使用:0次
解题方法
6 . 某研究性学习小组进行某补血剂中铁元素( 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下:不 正确的是
 价)含量测定的实验,其流程如下:
价)含量测定的实验,其流程如下: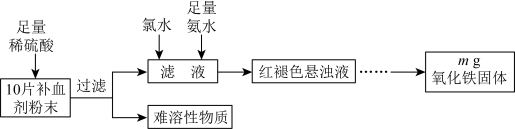
A.向过滤后的滤液中滴加 溶液,溶液可能呈红色 溶液,溶液可能呈红色 |
B.可以用 替代上述流程中的氯水 替代上述流程中的氯水 |
| C.红褐色悬浊液经过滤、洗涤、干燥,得到氧化铁固体 |
D.每片补血剂中铁元素的质量为 |
您最近半年使用:0次
名校
解题方法
7 . 某小组设计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略)。
已知:①测定原理为甲醛把 还原成
还原成 ,产生的
,产生的 与
与 定量反应生成
定量反应生成 ,
, 与菲洛嗪形成有色配合物,通过测定吸光度计算出甲醛的含量;
与菲洛嗪形成有色配合物,通过测定吸光度计算出甲醛的含量;
②吸光度用A表示,计算公式为 ,其中a为吸光度系数,b为光在样本中经过的距离,c为溶液浓度。
,其中a为吸光度系数,b为光在样本中经过的距离,c为溶液浓度。
(1)仪器A的名称是__________ 。
(2)制备银氨溶液,仪器B中放置的药品是__________ (填“ 溶液”或“氨水”)。
溶液”或“氨水”)。
(3)选择正确的操作,完成室内空气中甲醛含量的测定:__________
操作①:取下玻璃塞→操作②:__________→操作③:__________→操作④:使可滑动隔板处于最右端→操作⑤:__________→操作⑥:__________→操作⑦:__________→再将操作③~⑦重复 4 次 →测定溶液吸光度。
a.打开 ,关闭
,关闭 b.打开
b.打开 ,关闭
,关闭
c.将可滑动隔板拉至最左端 d.热水浴加热仪器A
e.将可滑动隔板缓慢推至最右端 f.将可滑动隔板迅速推至最右端
(4)写出甲醛与银氨溶液反应的化学方程式__________ 。
(5)将仪器A中溶液的 调至1,加入足量
调至1,加入足量 溶液,充分反应后加入菲洛嗪,通过测定吸光度确定生成
溶液,充分反应后加入菲洛嗪,通过测定吸光度确定生成 1.12mg,则空气中甲醛的含量为
1.12mg,则空气中甲醛的含量为__________ mg/L。
(6)下列说法正确的是__________。
已知:①测定原理为甲醛把
 还原成
还原成 ,产生的
,产生的 与
与 定量反应生成
定量反应生成 ,
, 与菲洛嗪形成有色配合物,通过测定吸光度计算出甲醛的含量;
与菲洛嗪形成有色配合物,通过测定吸光度计算出甲醛的含量;②吸光度用A表示,计算公式为
 ,其中a为吸光度系数,b为光在样本中经过的距离,c为溶液浓度。
,其中a为吸光度系数,b为光在样本中经过的距离,c为溶液浓度。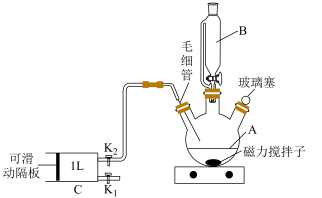
(1)仪器A的名称是
(2)制备银氨溶液,仪器B中放置的药品是
 溶液”或“氨水”)。
溶液”或“氨水”)。(3)选择正确的操作,完成室内空气中甲醛含量的测定:
操作①:取下玻璃塞→操作②:__________→操作③:__________→操作④:使可滑动隔板处于最右端→操作⑤:__________→操作⑥:__________→操作⑦:__________→
a.打开
 ,关闭
,关闭 b.打开
b.打开 ,关闭
,关闭
c.将可滑动隔板拉至最左端 d.热水浴加热仪器A
e.将可滑动隔板缓慢推至最右端 f.将可滑动隔板迅速推至最右端
(4)写出甲醛与银氨溶液反应的化学方程式
(5)将仪器A中溶液的
 调至1,加入足量
调至1,加入足量 溶液,充分反应后加入菲洛嗪,通过测定吸光度确定生成
溶液,充分反应后加入菲洛嗪,通过测定吸光度确定生成 1.12mg,则空气中甲醛的含量为
1.12mg,则空气中甲醛的含量为(6)下列说法正确的是__________。
| A.本实验缺少尾气处理装置 |
| B.实验应在室内不同点位进行空气取样,以保证数据的准确性 |
C.毛细管的作用是减小空气通入速率,保证空气中的 被吸收完全 被吸收完全 |
| D.有色配合物浓度越大,测得吸光度数值越大 |
您最近半年使用:0次
8 . 某碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下方案:①称取碱式碳酸镁样品mg;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用电子天平称量)。
(1)下列仪器中,该方案不会用到的是________ 。___________ ;本实验至少需要称量___________ 次。
(3)某研究小组进行三次实验,数据记录如下:
通过计算,该样品中碱式碳酸镁的纯度为___________ 。(4MgCO3·Mg(OH)2·4H2O式量466;写出简要的步骤)
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2 MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?___________ (填“正确”或“错误”),请说明自己的理由:___________ 。
(1)下列仪器中,该方案不会用到的是
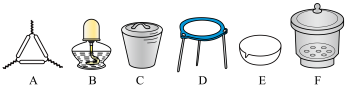
(3)某研究小组进行三次实验,数据记录如下:
| 样品质量/g | 剩余固体质量/g | |
| 实验1 | 18.000 | 8.000 |
| 实验2 | 18.000 | 8.020 |
| 实验3 | 18.000 | 7.980 |
(4)有同学认为高温煅烧过程中会发生MgCO3+SiO2
 MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
MgSiO3+CO2↑,会导致测定结果有误,你认为这位同学的观点正确吗?
您最近半年使用:0次
解题方法
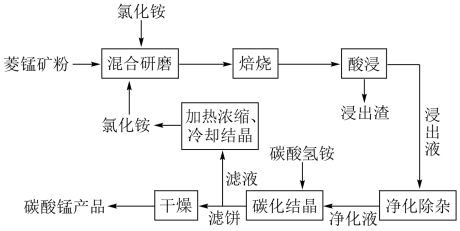
9 . 工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示: 其余为
其余为 等元素。
等元素。
②部分阳离子沉淀时溶液的 :
:
③“焙烧”过程中主要反应为 。
。
(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、 分别为
分别为___________ 、___________ 、___________ 。 ,作用是
,作用是___________ ,再调节溶液 的范围为
的范围为___________ ,将 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将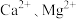 变为氟化物沉淀除去。
变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为___________ 。
(4)上述流程中可循环使用的物质是___________ (填化学式)。
(5)现用滴定法测定产品中锰的含量。实验步骤:称取 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应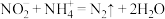 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用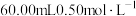 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为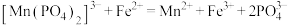 ;用
;用 酸性
酸性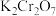 溶液恰好除去过量的
溶液恰好除去过量的 。
。
①酸性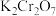 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为___________ 。
②试样中锰的质量分数为___________ 。
 其余为
其余为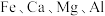 等元素。
等元素。②部分阳离子沉淀时溶液的
 :
:| 离子 |  |  |  |  |  |
开始沉淀的 | 4.1 | 2.2 | 10.6 | 8.1 | 9.1 |
沉淀完全的 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
 。
。(1)结合图1、2、3,分析“焙烧”过程中最佳的焙烧温度、焙烧时间、
 分别为
分别为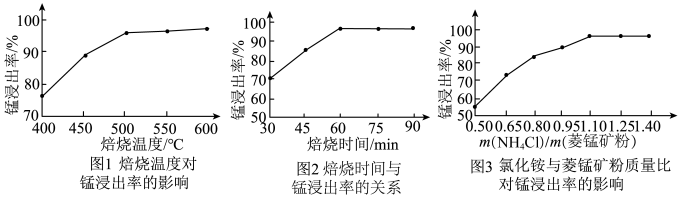
 ,作用是
,作用是 的范围为
的范围为 和
和 变为沉淀而除去,然后加入
变为沉淀而除去,然后加入 将
将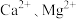 变为氟化物沉淀除去。
变为氟化物沉淀除去。(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为
(4)上述流程中可循环使用的物质是
(5)现用滴定法测定产品中锰的含量。实验步骤:称取
 试样,向其中加入稍过量的磷酸和硝酸,加热使产品中
试样,向其中加入稍过量的磷酸和硝酸,加热使产品中 完全转化为
完全转化为 (其中
(其中 转化为
转化为 );加入稍过量的硫酸铵,发生反应
);加入稍过量的硫酸铵,发生反应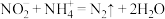 以除去
以除去 ;加入稀硫酸酸化,用
;加入稀硫酸酸化,用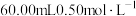 硫酸亚铁铵标准溶液进行滴定,发生的反应为
硫酸亚铁铵标准溶液进行滴定,发生的反应为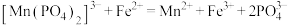 ;用
;用 酸性
酸性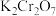 溶液恰好除去过量的
溶液恰好除去过量的 。
。①酸性
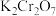 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为②试样中锰的质量分数为
您最近半年使用:0次
10 . 利用滴定法可以测定胆矾中铜的含量,原理如下:
①2Cu2+ + 4I–=2CuI↓+ I2 ②I2 +2 S2O32–=2I–+S4O62–
1.需加入的指示剂为___________ ;需要的物理量除胆矾晶体的质量外,还需要___________ ;判定滴定终点的方法为___________ 。
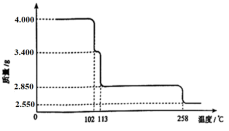
2.将制得的胆矾(CuSO4•5H2O)进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。试确定200℃时固体物质的化学式___________ 。(写出计算过程)
①2Cu2+ + 4I–=2CuI↓+ I2 ②I2 +2 S2O32–=2I–+S4O62–
1.需加入的指示剂为
2.将制得的胆矾(CuSO4•5H2O)进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。试确定200℃时固体物质的化学式
您最近半年使用:0次



