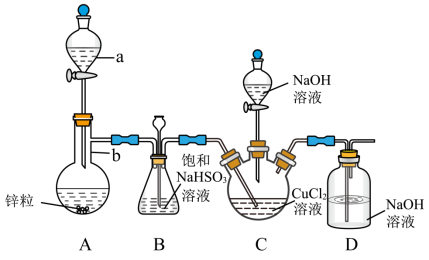
1 . CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装置略去)将SO2通入新制氢氧化铜悬浊液中制备CuCl。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有 的操作方法是
的操作方法是_______ 。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有
 的操作方法是
的操作方法是
您最近半年使用:0次
2 .  溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
已知:
ⅰ.
ⅱ.某些盐的溶解性(注: 、
、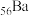 同主族)
同主族)
ⅲ. 、
、 、
、 、
、 、ZnS均可被
、ZnS均可被 氧化。
氧化。
(1)查阅资料可知,溶液变黄是因为生成了 ,
, 转化为
转化为 时,溶液的pH会
时,溶液的pH会___________ (填“升高”或“降低”)。
(2)探究溶液A中含硫粒子的种类。 和
和___________ (填离子符号)。
②向少量含淀粉的稀碘水中滴加滤液2(已调至中性),___________ (填现象),证实溶液A中有 。
。
③加入过量 溶液的目的是
溶液的目的是___________ 。
(3)利用如下实验可测定 中x的值。
中x的值。
【实验原理】 ,其中
,其中 和
和 的化学计量数之比等于
的化学计量数之比等于___________ 。通过测定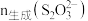 和
和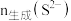 可确定x的值。
可确定x的值。
【实验过程】
实验Ⅰ 的目的是除去
的目的是除去 ,相关离子方程式是
,相关离子方程式是___________ 。
②实验Ⅱ中操作X是加入___________ (补全试剂和操作)。
③用 标准溶液滴定
标准溶液滴定___________ (填序号,下同),可确定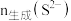 ;再用
;再用 标准溶液滴定
标准溶液滴定___________ ,可确定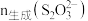 。(说明:滴定过程中需调节pH)
。(说明:滴定过程中需调节pH)
a.溶液A b.溶液 c.沉淀E d.溶液F
c.沉淀E d.溶液F
【数据处理】计算x的值。
 溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。
溶液久置变为黄色(记为溶液A)。探究溶液A中阴离子的种类。已知:
ⅰ.

ⅱ.某些盐的溶解性(注:
 、
、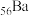 同主族)
同主族)| 盐 | ZnS(白色) | CuS(黑色) | SrS | 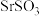 |  |  |
| 溶解性 | 难溶 | 极难溶 | 易溶 | 难溶 | 难溶 | 易溶 |
 、
、 、
、 、
、 、ZnS均可被
、ZnS均可被 氧化。
氧化。(1)查阅资料可知,溶液变黄是因为生成了
 ,
, 转化为
转化为 时,溶液的pH会
时,溶液的pH会(2)探究溶液A中含硫粒子的种类。
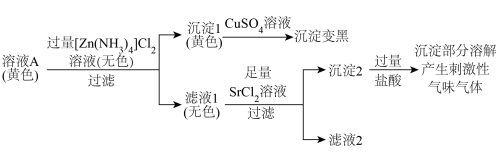
 和
和②向少量含淀粉的稀碘水中滴加滤液2(已调至中性),
 。
。③加入过量
 溶液的目的是
溶液的目的是(3)利用如下实验可测定
 中x的值。
中x的值。【实验原理】
 ,其中
,其中 和
和 的化学计量数之比等于
的化学计量数之比等于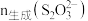 和
和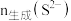 可确定x的值。
可确定x的值。【实验过程】
实验Ⅰ

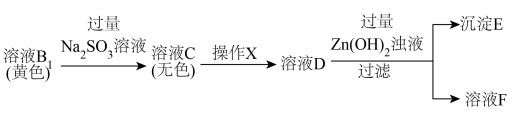
 的目的是除去
的目的是除去 ,相关离子方程式是
,相关离子方程式是②实验Ⅱ中操作X是加入
③用
 标准溶液滴定
标准溶液滴定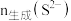 ;再用
;再用 标准溶液滴定
标准溶液滴定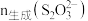 。(说明:滴定过程中需调节pH)
。(说明:滴定过程中需调节pH)a.溶液A b.溶液
 c.沉淀E d.溶液F
c.沉淀E d.溶液F【数据处理】计算x的值。
您最近半年使用:0次
3 . 根据下列实验操作及现象得出的结论正确的是
| 选项 | 操作及现象 | 结论 |
| A | 向某溶液中滴加盐酸,产生无色无味气体 | 该溶液中含有 |
| B | 将铁的氧化物溶于稀硝酸中,滴加 溶液,溶液变红色 溶液,溶液变红色 | 该氧化物一定是 |
| C | 向某溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 | 该溶液中含有 |
| D | 某样品进行焰色试验,焰色呈黄色 | 该样品可能是纯碱 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 室温下,探究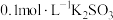 溶液的性质,下列实验方案能达到探究目的的是
溶液的性质,下列实验方案能达到探究目的的是
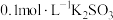 溶液的性质,下列实验方案能达到探究目的的是
溶液的性质,下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A | 溶液中是否含有 | 用铂丝或螺旋状的铜丝蘸取溶液,在酒精灯火焰上灼烧,观察火焰颜色 |
| B |  是否被氧化变质 是否被氧化变质 | 向2mL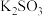 溶液中加入足量盐酸酸化,再滴加 溶液中加入足量盐酸酸化,再滴加 溶液,观察有无白色沉淀生成 溶液,观察有无白色沉淀生成 |
| C |  是否具有氧化性 是否具有氧化性 | 向2mL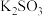 溶液中滴加 溶液中滴加 溶液,再滴加几滴KOH溶液,观察是否浑浊 溶液,再滴加几滴KOH溶液,观察是否浑浊 |
| D |  是否水解 是否水解 | 向2mL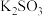 溶液中滴加2~3滴甲基橙溶液,观察溶液颜色变化 溶液中滴加2~3滴甲基橙溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 下列对某溶液中离子检验的方法、现象与结论的描述中,均正确的是
A.加入 溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有 存在 存在 |
| B.取某溶液少量,进行焰色反应,观察到火焰呈黄色,说明原溶液一定是钠盐溶液 |
C.取某溶液少量,加入烧碱溶液并加热,生成使蓝色石蕊试纸变红的气体,说明原溶液中有 |
D.取某溶液少量,加入足量盐酸无现象,再加入几滴氯化钡溶液,有白色沉淀,说明原溶液中有 |
您最近半年使用:0次
6 . 下列物质的检验中,其结论一定正确的是
A.向某溶液中加入BaCl2溶液,产生白色沉淀,加入稀HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有 |
B.向某溶液中加入盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有 或 或 |
| C.取少量久置的Na2SO3样品于试管中加水溶解,再加足量盐酸酸化,然后加BaCl2溶液,若加盐酸时有气体产生,加BaCl2溶液时有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
D.向某溶液中滴加NaOH溶液并加热,用湿润的蓝色石蕊试纸检验产生的气体,若试纸变红,该溶液中含有 |
您最近半年使用:0次
名校
7 . 下列关于物质的除杂、鉴别、检验的方法中错误的是
A.除去 溶液中 溶液中 的方法是往溶液中缓缓通入氧气 的方法是往溶液中缓缓通入氧气 |
B. 与溴蒸气的鉴别可以用水、 与溴蒸气的鉴别可以用水、 溶液或 溶液或 ,但不能用湿润的碘化钾淀粉试纸 ,但不能用湿润的碘化钾淀粉试纸 |
C.检验 是否变质,可取少量样品溶解并滴加 是否变质,可取少量样品溶解并滴加 溶液,观察溶液是否褪色 溶液,观察溶液是否褪色 |
D.检验 溶液是否变质,可取少量样品于试管中并滴加KSCN,观察溶液是否变红 溶液是否变质,可取少量样品于试管中并滴加KSCN,观察溶液是否变红 |
您最近半年使用:0次
8 . 根据下列各实验的操作和现象所得出的结论错误的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将 分别通入品红的乙醇溶液和品红的水溶液 分别通入品红的乙醇溶液和品红的水溶液 | 品红的乙醇溶液不褪色,品红的水溶液慢慢褪色 | 使品红褪色的不是 ,而是 ,而是 与水反应后的产物 与水反应后的产物 |
| B | 向 溶液中通入 溶液中通入 | 有淡黄色沉淀产生 | 氧化性: |
| C | 向某待测溶液中滴加 溶液 溶液 | 有白色沉淀产生 | 该溶液中含有 |
| D | 向蔗糖中滴入浓硫酸 | 蔗糖变黑后膨胀,同时有刺激性气味的气体产生 | 浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列实验操作对应的现象和根据现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某溶液中加盐酸 | 产生无色无味的气体能使澄清石灰水变浑浊 | 溶液中一定有 |
| B | 碳和浓硫酸加热所得气体产物依次通过品红溶液和澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 气体产物中含有 和 和 |
| C | 将灼烧至黑色的铜丝插入无水乙醇 | 铜丝变成红色 | 乙醇发生氧化反应 |
| D | 向溶液中加入 溶液、加热,试管口用湿润的蓝色石蕊试纸检验 溶液、加热,试管口用湿润的蓝色石蕊试纸检验 | 试纸不显红色 | 溶液中不含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物。某化学兴趣小组进行以下有关实验,填写下列空白。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有___________ (填标号)。
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是___________ 。
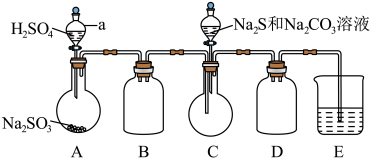
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验___________ 。
(3)装置D的作用是___________ 。
(4)实验中,为使 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是___________ 。
实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。
(5)样品中Na2S2O3的百分含量为___________ (保留三位有效数字)。
实验Ⅰ:证明Na2SO3中硫元素的价态能发生+4→+6转化
(1)实验中,不需要用到的试剂有
a.稀硫酸 b.H2O2溶液 c.稀盐酸 d.淀粉碘化钾溶液 e.BaCl2溶液
观察到的现象是
实验Ⅱ:制取硫代硫酸钠
利用如图所示装置进行实验
(3)装置D的作用是
(4)实验中,为使
 缓慢通入烧瓶C,采取的操作是
缓慢通入烧瓶C,采取的操作是实验Ⅲ:测定某硫代硫酸钠样品的纯度(设样品中只含Na2SO3杂质)
设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品7.9g,配制成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用0.1mol·L-1I2标准溶液滴定(发生反应:2S2O
 +I2=S4O
+I2=S4O +2I-),至滴定终点共消耗标准溶液23.60mL。
+2I-),至滴定终点共消耗标准溶液23.60mL。(5)样品中Na2S2O3的百分含量为
您最近半年使用:0次



