29.
亚氯酸钠(NaClO2)是一种重要漂白剂,某探究小组开展如下实验,回答下列问题:实验Ⅰ:制取NaClO2晶体,按如下图装置进行制取。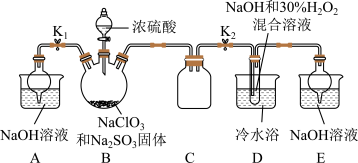 已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。(1)已知装置B中的产物有ClO2气体,装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还可能含有的一种阴离子是________;检验该离子的方法是________。(2)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。(1)已知装置B中的产物有ClO2气体,装置B中反应后的溶液中阴离子除了ClO2﹣、ClO3﹣、Cl﹣、ClO﹣、OH﹣外还可能含有的一种阴离子是________;检验该离子的方法是________。(2)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。①减压,55℃蒸发结晶;②
________;③用38℃~60℃热水洗涤;④低于60℃干燥;得到成品并转移产品。操作的四个步骤中都用到的玻璃仪器是
________。
(3)D中用冷水浴,其目的是
________(回答一点即可)。
实验Ⅱ:样品杂质分析与纯度测定(4)测定样品中NaClO2的纯度.测定时进行如下实验:①准确称0.4000g样品,加入适量蒸馏水和过量的KI晶体和硫酸,发生如下反应:ClO
2﹣+4I
﹣+4H
+=2H
2O+2I
2+Cl
﹣②将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用0.200 mol•L
﹣1 Na
2S
2O
3标准液滴定至终点,测得消耗标准溶液体积的平均值为15.00mL(已知:I
2+2S
2O
32﹣=2I
﹣+S
4O
62﹣)。判定滴定到终点的标准是
_______________________;请计算所称取的样品中NaClO
2的质量分数? 并写出计算过程
______。