名校
解题方法
1 . 钠是一种活泼金属,其单质及化合物在科研、生产中有重要的作用。
(1)基态钠原子核外电子的空间运动状态有___________ 种。
(2)冰晶石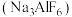 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。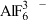 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是___________ (填字母)。
A. B.
B. C.
C. D.
D.
② 晶体中存在的作用力有
晶体中存在的作用力有___________ (填字母)。
A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3) 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是___________ 。
(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为___________ ,硼氢化钠晶胞中与 紧邻的
紧邻的 个数是
个数是___________ 。
(5)有研究表明,在超高压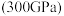 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成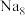 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示: 的最短距离为
的最短距离为___________  (用含a的代数式表示)。
(用含a的代数式表示)。
(1)基态钠原子核外电子的空间运动状态有
(2)冰晶石
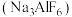 是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示),
是铝电解的助熔剂,其晶胞与氯化钠的晶胞结构相似(如图所示), 占据的位置相当于氯化钠晶胞中
占据的位置相当于氯化钠晶胞中 占据的位置。
占据的位置。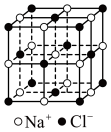
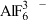 是正八面体结构,中心原子的杂化方式是
是正八面体结构,中心原子的杂化方式是A.
 B.
B. C.
C. D.
D.
②
 晶体中存在的作用力有
晶体中存在的作用力有A.非极性共价键 B.配位键 C.范德华力 D.离子键
(3)
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,其原因是
,其原因是(4)硼氢化钠是一种常用的还原剂和催化剂。硼氢化钠的晶胞结构如图所示。
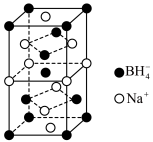
 ,硼氢化钠溶于水的化学方程式为
,硼氢化钠溶于水的化学方程式为 紧邻的
紧邻的 个数是
个数是(5)有研究表明,在超高压
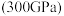 下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成
下,金属钠和氦之间可形成化合物电子盐(即电子是阴离子),在这一结构中,钠离子主要是按照简单立方排列的(如图1),并且形成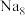 立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
立方体空隙,电子对(2e-)和氦原子交替分布填充在立方体的中心。晶体结构俯视图如图2所示:
 的最短距离为
的最短距离为 (用含a的代数式表示)。
(用含a的代数式表示)。
您最近一年使用:0次
名校
解题方法
2 . 化学之美随处可见。下列说法正确的是
| A.天然色素红曲红可从植物或者微生物中得到 |
| B.苯是单双键交替的正六边形结构 |
| C.碘升华时会产生大量紫色蒸气,该过程有共价键断裂 |
| D.用X射线衍射仪照射水晶时,记录仪上不会产生明锐的衍射峰 |
您最近一年使用:0次
昨日更新
|
167次组卷
|
3卷引用:广东省部分学校2024届高三下学期5月份大联考化学试题
名校
解题方法
3 . 对于超分子聚合物和材料的组装而言, 配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是
配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是 —为甲基。
—为甲基。
 配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是
配位键的动态性质和易于调节的特性起着重要作用。某种超分子的结构如图。下列叙述错误的是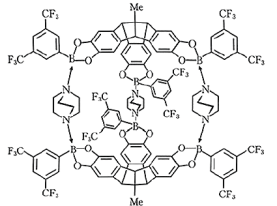
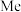 —为甲基。
—为甲基。A.该超分子形成的 配位键中, 配位键中, 原子提供孤电子对 原子提供孤电子对 |
B.该超分子中涉及的元素均为 区元素 区元素 |
| C.超分子具有分子识别和自组装的特征 |
D.第一电离能: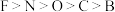 |
您最近一年使用:0次
昨日更新
|
120次组卷
|
3卷引用:河北省保定市九校2024届高三下学期二模化学试题
解题方法
4 . 如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:_______ ,其最高能层的电子占据的原子轨道电子云轮廓为_______ 形。若将其最高价氧化物的水化物溶于氨水中可得到一种透明的深蓝色溶液,写出反应的化学方程式为:_______ 。
(2)第二周期所有元素中第一电离能介于⑤⑦之间的有_______ 种。由②③④形成的简单离子半径由小到大顺序是_______ (填化学用语)。
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式_______ ,该分子为_______ (填“极性分子”或“非极性分子”。
(4)元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式_______ ,它的熔点高,硬度大,电绝缘性好,化学性质稳定,它的晶体类型是_______ 。
(5)下列有关性质的比较正确且能用元素周期律解释的是_______(填标号)。
(6)一种由②和⑤两种元素形成化合物的晶胞如图所示,该晶胞的化学式为_______ 。

(2)第二周期所有元素中第一电离能介于⑤⑦之间的有
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(4)元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式
(5)下列有关性质的比较正确且能用元素周期律解释的是_______(填标号)。
| A.第一电离能:②>③ |
| B.单质的氧化性:⑦>⑧ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ |
| D.氢化物的沸点:③>⑦ |
(6)一种由②和⑤两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

您最近一年使用:0次
解题方法
5 . Ga与B、Al处于同一主族,氮化镓是制造LED的重要材料,被誉为第三代半导体材料。回答下列问题:
(1)基态Ga原子的价电子排布式为___________ 。
(2)Be、B、C的电负性由小到大的顺序为___________ ,第一电离能由小到大的顺序为___________ 。
(3)①乙硼烷( )的结构如图,其中B原子的轨道杂化类型是
)的结构如图,其中B原子的轨道杂化类型是___________ 。 与
与 反应生成环氮硼烷(
反应生成环氮硼烷( 具有规则的平面六角形环状结构),写出一种与
具有规则的平面六角形环状结构),写出一种与 原子总数相同、价电子总数相同的分子
原子总数相同、价电子总数相同的分子___________ 。 极易水解,从配位角度解释原因
极易水解,从配位角度解释原因___________ 。
③B和N形成的BN有石墨型与金刚石型结构,金刚石型BN的硬度大于金刚石,原因是___________ 。
(4)氮化镓的一种晶体结构如图所示(属六方晶系),Ga的配位数为___________ ,晶体的密度为___________  (用含a、c、
(用含a、c、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态Ga原子的价电子排布式为
(2)Be、B、C的电负性由小到大的顺序为
(3)①乙硼烷(
 )的结构如图,其中B原子的轨道杂化类型是
)的结构如图,其中B原子的轨道杂化类型是 与
与 反应生成环氮硼烷(
反应生成环氮硼烷( 具有规则的平面六角形环状结构),写出一种与
具有规则的平面六角形环状结构),写出一种与 原子总数相同、价电子总数相同的分子
原子总数相同、价电子总数相同的分子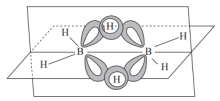
 极易水解,从配位角度解释原因
极易水解,从配位角度解释原因③B和N形成的BN有石墨型与金刚石型结构,金刚石型BN的硬度大于金刚石,原因是
(4)氮化镓的一种晶体结构如图所示(属六方晶系),Ga的配位数为
 (用含a、c、
(用含a、c、 的代数式表示,
的代数式表示, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。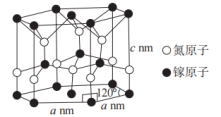
您最近一年使用:0次
名校
解题方法
6 . 某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为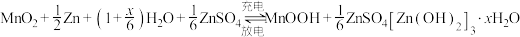 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是___________ (填名称,下同),存在分子间作用力的是___________ ;属于共价晶体的是___________ 。 中
中 的化合价是
的化合价是_________ ,有机高聚物中C的杂化方式为__________ 。
(3) 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是___________ 。 的第二电离能
的第二电离能___________ (填“大于”或“小于”) 。
。
(4)一种新型稀磁半导体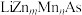 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。___________ ,n=___________ 。
②已知 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,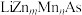 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为___________ nm(列出计算式)。
 溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为
溶液的有机高聚物(结构片段如图所示)作固态电解质,其电池总反应为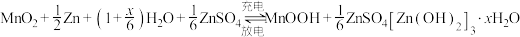 ,电池结构如图所示。
,电池结构如图所示。
(1)如图所示的几种含碳物质中,不与碳纳米管互为同素异形体的是

 中
中 的化合价是
的化合价是(3)
 键中离子键成分的百分数小于
键中离子键成分的百分数小于 键,原因是
键,原因是 的第二电离能
的第二电离能 。
。(4)一种新型稀磁半导体
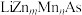 的立方晶胞结构如图所示。
的立方晶胞结构如图所示。
②已知
 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,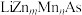 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为 。该晶体中
。该晶体中 原子与
原子与 原子之间的最短距离为
原子之间的最短距离为
您最近一年使用:0次
名校
解题方法
7 . 请回答下列问题。
(1)染发剂中普遍含有对苯二胺(其化学式为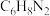 )会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此:慎用染发剂,少染发为好。一个对苯二胺分子中碳氢氮原子最简个数比
)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此:慎用染发剂,少染发为好。一个对苯二胺分子中碳氢氮原子最简个数比_______ 。
(2)请判断下列物质之间的关系:A.同系物,B.同分异构体。2-甲基丁烷和丁烷_______ ;(填“A”或者“B”)异戊烷和2,2-二甲基丙烷_______ ;(填“A”或者“B”)
(3)单烯烃通式:(链状烯烃只含有一个碳碳双键),其通式为_______ 。
(4)请写出异丁烷的结构简式_______
(5)( )和(
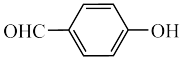
)和(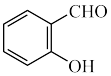 )两种有机物是同分异构体,已知易形成分子间氢键的物质沸点更高,则沸点更低芳香族化合物的命名为
)两种有机物是同分异构体,已知易形成分子间氢键的物质沸点更高,则沸点更低芳香族化合物的命名为_______ 。
(6)① 、②
、② 、③
、③ 三种分子中,键角由大到小的顺序
三种分子中,键角由大到小的顺序_______ 。
(7)苯丙氨酸(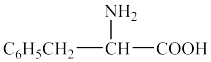 )有多种同分异构体,其中同时符合条件:①有带两个取代基的苯环②有一个硝基直接连接在苯环上的同分异构体有
)有多种同分异构体,其中同时符合条件:①有带两个取代基的苯环②有一个硝基直接连接在苯环上的同分异构体有_______ 种(不考虑立体异构)。
(1)染发剂中普遍含有对苯二胺(其化学式为
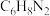 )会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此:慎用染发剂,少染发为好。一个对苯二胺分子中碳氢氮原子最简个数比
)会使易过敏的人引起发痒、水肿、气喘、胃炎和贫血等症状,另外它还具有致癌作用。因此:慎用染发剂,少染发为好。一个对苯二胺分子中碳氢氮原子最简个数比(2)请判断下列物质之间的关系:A.同系物,B.同分异构体。2-甲基丁烷和丁烷
(3)单烯烃通式:(链状烯烃只含有一个碳碳双键),其通式为
(4)请写出异丁烷的结构简式
(5)(
 )和(
)和( )两种有机物是同分异构体,已知易形成分子间氢键的物质沸点更高,则沸点更低芳香族化合物的命名为
)两种有机物是同分异构体,已知易形成分子间氢键的物质沸点更高,则沸点更低芳香族化合物的命名为(6)①
 、②
、② 、③
、③ 三种分子中,键角由大到小的顺序
三种分子中,键角由大到小的顺序(7)苯丙氨酸(
 )有多种同分异构体,其中同时符合条件:①有带两个取代基的苯环②有一个硝基直接连接在苯环上的同分异构体有
)有多种同分异构体,其中同时符合条件:①有带两个取代基的苯环②有一个硝基直接连接在苯环上的同分异构体有
您最近一年使用:0次
解题方法
8 . Cu(Ⅱ)可形成多种配合物,呈现出多样化的性质和用途。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出 晶体。
晶体。
①产生蓝色沉淀的离子方程式是___________ 。
② 在水中电离的方程式是
在水中电离的方程式是___________ 。
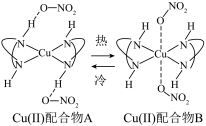
(2)如下图所示, Cu(Ⅱ)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。 的价层电子排布式为
的价层电子排布式为___________ 。
② 、
、 、
、 的第一电离能由大到小顺序为
的第一电离能由大到小顺序为___________ 。
③A中氮原子与其它原子(或离子)之间存在的作用力类型有___________ ,氢原子与其它原子之间存在的作用力类型有___________ 。
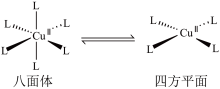
④已知:当Cu(Ⅱ)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。___________ 。
(3)已知:
①
②蓝色溶液与黄色溶液混合为绿色溶液,在 溶液中加入
溶液中加入 浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因
浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因___________ 。
(4)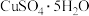 脱水过程中部分中间体的结构示意图如下图。
脱水过程中部分中间体的结构示意图如下图。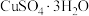 写成配合物形式为
写成配合物形式为___________ ,其转化为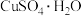 过程中,破坏的分子间作用力是
过程中,破坏的分子间作用力是___________ 。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出
 晶体。
晶体。①产生蓝色沉淀的离子方程式是
②
 在水中电离的方程式是
在水中电离的方程式是(2)如下图所示, Cu(Ⅱ)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。
 的价层电子排布式为
的价层电子排布式为②
 、
、 、
、 的第一电离能由大到小顺序为
的第一电离能由大到小顺序为③A中氮原子与其它原子(或离子)之间存在的作用力类型有
④已知:当Cu(Ⅱ)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。
(3)已知:
①
| 物质 | 颜色 |
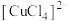 | 黄色 |
 | 蓝色 |
 溶液中加入
溶液中加入 浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因
浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因(4)
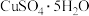 脱水过程中部分中间体的结构示意图如下图。
脱水过程中部分中间体的结构示意图如下图。
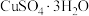 写成配合物形式为
写成配合物形式为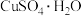 过程中,破坏的分子间作用力是
过程中,破坏的分子间作用力是
您最近一年使用:0次
解题方法
9 . 下列有关物质结构和性质的说法正确的是
| A.晶体中有阳离子,不一定有阴离子 |
B. 中的H-O-H键角比水中的小 中的H-O-H键角比水中的小 |
| C.共价键的键能越大,分子晶体的熔点越高 |
| D.非金属元素都位于元素周期表中的p区 |
您最近一年使用:0次
名校
解题方法
10 . 氟化物在生产、生活和科研中应用广泛。请回答下列问题:
(1)基态氟原子核外电子的空间运动状态有________ 种,核外电子的最高能级的原子轨道相互________ 。
(2)夜明珠的主要成分是 。
。 难溶于水,但可溶于含
难溶于水,但可溶于含 的溶液中,其反应为
的溶液中,其反应为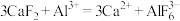 ,下列对
,下列对 中心原子杂化方式推断合理的是________(填字母)。
中心原子杂化方式推断合理的是________(填字母)。
(3) 与一定量的水形成
与一定量的水形成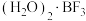 ,一定条件下
,一定条件下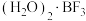 可发生如下转化:
可发生如下转化:________ (填“无”或“有”)离子键形成。 (该物质仍具有润滑性),其单层局部结构如图所示。
(该物质仍具有润滑性),其单层局部结构如图所示。 的导电性
的导电性________ (填“增强”或“减弱”)。
②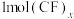 中含有
中含有________ molσ键(用含x的代数式表示)。
(5) 晶体属四方晶系(晶胞参数
晶体属四方晶系(晶胞参数 ),晶胞中代表Xe的是
),晶胞中代表Xe的是________ 球(填“黑”或“白”)。已知晶胞中A、B原子间距离为xpm,则B、C间距离为________ pm(用含a、c、x的代数式表示)。
(1)基态氟原子核外电子的空间运动状态有
(2)夜明珠的主要成分是
 。
。 难溶于水,但可溶于含
难溶于水,但可溶于含 的溶液中,其反应为
的溶液中,其反应为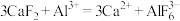 ,下列对
,下列对 中心原子杂化方式推断合理的是________(填字母)。
中心原子杂化方式推断合理的是________(填字母)。A. | B. | C. | D. |
(3)
 与一定量的水形成
与一定量的水形成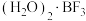 ,一定条件下
,一定条件下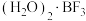 可发生如下转化:
可发生如下转化: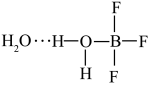

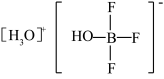
②多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”,如 分子中存在“离域π键”,可表示成
分子中存在“离域π键”,可表示成 。实验测得
。实验测得 中硼氟键的键长比
中硼氟键的键长比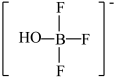 中B-F键的键长小,原因是
中B-F键的键长小,原因是
 (该物质仍具有润滑性),其单层局部结构如图所示。
(该物质仍具有润滑性),其单层局部结构如图所示。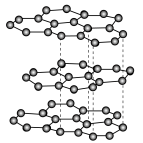
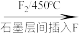
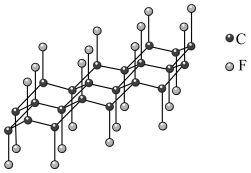
 的导电性
的导电性②
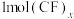 中含有
中含有(5)
 晶体属四方晶系(晶胞参数
晶体属四方晶系(晶胞参数 ),晶胞中代表Xe的是
),晶胞中代表Xe的是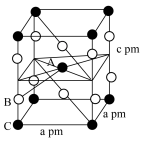
您最近一年使用:0次



