解题方法
1 . 部分含氮物质的分类与相应化合物关系如图所示。下列说法错误的是

| A.b具有碱性和还原性 |
| B.反应Ⅰ中氧化产物和还原产物的物质的量之比为1∶1 |
C.反应Ⅱ过程中生成0.1mol  时,转移1mol电子 时,转移1mol电子 |
| D.反应Ⅲ能有效降低水体中的氮元素含量 |
您最近一年使用:0次
2 . 废水中过量氨氮( 、
、 )会导致水体富营养化,去除氨氮的研究一直备受关注。
)会导致水体富营养化,去除氨氮的研究一直备受关注。
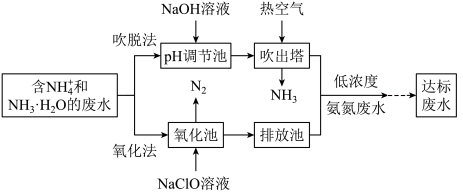
I.吹脱法、氧化法除氨氮 调节池”中加入
调节池”中加入 溶液的目的是
溶液的目的是______________________ 。
(2)“吹出塔”用热空气比用冷空气吹脱效果更好的原因是______________________ 。
(3)①写出酸性条件下 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:______________________ 。
②为研究空气对 氧化氨氮的影响,其他条件不变,仅增加单位时间内通入的空气量,发现氨氮去除率几乎不变。其原因可能是
氧化氨氮的影响,其他条件不变,仅增加单位时间内通入的空气量,发现氨氮去除率几乎不变。其原因可能是___________ (填标号)。
A. 氧化性比
氧化性比 弱 B.
弱 B. 在溶液中溶解度小 C.空气中
在溶液中溶解度小 C.空气中 进入溶液中
进入溶液中
Ⅱ.生物脱氨氮法

(4)理论上,参与I、Ⅱ中反应的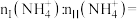
___________ 时,氨氮的脱除效果最好。
(5)废水中溶解氧浓度对氨氮的脱除率的影响如图所示。当溶解氧浓度在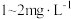 之间时,随着溶解氧浓度的增大,氨氮的脱除率下降,其原因可能有:氧气浓度越高厌氧氨氧化细菌活性越低、
之间时,随着溶解氧浓度的增大,氨氮的脱除率下降,其原因可能有:氧气浓度越高厌氧氨氧化细菌活性越低、___________ 。
 、
、 )会导致水体富营养化,去除氨氮的研究一直备受关注。
)会导致水体富营养化,去除氨氮的研究一直备受关注。I.吹脱法、氧化法除氨氮
 调节池”中加入
调节池”中加入 溶液的目的是
溶液的目的是(2)“吹出塔”用热空气比用冷空气吹脱效果更好的原因是
(3)①写出酸性条件下
 氧化
氧化 生成
生成 的离子方程式:
的离子方程式:②为研究空气对
 氧化氨氮的影响,其他条件不变,仅增加单位时间内通入的空气量,发现氨氮去除率几乎不变。其原因可能是
氧化氨氮的影响,其他条件不变,仅增加单位时间内通入的空气量,发现氨氮去除率几乎不变。其原因可能是A.
 氧化性比
氧化性比 弱 B.
弱 B. 在溶液中溶解度小 C.空气中
在溶液中溶解度小 C.空气中 进入溶液中
进入溶液中Ⅱ.生物脱氨氮法

(4)理论上,参与I、Ⅱ中反应的
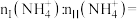
(5)废水中溶解氧浓度对氨氮的脱除率的影响如图所示。当溶解氧浓度在
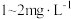 之间时,随着溶解氧浓度的增大,氨氮的脱除率下降,其原因可能有:氧气浓度越高厌氧氨氧化细菌活性越低、
之间时,随着溶解氧浓度的增大,氨氮的脱除率下降,其原因可能有:氧气浓度越高厌氧氨氧化细菌活性越低、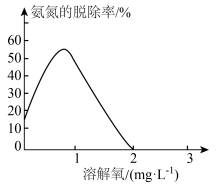
您最近一年使用:0次
名校
3 . 过量使用尿素[CO(NH2)2]会造成水体中氨氮(以 表示)浓度过量,造成水体富营养化,可用
表示)浓度过量,造成水体富营养化,可用 在酸性环境下将其氧化为无害气体除法
在酸性环境下将其氧化为无害气体除法
(1)写出上述反应的离子方程式。___________ 。
(2)若收集到标况下 气体,转移电子的数目为
气体,转移电子的数目为___________ 。
(3)氨氮去除率随 的不断通入先升高后降低,原因是
的不断通入先升高后降低,原因是___________ 。
(4)某废水中氨氮浓度(以 计)为
计)为 ,通入
,通入 ,氨氮去除率为
,氨氮去除率为 。已知氮元素只被氧化为
。已知氮元素只被氧化为 ,则处理每升废水消耗
,则处理每升废水消耗 质量为
质量为______ ?(写出计算过程)
 表示)浓度过量,造成水体富营养化,可用
表示)浓度过量,造成水体富营养化,可用 在酸性环境下将其氧化为无害气体除法
在酸性环境下将其氧化为无害气体除法(1)写出上述反应的离子方程式。
(2)若收集到标况下
 气体,转移电子的数目为
气体,转移电子的数目为(3)氨氮去除率随
 的不断通入先升高后降低,原因是
的不断通入先升高后降低,原因是(4)某废水中氨氮浓度(以
 计)为
计)为 ,通入
,通入 ,氨氮去除率为
,氨氮去除率为 。已知氮元素只被氧化为
。已知氮元素只被氧化为 ,则处理每升废水消耗
,则处理每升废水消耗 质量为
质量为
您最近一年使用:0次
4 . 研究和采取措施去除氮氧化物尾气和水中硝酸盐造成的氮污染备受关注。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化 、NO和
、NO和 等生成
等生成 和
和 。
。
(1)其他条件一定, 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是________ 。
②在酸性水体中,加入NaClO溶液吸收 的离子方程式为
的离子方程式为________ 。
③水体溶液初始pH越小, 转化率越高。其原因是
转化率越高。其原因是________ 。
(2)NaClO吸收液还可以同时脱除烟气中NO和 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
①酸性条件下, 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是________ 。
②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为________ 。
Ⅱ催化还原法
(3)在 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步:________ (补充完整该步反应机理);第二步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。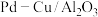 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是________ 。
Ⅰ氧化吸收法 酸性条件下,NaClO溶液氧化
 、NO和
、NO和 等生成
等生成 和
和 。
。(1)其他条件一定,
 转化为
转化为 的转化率随水体溶液初始pH的变化如图1所示。
的转化率随水体溶液初始pH的变化如图1所示。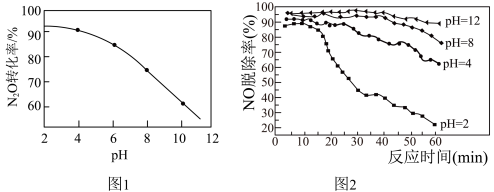
 、NO和
、NO和 三种气体中,相同条件下最易被NaClO氧化的是
三种气体中,相同条件下最易被NaClO氧化的是②在酸性水体中,加入NaClO溶液吸收
 的离子方程式为
的离子方程式为③水体溶液初始pH越小,
 转化率越高。其原因是
转化率越高。其原因是(2)NaClO吸收液还可以同时脱除烟气中NO和
 。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:
。研究发现NaClO吸收液在不同初始pH条件下,对流动烟气的脱硫效率都接近100%,而对NO的脱除率如图2所示:①酸性条件下,
 的脱除率高于NO,其原因除
的脱除率高于NO,其原因除 的还原性比NO强外,还可能是
的还原性比NO强外,还可能是②若用盐酸调节NaClO吸收液pH,不仅不利于NO的吸收,还会在反应过程中生成一种有毒气体,其化学式为
Ⅱ催化还原法
(3)在
 的催化条件下,使用
的催化条件下,使用 作为还原剂,可将水中的
作为还原剂,可将水中的 转化为
转化为 。该反应机理分为三步,如题17图3所示:第一步:
。该反应机理分为三步,如题17图3所示:第一步: 从Cu表面迁移至W的表面;第三步:
从Cu表面迁移至W的表面;第三步: 在W表面吸附并解离为活性氢原子(W-H),W-H将
在W表面吸附并解离为活性氢原子(W-H),W-H将 还原为
还原为 ,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。
,同时W-H将CuO还原为Cu,自身转化为W,实现Cu和W的催化循环。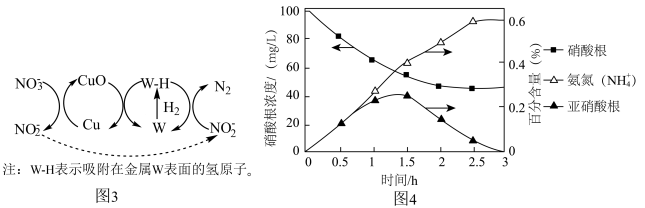
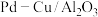 作为还原硝酸盐过程的催化剂,其催化机理与
作为还原硝酸盐过程的催化剂,其催化机理与 相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后,
相似。但还原过程中检测到三种含氮化合物微粒,其浓度变化如图4所示,在1.5小时以后, 的百分含量不断减少,
的百分含量不断减少, 的百分含量不断增多的可能原因是
的百分含量不断增多的可能原因是
您最近一年使用:0次
名校
解题方法
5 . 氮是生物体的重要组成元素同时也会引发环境污染,研究氮的转化对生产、生活有重要价值。
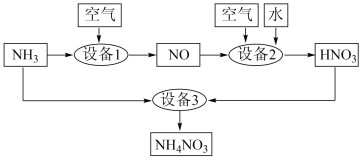
I.某工厂用氨制硝酸和铵盐的流程如图所示。__________________ 。
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为_________ 。
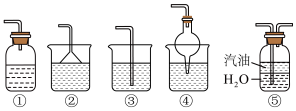
(3)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。________________ 。
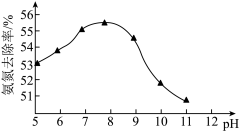
(5)“氧化池”中溶液pH对NaClO去除能力的影响如图所示。_________________ 。“氧化池”中NH3·H2O与NaClO发生反应的的离子方程式为__________________ 。
(6)“硝化池”是在微生物硝化菌(亚硝酸菌和硝酸菌)作用下实现 →
→ →
→ 的转化,根据下图判断使用亚硝酸菌的最佳条件为
的转化,根据下图判断使用亚硝酸菌的最佳条件为_______________ 。 共同作用转化为CO2,N2而排放,其中 CH3OH的作用为
共同作用转化为CO2,N2而排放,其中 CH3OH的作用为_______ (填“氧化剂”或“还原剂”)理论上反应生成的CO2与N2的物质的量之比为_________ 。
I.某工厂用氨制硝酸和铵盐的流程如图所示。
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为
(3)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是
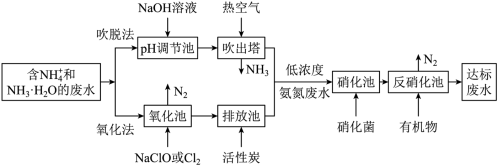
(5)“氧化池”中溶液pH对NaClO去除能力的影响如图所示。
(6)“硝化池”是在微生物硝化菌(亚硝酸菌和硝酸菌)作用下实现
 →
→ →
→ 的转化,根据下图判断使用亚硝酸菌的最佳条件为
的转化,根据下图判断使用亚硝酸菌的最佳条件为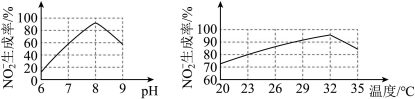
 共同作用转化为CO2,N2而排放,其中 CH3OH的作用为
共同作用转化为CO2,N2而排放,其中 CH3OH的作用为
您最近一年使用:0次
名校
解题方法
6 . 硫氧化率(SOR)和氮氧化率(NOR)通常用来分别表示气体污染物 和
和 向
向 和
和 的转化程度。SOR和NOR的计算公式为:
的转化程度。SOR和NOR的计算公式为: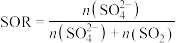 ;
;
已知PM2.5中 主要以
主要以 形式存在,
形式存在, 主要以
主要以 形式存在。
形式存在。 比
比 更稳定;
更稳定; 和
和 加热或光照均易分解。
加热或光照均易分解。
某地SOR和NOR的数据如表所示:
1.由表中数据可知,SOR和NOR差异最大的季节是______ 。
A.春季 B.夏季 C.秋季 D.冬季
结合相关化学原理推测该季节产生这种差异可能的原因______ 。
2.设 ,r值可以较好地反映机动车等移动源污染与燃煤等固定源污染的相对大小。已知某地PM2.5浓度及r值随季节变化如图所示。根据该图分析,造成秋冬季节PM2.5偏高的首要原因是
,r值可以较好地反映机动车等移动源污染与燃煤等固定源污染的相对大小。已知某地PM2.5浓度及r值随季节变化如图所示。根据该图分析,造成秋冬季节PM2.5偏高的首要原因是______ 。
假如你是城市管理者,请你提出一条有针对性的措施,以缓解秋冬季节PM2.5污染较严重的问题______ 。
 和
和 向
向 和
和 的转化程度。SOR和NOR的计算公式为:
的转化程度。SOR和NOR的计算公式为: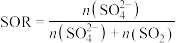 ;
;
已知PM2.5中
 主要以
主要以 形式存在,
形式存在, 主要以
主要以 形式存在。
形式存在。 比
比 更稳定;
更稳定; 和
和 加热或光照均易分解。
加热或光照均易分解。某地SOR和NOR的数据如表所示:
| 季节 | 春季 | 夏季 | 秋季 | 冬季 | 平均 |
| SOR | 0.29 | 0.42 | 0.28 | 0.26 | 0.31 |
| NOR | 0.21 | 0.14 | 0.23 | 0.25 | 0.21 |
1.由表中数据可知,SOR和NOR差异最大的季节是
A.春季 B.夏季 C.秋季 D.冬季
结合相关化学原理推测该季节产生这种差异可能的原因
2.设
 ,r值可以较好地反映机动车等移动源污染与燃煤等固定源污染的相对大小。已知某地PM2.5浓度及r值随季节变化如图所示。根据该图分析,造成秋冬季节PM2.5偏高的首要原因是
,r值可以较好地反映机动车等移动源污染与燃煤等固定源污染的相对大小。已知某地PM2.5浓度及r值随季节变化如图所示。根据该图分析,造成秋冬季节PM2.5偏高的首要原因是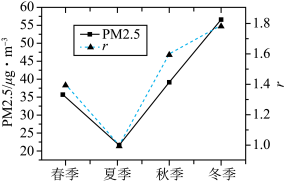
假如你是城市管理者,请你提出一条有针对性的措施,以缓解秋冬季节PM2.5污染较严重的问题
您最近一年使用:0次
名校
解题方法
7 . 氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含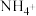 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:

已知: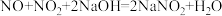

(1)固体1的主要成分有 、
、_________ 、_________ (填化学式)。
(2)若实验室需要配制 溶液
溶液 进行模拟测试,需称取
进行模拟测试,需称取 固体质量为
固体质量为_______  ,并配制溶液,所用玻璃仪器为玻璃棒、烧杯、量筒、
,并配制溶液,所用玻璃仪器为玻璃棒、烧杯、量筒、________ 。
(3)用 溶液处理含
溶液处理含 废水反应的离子方程式为
废水反应的离子方程式为_____________ 。
(4)气体1转化为气体2时空气不能过量的原因是__________________ 。
(5)捕获剂捕获的气体主要是_________ (填化学式)。
(6)流程中生成的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: ;
; 可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别
可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别 和
和 。需选用的物质是_____。
。需选用的物质是_____。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
 废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
已知:
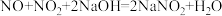

(1)固体1的主要成分有
 、
、(2)若实验室需要配制
 溶液
溶液 进行模拟测试,需称取
进行模拟测试,需称取 固体质量为
固体质量为 ,并配制溶液,所用玻璃仪器为玻璃棒、烧杯、量筒、
,并配制溶液,所用玻璃仪器为玻璃棒、烧杯、量筒、(3)用
 溶液处理含
溶液处理含 废水反应的离子方程式为
废水反应的离子方程式为(4)气体1转化为气体2时空气不能过量的原因是
(5)捕获剂捕获的气体主要是
(6)流程中生成的
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: ;
; 可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别
可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别 和
和 。需选用的物质是_____。
。需选用的物质是_____。①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
| A.①③⑤ | B.①②④ | C.①②⑤ | D.①②③⑤ |
您最近一年使用:0次
8 . “环境就是民生,青山就是美丽、蓝天也是幸福”。回答下列问题:
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是___________ 。
②某团队设计处理流程如下:
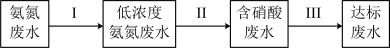
过程Ⅱ为硝化过程,在微生物的作用下实现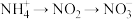 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为___________ ;
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现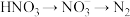 的转化,反应的化学方程式为
的转化,反应的化学方程式为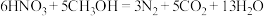 ,氧化产物是
,氧化产物是___________ ,当有1mol硝酸完全转化时,转移的电子数目为___________ 。
(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________ 。也可用NaClO2在酸性条件下氧化处理SO2,反应的离子方程式是___________ 。
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
引起雨水pH变化的主要原因是___________ (用化学方程式表示)。
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为___________ 。
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是②某团队设计处理流程如下:

过程Ⅱ为硝化过程,在微生物的作用下实现
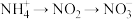 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现
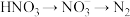 的转化,反应的化学方程式为
的转化,反应的化学方程式为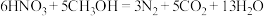 ,氧化产物是
,氧化产物是(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
| 时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为
您最近一年使用:0次



