1 . 下列说法正确的是
| A.1 mol N2分子中的π键与1 mol CO2分子中的π键的数目之比为2∶1 |
| B.键能:甲烷(C-C)<乙烯(C=C) |
| C.强度:氢键>化学键>范德华力 |
D.沸点: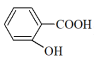 > >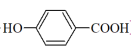 |
您最近半年使用:0次
2 . 下列有关化学用语正确的是
| A.HF的电子式:H:F |
B.铍原子最外层电子的原子轨道电子云图: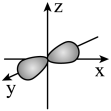 |
C.p—pπ键电子云模型: |
D.氧原子核外电子轨道表示式: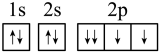 |
您最近半年使用:0次
名校
解题方法
3 . 某稀溶液中含有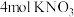 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是
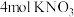 和
和 ,向其中加入
,向其中加入 ,充分反应(已知
,充分反应(已知 被还原为NO),最终溶液体积为
被还原为NO),最终溶液体积为 ,下列说法正确的是
,下列说法正确的是A.所得溶液中的溶质只有 、 、 |
B.所得溶液中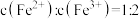 |
C.反应后生成NO的体积为 (标准状况下) (标准状况下) |
D.所得溶液中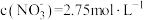 |
您最近半年使用:0次
名校
4 . 用 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是
 表示阿伏伽德罗常数的值,下列说法正确的是
表示阿伏伽德罗常数的值,下列说法正确的是A.现有乙烯、丙烯的混合气体共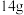 ,其原子数为 ,其原子数为 |
B.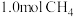 与 与 在光照下反应生成的 在光照下反应生成的 分子数为 分子数为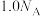 |
C.足量的铜与 浓硝酸充分反应,转移的电子数目为 浓硝酸充分反应,转移的电子数目为 |
D.常温常压下, 46%的乙醇溶液中,含H—O键的数目为 46%的乙醇溶液中,含H—O键的数目为 |
您最近半年使用:0次
名校
解题方法
5 . 二氧化硫是最常见、最简单、有刺激性的硫氧化物,大气主要污染物之一,火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。SO2在生活、生产中有重要用途,使用不当会造成环境污染。
(1)某同学利用如图所示装置研究二氧化硫的性质。___________ ,加入药品前需要___________ 。
②实验开始前先通入一段时间N2,此操作的目的是___________ 。
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有___________ 性。
④装置c中的溶液___________ (填能或不能)用澄清石灰水替换,理由是___________ 。
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。___________ 。该空气中二氧化硫的体积分数为___________ 。
(1)某同学利用如图所示装置研究二氧化硫的性质。

②实验开始前先通入一段时间N2,此操作的目的是
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有
④装置c中的溶液
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。

您最近半年使用:0次
名校
6 . 氮及其化合物与生产生活及环境息息相关。请回答下列问题:
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:___________ 。
(2)硝酸与金属反应会产生氮氧化物。下列环境问题与氮的氧化物排放无关的是___________ 。
A酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式___________ ,氧化产物与还原产物的物质的量之比为___________ 。
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸(HSbF6),称为超强酸。氟锑酸可由SbF5与HF混合得到。制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是___________ (用化学方程式回答)
(1)N2在常温下性质很稳定,任意写出一种与此性质有关的用途:
(2)硝酸与金属反应会产生氮氧化物。下列环境问题与氮的氧化物排放无关的是
A酸雨 B.光化学烟雾 C.臭氧层空洞 D.白色污染 E.温室效应
(3)汽车尾气中存在NO和CO,通过在排气管处加装催化剂,可以使其转化为对环境友好的物质,请写出发生反应的化学方程式
(4)氮的同族元素锑(Sb)可形成酸性超过100%硫酸的酸——氟锑酸(HSbF6),称为超强酸。氟锑酸可由SbF5与HF混合得到。制备氟锑酸一般在塑料容器中进行,不在玻璃仪器中进行的原因是
您最近半年使用:0次
7 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.2 mol/LAlCl3溶液中Cl-物质的量为0.6 mol |
| B.25℃ 101KPa,22.4L NH3中电子的数目为10NA |
| C.标准状况下,44.8LNO和22.4LO2反应后的分子数小于2NA |
| D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
您最近半年使用:0次
名校
解题方法
8 . 室温下,下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明的溶液中: 、 、 、 、 、 、 |
B.使石蕊变红的溶液中: 、 、 、S2-、 、S2-、 |
C.强碱性溶液中: 、 、 、 、 、 、 |
D.有SO 存在的溶液中:Na+、Mg2+、Ca2+、Br- 存在的溶液中:Na+、Mg2+、Ca2+、Br- |
您最近半年使用:0次
名校
解题方法
9 . 正确掌握化学用语是学好化学的基础,下列化学用语表达正确的是
A.NH3分子的电子式: |
B.中子数为10的氧原子形成的过氧根离子: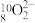 |
C.小苏打在水中的电离方程式: |
D.用电子式表示K2S的形成过程: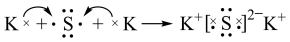 |
您最近半年使用:0次
名校
10 . 氰化氢(HCN,一元弱酸,易挥发)主要应用于电镀、采矿、药物合成等工业生产。HCN,CN-能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,___________ 。
(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是___________ 。
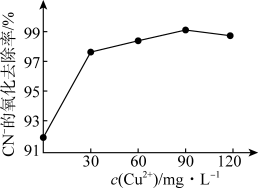
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是___________ 。 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g) NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0
除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是___________ 。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是
 ,其反应的离子方程式为
,其反应的离子方程式为(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g)
 NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近半年使用:0次



