名校
解题方法
1 . 某化学兴趣小组设计如图实验装置(夹持装置已省略),探究 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是__________ 。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。
①装置A中制备 的离子方程式为
的离子方程式为__________ 。
②证明 的氧化性大于
的氧化性大于 的现象是
的现象是__________ 。
③装置C的作用是__________ ,装置D中所盛试剂为__________ (填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。
① 发生反应的化学方程式为
发生反应的化学方程式为__________ 。
②实验完成后,打开弹簧夹,持续通入 的目的是
的目的是__________ 。
(4)淀粉 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(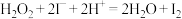 ,
, )。
)。
①滴定终点现象是__________ 。
②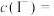
__________  。
。
 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞
 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。①装置A中制备
 的离子方程式为
的离子方程式为②证明
 的氧化性大于
的氧化性大于 的现象是
的现象是③装置C的作用是
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞
 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。①
 发生反应的化学方程式为
发生反应的化学方程式为②实验完成后,打开弹簧夹,持续通入
 的目的是
的目的是(4)淀粉
 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(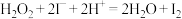 ,
, )。
)。①滴定终点现象是
②
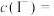
 。
。
您最近半年使用:0次
2 . 铅与碳是同族元素,有 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是
 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是A. 可写成 可写成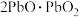 的形式 的形式 |
B.反应②中 是氧化产物 是氧化产物 |
C.生成相同质量的 ,反应①②转移电子数之比为 ,反应①②转移电子数之比为 |
D.根据反应可推测在题给条件下氧化性: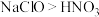 |
您最近半年使用:0次
名校
解题方法
3 . 下列设计的实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 探究化学反应的限度 | 取5mL0.1 mol·L-1 KI溶液,滴加0.1 mol·L-1 FeCl3溶液5~6滴,充分反应后,再滴加淀粉溶液 |
| B | 比较Mg与Al的金属性强弱 | 常温下,将Mg、Al与NaOH溶液组成原电池 |
| C | 比较Cl2、Br2、I2的氧化性强弱 | 向NaBr溶液中滴加少量氯水,充分反应后,再加入淀粉KI溶液 |
| D | 检验某溶液中是否含有K+ | 用洁净的铂丝蘸取待测液,在酒精灯火焰上灼烧 直接观察火焰的颜色 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
4 . 下列有关说法或各组性质的比较中,正确的有几项
①通过反应 ,可以证明非金属性的强弱:
,可以证明非金属性的强弱:
 在熔融状态下不仅破坏了离子键,还破坏了共价键
在熔融状态下不仅破坏了离子键,还破坏了共价键
④沸点: ⑤离子还原性:
⑤离子还原性: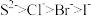
⑥酸性: ⑦金属性:
⑦金属性: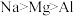
⑧气态氢化物稳定性:
①通过反应
 ,可以证明非金属性的强弱:
,可以证明非金属性的强弱:
② 的电子式可表示为
的电子式可表示为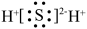
 在熔融状态下不仅破坏了离子键,还破坏了共价键
在熔融状态下不仅破坏了离子键,还破坏了共价键④沸点:
 ⑤离子还原性:
⑤离子还原性: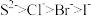
⑥酸性:
 ⑦金属性:
⑦金属性: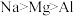
⑧气态氢化物稳定性:

| A.2 | B.3 | C.4 | D.5 |
您最近半年使用:0次
解题方法
5 . 根据下列实验操作和现象所得到的结论正确 的是
选项 | 实验操作和现象 | 实验结论 |
A | 向盛有FeSO4溶液的试管中滴加几滴KSCN溶液,振荡,再滴加几滴新制的氯水,观察到溶液变血红色 | Fe2+具有还原性 |
B | 向装有溶液X的试管中滴入稀的NaOH溶液,在试管口放湿润的红色石蕊试纸,试纸未变蓝色 | 溶液X中一定不存在 |
C | 淀粉-KI溶液中通入Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去 | 还原性:SO2<I-<Cl- |
D | 在淀粉溶液中加入稀硫酸,充分加热冷却后,再加入碘水,溶液变蓝 | 淀粉未发生水解 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
6 . 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,
①浓盐酸与 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为______ ;
②电极反应式:
ⅰ.还原反应:
ⅱ.氧化反应:____________ 。
③根据电极反应式,分析A中仍存在盐酸和 的原因。
的原因。
ⅰ.随 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,____________ 。
④补充实验证实了③中的分析。
a是______ ,b是______ 。
(2)利用 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。
相同浓度的KCl、KBr和KI溶液,能与 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是____________ ,从原子结构角度说明理由____________ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是____________ 。
(4)总结:物质氧化性和还原性变化的一般规律是____________ 。
(1)浓盐酸与
 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,①浓盐酸与
 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为②电极反应式:
ⅰ.还原反应:

ⅱ.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和
 的原因。
的原因。ⅰ.随
 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。ⅱ.随
 降低,
降低,④补充实验证实了③中的分析。
序号 | 实验 | 加入试剂 | 现象 |
Ⅰ |
| 较浓硫酸 | 有氯气 |
Ⅱ | a | 有氯气 | |
III | a和b | 无氯气 |
(2)利用
 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与
 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将
 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是(4)总结:物质氧化性和还原性变化的一般规律是
您最近半年使用:0次
7 . 已知有如下反应:①ClO +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
 +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是| A.I->Cl->Fe2+>Cl2 | B.Fe2+>I->Cl->Cl2 |
| C.I->Fe2+>Cl->Cl2 | D.I->Cl->Fe2+>Cl2 |
您最近半年使用:0次
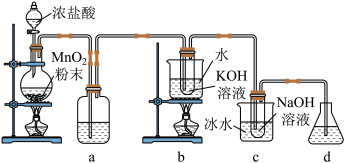
8 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)d中可选用试剂___________(填字母)。
(3)浓盐酸与二氧化锰反应的离子方程式是___________ 。
(4)b中采用的加热方式是___________ ,化学反应的离子方程式是___________ 。
(5)c中采用冰水浴冷却的目的是___________ 。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ (填“大于”或“小于”)NaClO。
(1)盛放浓盐酸的仪器名称是
(2)d中可选用试剂___________(填字母)。
| A.Na2S | B.NaCl | C.Ca(OH)2 | D.H2SO4 |
(3)浓盐酸与二氧化锰反应的离子方程式是
(4)b中采用的加热方式是
(5)c中采用冰水浴冷却的目的是
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近半年使用:0次
9 . 已知反应:
①
②
③
请根据上述反应判断氧化性由强到弱的顺序是
①

②

③

请根据上述反应判断氧化性由强到弱的顺序是
A.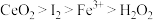 | B. |
C.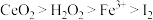 | D.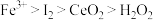 |
您最近半年使用:0次
名校
解题方法
10 . 下列实验操作和现象能得出相应结论或达到相应目的的是
| 选项 | 实验操作、现象 | 结论或目的 |
| A | 向某样品溶液中加入NaOH溶液并微热,产生能使湿润的蓝色石蕊试纸变红的气体 | 该样品中一定含 |
| B | 向某样品溶液中加入 溶液,生成白色沉淀,再加入硝酸,沉淀不溶解 溶液,生成白色沉淀,再加入硝酸,沉淀不溶解 | 该样品中一定含 |
| C | 向硫酸酸化的 溶液中滴入 溶液中滴入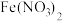 ,溶液变黄 ,溶液变黄 | 比较氧化性: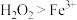 |
| D | 向 溶液中通入少量的氯气,出现淡黄色浑浊 溶液中通入少量的氯气,出现淡黄色浑浊 | 氯气的氧化性大于硫 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次




