名校
1 . 一节1号干电池可以让1平方米土地上的庄稼颗粒无收,回收电池既可以防止污染又可以变废为宝。废旧锌锰干电池内部的黑色物质A主要含有 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:________ (填化学式)。
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是________ 。灼烧时,MnOOH与空气中的氧气反应的化学方程式为________________ 。
(3)第III步中为提高反应速率,可以采取的措施有________ (任写一条)。
(4)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为________________ ;
②操作VI中需要的玻璃仪器有________ ;
③你认为操作VII中检测的方法及现象是________ 时可继续进行操作VIII;
④操作VIII中用无水乙醇洗涤的目的是________ 。
 、
、 、
、 、
、 、碳单质、少量有机物(有机物易燃烧生成
、碳单质、少量有机物(有机物易燃烧生成 和
和 ),用黑色物质A制备高纯
),用黑色物质A制备高纯 的流程如图:
的流程如图:
(2)第I步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)第III步中为提高反应速率,可以采取的措施有
(4)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第IV步中的多步操作可按如图步骤进行:
沉淀。第IV步中的多步操作可按如图步骤进行: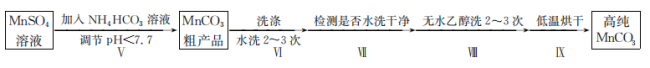
 溶液调节溶液pH的过程中有
溶液调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为②操作VI中需要的玻璃仪器有
③你认为操作VII中检测的方法及现象是
④操作VIII中用无水乙醇洗涤的目的是
您最近一年使用:0次
解题方法
2 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;②H2O2(在水中一部分可以电离出阴、阳离子);③ClO2;④O3;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于电解质的是___________ (填序号),“84”消毒液中有效成分的电离方程式为___________ ,双氧水的电子式为___________ 。
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO___________ H2O2(填“>”或“<”),若1 mol NaClO参加反应,转移电子数___________ (阿伏加德罗常数为NA)。
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)___________ 。
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是___________ (填标号)。
a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
(1)上述杀菌消毒剂属于电解质的是
(2)各类杀菌消毒剂使用时,必须严格按照使用说明。
①巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。该反应说明氧化性:NaClO
②若混合使用“洁厕灵”(主要成分为盐酸)与“84”消毒液会产生氯气。原因是(用离子方程式表示)
(3)ClO2在杀菌消毒过程中会产生亚氯酸盐(ClO
 ),需将其转化为Cl− 除去,下列试剂可将ClO
),需将其转化为Cl− 除去,下列试剂可将ClO 转化为Cl− 的是
转化为Cl− 的是a.FeSO4 b.O3 c.KMnO4 d.Na2CO3
您最近一年使用:0次
3 . 某主族元素的离子 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
 的最外层电子排布式为
的最外层电子排布式为 ,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是
,当把X的最高价氧化物溶于浓盐酸时,有黄绿色气体产生,则下列说法不正确的是A. 具有强氧化性 具有强氧化性 | B.X的最高价氧化物具有强氧化性 |
| C.该元素是第IVA族元素 | D.X的常见化合价有 、 、 |
您最近一年使用:0次
名校
解题方法
4 . 下列反应的离子方程式书写正确的是
A.碘化亚铁溶液中通入足量的氯气: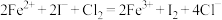 |
B.加碘盐与药物碘化钾片尽量不要同时服用: |
C.向 溶液中加入过量的NaOH溶液: 溶液中加入过量的NaOH溶液: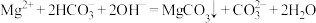 |
D.向 溶液中滴入 溶液中滴入 使 使 反应完全: 反应完全: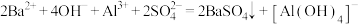 |
您最近一年使用:0次
2024-04-27更新
|
1117次组卷
|
4卷引用:湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题
湖南省“一起考”大联考2023-2024学年高三下学期3月模拟考试(模拟一)化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 (已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届江西省吉安市第一中学高三下学期一模化学试题
名校
5 . 利用含钴废料(主要成分为Co3O4,还含有少量SiO2、Fe2O3、Al2O3等杂质)制备LiCoO2的工艺如下。
回答下列问题:
(1)“酸浸”时_______ (填“可”或“不可”)用SO2代替H2O2。
(2)写出沉钴的离子反应方程式:_______ 。
(3)“调pH”的范围为4.5~7.8,滤液中残留的
_______ 。
(4)“高温焙烧"时的化学方程式:_______ 。

| 金属离子 | Fe2+ | Fe3+ | Al3+ | Co2+ |
| 开始沉淀的pH | 8.5 | 2.2 | 3.4 | 7.8 |
| 完全沉淀[c(金属离子)≤1×10-5mol/L]的pH | 10.0 | 3.0 | 4.5 | 9.4 |
(1)“酸浸”时
(2)写出沉钴的离子反应方程式:
(3)“调pH”的范围为4.5~7.8,滤液中残留的

(4)“高温焙烧"时的化学方程式:
您最近一年使用:0次
名校
6 . 某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,
①浓盐酸与 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为______ ;
②电极反应式:
ⅰ.还原反应:
ⅱ.氧化反应:____________ 。
③根据电极反应式,分析A中仍存在盐酸和 的原因。
的原因。
ⅰ.随 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。
ⅱ.随 降低,
降低,____________ 。
④补充实验证实了③中的分析。
a是______ ,b是______ 。
(2)利用 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。
相同浓度的KCl、KBr和KI溶液,能与 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是____________ ,从原子结构角度说明理由____________ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是____________ 。
(4)总结:物质氧化性和还原性变化的一般规律是____________ 。
(1)浓盐酸与
 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和 ,
,①浓盐酸与
 混合加热生成氯气的离子方程式为
混合加热生成氯气的离子方程式为②电极反应式:
ⅰ.还原反应:

ⅱ.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和
 的原因。
的原因。ⅰ.随
 降低或
降低或 升高,
升高, 氧化性减弱。
氧化性减弱。ⅱ.随
 降低,
降低,④补充实验证实了③中的分析。
序号 | 实验 | 加入试剂 | 现象 |
Ⅰ |
| 较浓硫酸 | 有氯气 |
Ⅱ | a | 有氯气 | |
III | a和b | 无氯气 |
(2)利用
 对
对 氧化性的影响,探究卤素离子的还原性。
氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与
 反应所需的最低
反应所需的最低 由大到小的顺序是
由大到小的顺序是(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将
 氧化为
氧化为 。经实验证实了推测。该化合物是
。经实验证实了推测。该化合物是(4)总结:物质氧化性和还原性变化的一般规律是
您最近一年使用:0次
名校
解题方法
7 . 氮化硅( )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示,下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示,下列说法正确的是 在潮湿的空气中易水解,产生白雾,
在潮湿的空气中易水解,产生白雾, 中各元素的化合价与
中各元素的化合价与 相同。
相同。
 )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示,下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示,下列说法正确的是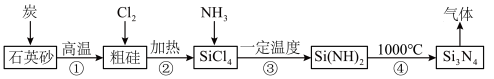
 在潮湿的空气中易水解,产生白雾,
在潮湿的空气中易水解,产生白雾, 中各元素的化合价与
中各元素的化合价与 相同。
相同。A.该流程中可循环使用的物质是 |
| B.第①步反应中产生的气体能使澄清石灰水变浑浊 |
| C.图示①~④的变化中,属于氧化还原反应的是①②③ |
D.第③步反应可用氨水代替 |
您最近一年使用:0次
名校
解题方法
8 .  可用作脱硝剂。某科研小组为了探究
可用作脱硝剂。某科研小组为了探究 能否被
能否被 还原,设计的装置如图所示(夹持、加热装置已略去,
还原,设计的装置如图所示(夹持、加热装置已略去, 、
、 为止水夹),下列说法不正确的是
为止水夹),下列说法不正确的是
 可用作脱硝剂。某科研小组为了探究
可用作脱硝剂。某科研小组为了探究 能否被
能否被 还原,设计的装置如图所示(夹持、加热装置已略去,
还原,设计的装置如图所示(夹持、加热装置已略去, 、
、 为止水夹),下列说法不正确的是
为止水夹),下列说法不正确的是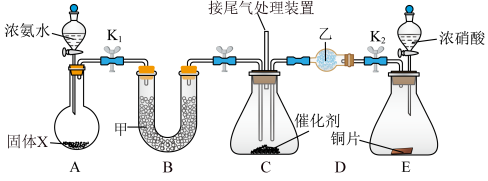
| A.固体X可以是碱石灰 |
| B.甲、乙试剂均可以是无水氯化钙 |
C.实验时宜先通入 ,再通入 ,再通入 有利于减少空气对实验的干扰 有利于减少空气对实验的干扰 |
| D.装置C的反应中n(还原剂)∶n(氧化剂)=4∶3 |
您最近一年使用:0次
2024-04-27更新
|
110次组卷
|
2卷引用:山东省淄博市高青县第一中学2023-2024学年高一下学期期中考试化学试题
9 . 已知有如下反应:①ClO +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
 +5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是
+5Cl-+6H+=3Cl2+3H2O,②2FeCl3+2KI=2FeCl2+2KCl+I2,③2FeCl2+Cl2=2FeCl3.下列各微粒还原能力由强到弱的顺序正确的是| A.I->Cl->Fe2+>Cl2 | B.Fe2+>I->Cl->Cl2 |
| C.I->Fe2+>Cl->Cl2 | D.I->Cl->Fe2+>Cl2 |
您最近一年使用:0次
10 . 为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生的反应为2NO+2CO=N2+2CO2。碳元素的化合价___________ (填“升高”或“降低”),被___________ (填“氧化”或“还原”),CO是___________ 剂(填“氧化”或“还原”),NO是___________ 剂(填“氧化”或“还原”),发生___________ 反应。(填“氧化”或“还原”)
您最近一年使用:0次




