名校
1 . 由下列实验步骤得到的实验现象、结论或解释均正确的是
| 选项 | 实验步骤 | 实验现象 | 结论或解释 |
| A | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | 溶液紫色褪去 |  具有还原性 具有还原性 |
| B | 分别向置于不同温度下的 氢硫酸和 氢硫酸和 氢硫酸中通入等量氯气 氢硫酸中通入等量氯气 |  氢硫酸先出现浑浊 氢硫酸先出现浑浊 | 增大浓度可加快反应速率 |
| C | 向 溶液中同时通入 溶液中同时通入 和 和 | 出现白色沉淀 | 白色沉淀为 |
| D | 向 溶液中逐滴加入氨水至过量 溶液中逐滴加入氨水至过量 | 产生蓝色沉淀 |  难溶于水 难溶于水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元素可形成化合物甲,其结构式如图所示,1mol甲含58mol电子,并且含有1mol配位键。下列说法正确的是
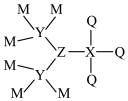
| A.Q是五种元素中原子半径最大的 |
B.水中溶解性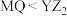 |
| C.Q、Y、Z三种元素的最简单氢化物具有相同的电子数 |
D.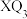 中所有原子均达到 中所有原子均达到 稳定结构 稳定结构 |
您最近一年使用:0次
昨日更新
|
114次组卷
|
3卷引用:2024届甘肃省高三下学期二模化学试题
3 . 下列各组离子在对应的溶液中能大量共存的是
A.0.1mol·L-1 K3[Fe(CN)6]溶液中: 、 、 、 、 、 、 |
B.0.1mol·L-1 HNO3溶液中: 、 、 、 、 、 、 |
C.0.1mol·L-1氨水中: 、 、 、 、 、 、 |
D.0.1mol·L-1 Ba(OH)2溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
4 . 若X、Y两种粒子之间可形成配位键,则下列说法正确的是
| A.X、Y只能是分子 |
| B.X、Y只能是离子 |
| C.若X提供空轨道,则Y至少要提供一对孤电子对 |
| D.一定是X提供空轨道,Y提供孤电子对 |
您最近一年使用:0次
名校
5 . 某种以辉铜矿[ ,含
,含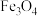 、
、 杂质]为原料制备
杂质]为原料制备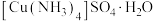 的流程如图所示,下列说法错误的是
的流程如图所示,下列说法错误的是
 ,含
,含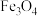 、
、 杂质]为原料制备
杂质]为原料制备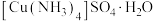 的流程如图所示,下列说法错误的是
的流程如图所示,下列说法错误的是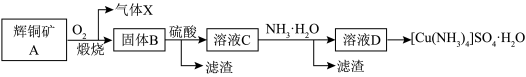
| A.向溶液D中加入无水乙醇并用玻璃棒摩擦试管壁可析出目标产物 |
| B.向溶液C中加入硫氰化钾溶液后呈现红色 |
C.煅烧过程中涉及到的主要方程式为 |
D.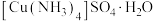 中配位原子为N 中配位原子为N |
您最近一年使用:0次
名校
6 . 下列由实验操作和现象得出结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向2mL 0.1  溶液中加入6mL 0.1 溶液中加入6mL 0.1  NaOH溶液。出现白色沉淀后,继续滴入几滴浓 NaOH溶液。出现白色沉淀后,继续滴入几滴浓 溶液,静置 溶液,静置 | 出现红褐色沉淀 | 同温下,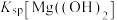 > >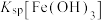 |
| B | 向某溶液中先滴加氯水,后滴加KSCN溶液 | 溶液显红色 | 原溶液中有 ,无 ,无 |
| C | 分别向等物质的量浓度、等体积的KCl和KI的溶液中滴加2滴稀的 溶液,充分振荡后 溶液,充分振荡后 | KCl溶液中无白色沉淀,KI溶液中有黄色沉淀 |  结合微粒的能力: 结合微粒的能力: |
| D | 向淀粉溶液中滴入稀硫酸,加热一段时间,冷却后加入氢氧化钠溶液至溶液呈碱性,再滴加碘水 | 溶液未变蓝色 | 证明淀粉水解完全 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 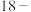 冠
冠 的结构如图所示,其空腔直径为
的结构如图所示,其空腔直径为 。已知部分粒子直径如下表,该冠醚能识别的粒子是
。已知部分粒子直径如下表,该冠醚能识别的粒子是
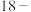 冠
冠 的结构如图所示,其空腔直径为
的结构如图所示,其空腔直径为 。已知部分粒子直径如下表,该冠醚能识别的粒子是
。已知部分粒子直径如下表,该冠醚能识别的粒子是
| 粒子 |  |  |  |  |
| 直径/pm | 152 | 204 | 276 | 334 |
A. | B. | C. | D. |
您最近一年使用:0次
8 . 某含氰废水中氰主要以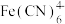 和少量
和少量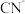 形式存在,对该废水进行除氰处理的步骤如下。
形式存在,对该废水进行除氰处理的步骤如下。
Ⅰ.取一定量处理好的铁屑和活性炭混合物(按照一定的体积比混合);
Ⅱ.加入一定体积的含氰废水,调节 值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液
值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液 ,总氰去除率接近
,总氰去除率接近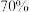 ;
;
Ⅲ.调节滤液 的
的 ,加入一定量的
,加入一定量的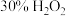 溶液,反应一段时间后过滤,得滤液
溶液,反应一段时间后过滤,得滤液 ,总氰去除率可达
,总氰去除率可达 以上;
以上;
Ⅳ.向滤液 中加入
中加入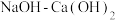 调节
调节 至
至 ,混凝沉淀,经过滤,总氰去除率接近
,混凝沉淀,经过滤,总氰去除率接近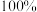 ,得到符合排放标准的废水。
,得到符合排放标准的废水。
(1)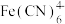 的中心离子是
的中心离子是_______ 。
(2)Ⅰ中,处理过程需用稀硫酸除去铁屑表面的氧化铁,反应的离子方程式是_______ 。
(3)步骤Ⅱ中,生成沉淀的主要成分是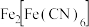 。
。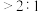 时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是:
时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是: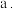 活性炭的吸附性减弱;
活性炭的吸附性减弱;
_______ 。
②反应过程中,会有部分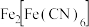 转化为
转化为 ,补全反应的离子方程式
,补全反应的离子方程式_______ 。
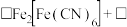 _______
_______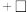 _______
_______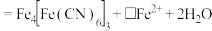
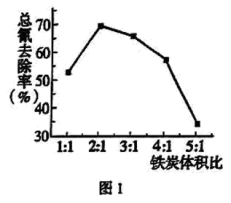
(4)步骤Ⅲ中,其他条件不变,研究 不同对滤液
不同对滤液 中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液
中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液 的
的 为4左右。
为4左右。 可将
可将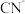 氧化为
氧化为 和
和 ,反应的离子方程式是
,反应的离子方程式是_______ 。
②当 时,随
时,随 增大,总氰去除率下降,可能的原因是
增大,总氰去除率下降,可能的原因是_______ 。
(5)在步骤Ⅳ中产生了胶体,使水中的氰经聚沉而除去。证明有胶体产生的方法是_______ 。
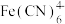 和少量
和少量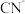 形式存在,对该废水进行除氰处理的步骤如下。
形式存在,对该废水进行除氰处理的步骤如下。Ⅰ.取一定量处理好的铁屑和活性炭混合物(按照一定的体积比混合);
Ⅱ.加入一定体积的含氰废水,调节
 值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液
值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液 ,总氰去除率接近
,总氰去除率接近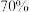 ;
;Ⅲ.调节滤液
 的
的 ,加入一定量的
,加入一定量的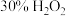 溶液,反应一段时间后过滤,得滤液
溶液,反应一段时间后过滤,得滤液 ,总氰去除率可达
,总氰去除率可达 以上;
以上;Ⅳ.向滤液
 中加入
中加入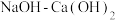 调节
调节 至
至 ,混凝沉淀,经过滤,总氰去除率接近
,混凝沉淀,经过滤,总氰去除率接近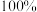 ,得到符合排放标准的废水。
,得到符合排放标准的废水。(1)
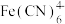 的中心离子是
的中心离子是(2)Ⅰ中,处理过程需用稀硫酸除去铁屑表面的氧化铁,反应的离子方程式是
(3)步骤Ⅱ中,生成沉淀的主要成分是
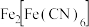 。
。
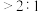 时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是:
时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是: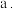 活性炭的吸附性减弱;
活性炭的吸附性减弱;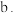
②反应过程中,会有部分
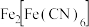 转化为
转化为 ,补全反应的离子方程式
,补全反应的离子方程式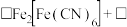 _______
_______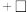 _______
_______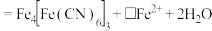
(4)步骤Ⅲ中,其他条件不变,研究
 不同对滤液
不同对滤液 中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液
中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液 的
的 为4左右。
为4左右。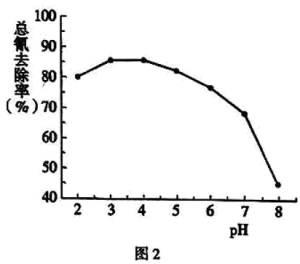
 可将
可将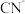 氧化为
氧化为 和
和 ,反应的离子方程式是
,反应的离子方程式是②当
 时,随
时,随 增大,总氰去除率下降,可能的原因是
增大,总氰去除率下降,可能的原因是(5)在步骤Ⅳ中产生了胶体,使水中的氰经聚沉而除去。证明有胶体产生的方法是
您最近一年使用:0次
解题方法
9 . 请按要求完成填空:
(1)完成下表中的空白:
(2)配合物[Cu(NH3)4]SO4的中心离子是___________ 、配体是___________ 、配位原子是___________ 、配位数是___________ 。
(1)完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | VSEPR模型 | 空间结构 |
| CO2 | ① | ② | ③ | ④ |
SO | ⑤ | ⑥ | ⑦ | ⑧ |
您最近一年使用:0次
名校
10 . 下列实验操作、现象与结论均正确的是
| 选项 | 实验操作、现象 | 结论 |
| A | 向 溶液中加入氨水至蓝色沉淀溶解,得到深蓝色透明溶液,再加入乙醇,析出深蓝色晶体 溶液中加入氨水至蓝色沉淀溶解,得到深蓝色透明溶液,再加入乙醇,析出深蓝色晶体 | 乙醇可降低 的溶解度 的溶解度 |
| B | 向 溶液中滴加 溶液中滴加 溶液,出现淡黄色沉淀 溶液,出现淡黄色沉淀 |  与 与 发生了归中反应 发生了归中反应 |
| C | 向某溶液中滴入几滴氯水,再滴入KSCN溶液,观察到溶液变红 | 证明原溶液中含有 |
| D | 先向一支试管中加入1 mL 10%蔗糖溶液和5滴10% 溶液,加热煮沸,再加入新制的 溶液,加热煮沸,再加入新制的 ,加热,无砖红色沉淀产生 ,加热,无砖红色沉淀产生 | 蔗糖未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



