河北省石家庄市第二十四中学2020-2021学年高一上学期9月月考化学试题
河北
高一
阶段练习
2021-08-21
187次
整体难度:
较易
考查范围:
认识化学科学、化学反应原理、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
| A.根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物和两性氧化物等 |
| B.根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
| C.根据是否有丁达尔现象将分散系分为溶液、胶体和浊液 |
| D.根据组成元素的种类将纯净物分为单质和化合物 |
选项 | 混合物 | 纯净物 | 单质 | 电解质 |
A | 盐酸 | NaOH | 石墨 | K2SO4溶液 |
B | 空气 | Fe(OH)3胶体 | 铁 | Na2CO3 |
C | CuSO4·5H2O | CaCl2 | 水银 | 铜 |
D | 氨水 | KNO3晶体 | O3 | NaCl |
| A.A | B.B | C.C | D.D |


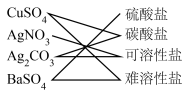
A. NaOH NaCl MgO NaOH NaCl MgO |
B. 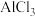  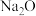 |
C.  CaO CaO  |
D.HBr KOH 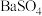 CuO CuO |
二、多选题 添加题型下试题
A.H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++ =BaSO4↓+H2O =BaSO4↓+H2O |
| B.将Fe投入到CuSO4溶液中:Fe+Cu2+=Fe2++Cu |
| C.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
D.大理石和盐酸: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
三、单选题 添加题型下试题
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
 +2H+=CO2↑+H2O表示的是
+2H+=CO2↑+H2O表示的是①Na2CO3+2HCl=2NaCl+CO2↑+H2O ②K2CO3+H2SO4=K2SO4+CO2↑+H2O
③CaCO3+2HCl=CaCl2+CO2↑+H2O ④2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O
| A.①② | B.①②③ | C.①③④ | D.②④ |
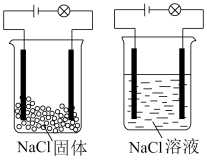
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出了可以自由移动的离子 |
| D.NaCl溶液中,水电离出大量的离子 |
A.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
D.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
A.NaNO3在通电的条件下电离出 和Na+ 和Na+ |
B.稀硝酸溶液中存在的微粒主要有H+、 和HNO3 和HNO3 |
C.Na2SO4溶于水后,主要以Na+和 形式存在 形式存在 |
| D.BaSO4难溶于水,不属于电解质 |
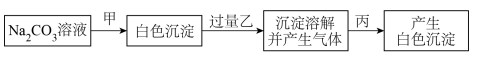
| A.BaCl2、H2SO4、MgCl2 | B.BaCl2、HCl、Na2SO4 |
| C.CaCl2、HNO3、NaCl | D.CaCl2、HNO3、BaCl2 |
【知识点】 离子反应的实际应用
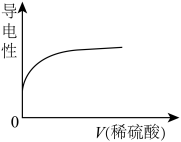
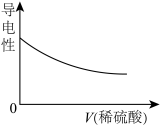
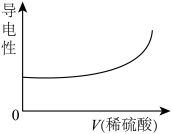
| A.氢氧化镁和稀盐酸反应 | B.Ba(OH)2溶液滴入稀硫酸中 |
| C.澄清石灰水和稀硝酸反应 | D.二氧化碳通入澄清石灰水中 |
【知识点】 离子反应的发生及书写
| A.在水溶液中和熔融状态下均不导电的化合物叫非电解质 |
| B.电解质、非电解质都指化合物而言,单质不属于此范畴 |
| C.电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D.纯水的导电性很差,但水也是电解质 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
 、
、 、OH-、Cl-,两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清的只含硝酸钠而排放,污染程度大大降低。关于污染源的分析,你认为正确的是
、OH-、Cl-,两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清的只含硝酸钠而排放,污染程度大大降低。关于污染源的分析,你认为正确的是A. 和 和 可能来自同一工厂 可能来自同一工厂 | B.Cl-和 一定在相同的工厂 一定在相同的工厂 |
| C.Ag+和Na+可能来自同一工厂 | D.Na+和 一定来自不同的工厂 一定来自不同的工厂 |
| A.BaCl2,K2CO3加稀HNO3 |
| B.Na2CO3,AgNO3加稀HNO3 |
| C.CuSO4,NaOH加稀H2SO4 |
| D.Ba(OH)2,CuCl2稀H2SO4 |
【知识点】 离子反应的发生及书写
| A.HClO | B.Cl2 | C.NH3 | D.NaHCO3 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.Na2FeO4中Fe元素是+6价 | B.还原产物是NaCl |
| C.FeCl3是还原剂 | D.NaClO被氧化 |
四、填空题 添加题型下试题
(1)写出下列物质在水溶液中的电离方程式:
NaHSO4
(2)现有以下物质:①NaCl溶液②干冰③液态HCl④铜⑤BaSO4固体⑥蔗糖⑦Na2O⑧NaOH固体⑨盐酸⑩NH3,其中能够导电的是
(1)硫酸氢钠与碳酸氢钠溶液混合
(2)氢氧化镁固体溶于足量稀盐酸
(3)硫酸钠和氯化钡溶液反应(离子方程式)
(4)稀盐酸与NaHCO3溶液反应(离子方程式)
(5)氧化铜和稀硫酸反应
(6)碳酸氢钠溶液和稀盐酸反应
(7)醋酸和氢氧化钠溶液反应
(8)氢氧化铁和稀盐酸反应:
(9)向澄清右灰水中通入少量二氧化碳:
(1)氧化剂
(2)氧化产物
(3)用单线桥的方法表示该反应的电子转移情况
(4)用双线桥的方法表示该反应的电子转移情况。
(5)当有8个NH3分子参加反时,转移的电子个数为
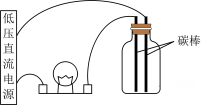
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③氯化钠溶液 ④氢氧化钠溶液
【知识点】 电解质、非电解质概念解读 物质水溶液的导电性解读
试卷分析
试卷题型(共 24题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 化学物质的分类方法 无机物质的分类 | |
| 2 | 0.94 | 无机物质的分类 分散系概念及其分类 非电解质、电解质物质类别判断 | |
| 3 | 0.94 | 化学物质的分类方法 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 4 | 0.94 | 交叉分类法 分类方法的应用 | |
| 5 | 0.94 | 交叉分类法 分类方法的应用 | |
| 7 | 0.85 | 限定条件下的离子共存 | |
| 8 | 0.85 | 离子方程式的书写 | |
| 9 | 0.65 | 电解质与非电解质 电解质、非电解质概念 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 10 | 0.65 | 限定条件下的离子共存 | |
| 11 | 0.85 | 电解质的电离 强电解质和弱电解质的判断 应用电离平衡分析生活中实例 | |
| 12 | 0.85 | 离子反应的实际应用 | |
| 13 | 0.85 | 离子反应的发生及书写 | |
| 14 | 0.85 | 电解质与非电解质 电解质的电离 物质水溶液的导电性 | |
| 15 | 0.85 | 物质水溶液的导电性 | |
| 16 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 17 | 0.65 | 离子共存 物质共存 离子反应在化合物组成的分析、鉴定的应用 离子的检验 | |
| 18 | 0.85 | 离子反应的发生及书写 | |
| 19 | 0.65 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 20 | 0.85 | 氧化还原反应的应用 氧化还原反应在生活、生产中的应用 高铁酸钠 | |
| 二、多选题 | |||
| 6 | 0.85 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 三、填空题 | |||
| 21 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 电离方程式 | |
| 22 | 0.65 | 离子反应的发生及书写 离子方程式的书写 碳酸氢钠 碳酸氢钠与酸反应 | |
| 23 | 0.65 | 氧化还原反应基本概念 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 | |
| 24 | 0.85 | 电解质、非电解质概念 物质水溶液的导电性 | |

 属于
属于