广东省东莞市翰林中学2019-2020学年高一上学期期中考试化学试题
广东
高一
期中
2020-11-10
285次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、常见无机物及其应用
一、单选题 添加题型下试题
| A.②③ |
| B.③⑦ |
| C.②⑥ |
| D.②⑥⑦ |
| A.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应 |
| B.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应 |
| C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应 |
| D.“丹砂(HgS)烧之成水银,积变又还成丹砂”描述的是升华和凝华过程 |
| A.稀盐酸 |
| B.乙醇 |
| C.明矾 |
| D.熔融的氯化钾 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读

下列说法中错误的是( )
| A.浸泡时加入乙醇有利于中草药有效成分的浸出 |
| B.高温条件下更有利于超临界CO2流体萃取 |
| C.升温、减压的目的是实现CO2与产品分离 |
| D.超临界CO2流体萃取中药材具有无溶剂残留、绿色环保等优点 |
| A.称量NaOH固体时,天平的托盘各放两张同样大小的纸片 |
| B.用l0mL量筒量取5.2mL盐酸 |
| C.用托盘天平称取25.20g碳酸钠 |
| D.做某实验需要用200mL0.10mol/LNaCl溶液,可以用100mL容量瓶配两次 |

| A.用图1所示装置从所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 |
| B.用图2所示装置从海水中得到粗盐 |
| C.用图3所示装置快速分离四氯化碳和水 |
| D.用图4所示装置分离乙醇与水的混合物 |
【知识点】 物质分离、提纯的常见物理方法
| A.容量瓶内有水,未经过干燥处理 |
| B.定容时,仰视刻度线 |
| C.用量筒量取浓盐酸时,用水洗涤量筒2~3次,洗涤液倒入容量瓶中 |
| D.定容后倒转容量瓶几次,发现液体最低点低于刻度线,再补加几滴水到刻度线 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
| A.青菜中含有多种维生素 |
| B.维生素具有还原性 |
| C.此致人中毒过程中砷发生还原反应 |
| D.此致人中毒过程中砒霜是氧化产物 |
【知识点】 氧化还原反应基本概念 氧化还原反应在生活、生产中的应用解读
| A.摩尔是七个基本物理量之一 |
| B.物质的摩尔质量等于1mol物质所具有的质量 |
| C.20℃、101kPa时,气体摩尔体积约为22.4L/mol |
| D.在温度、压强一定时,任何具有相同微粒数的气体都具有大致相同的体积 |
【知识点】 物质的量及单位——摩尔 摩尔质量 气体摩尔体积 阿伏加德罗定律
| A.通常状况下,1mol任何物质都约含NA个分子 |
| B.1mol/L的CaCl2溶液中含有的Cl−数目为2NA个 |
C.常温常压下,18g NH 中所含的质子数为10NA个 中所含的质子数为10NA个 |
| D.标准状况下,11.2L的CH4、C2H4中含有的氢原子数为2NA个 |
| A.XY3 | B.XY | C.X3Y | D.X2Y3 |
| A.质量相等、密度不等的N2和C2H4 |
| B.等体积、等密度的CO和N2 |
| C.等温、等体积的O2和Cl2 |
| D.等压、等体积的NH3和CO2 |
【知识点】 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | Na2CO3 | H2SO4 | Cu2(OH)2CO3 | Fe2O3 | SO3 |
| B | NaOH | CH3COOH | NaCl | Na2O | NO2 |
| C | KOH | NaHSO4 | CaF2 | MgO | SO2 |
| D | NH3·H2O | HNO3 | NaHCO3 | CuO | CO2 |
| A.A | B.B | C.C | D.D |
【知识点】 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系解读
| A.丁达尔效应是鉴别胶体和溶液的物理方法 |
| B.电泳实验说明某些胶体粒子带有电荷 |
| C.豆腐的制作与胶体的性质有关 |
| D.向氯化铁溶液中滴加氢氧化钠溶液可以制得氢氧化铁胶体 |
二、多选题 添加题型下试题

| A.XY段溶液的导电能力不断减弱,说明H2SO4不是电解质 |
| B.a时刻Ba(OH)2溶液与稀硫酸恰好完全中和 |
| C.Y处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 |
| D.YZ段溶液的导电能力不断增大,主要是由于Ba(OH)2电离出的离子导电 |
三、单选题 添加题型下试题
A.H+、Fe2+、 、 、 |
B.K+、Na+、 、 、 |
C.K+、 、 、 、 、 |
D.Na+、K+、 、OH− 、OH− |
【知识点】 限定条件下的离子共存解读
| A.氢氧化镁和稀盐酸反应 | B.Ba(OH)2溶液滴入稀硫酸中 |
| C.澄清石灰水和稀硝酸反应 | D.二氧化碳通入澄清石灰水中 |
【知识点】 离子反应的发生及书写
| A.向稀硫酸中投入铁粉:6H++Fe=2Fe3++3H2↑ |
| B.铜与AgNO3溶液反应:Cu+Ag+=Cu2++Ag |
| C.碳酸钙与醋酸溶液反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
D.往少量NaHSO4溶液中滴加Ba(OH)2溶液至不在产生沉淀:H++ +OH-+Ba2+=BaSO4↓+H2O +OH-+Ba2+=BaSO4↓+H2O |
【知识点】 离子方程式的正误判断解读
| A.某固体加入稀盐酸,固体溶解,产生无色气体,证明该固体一定是CaCO3 |
| B.某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性 |
C.某溶液中滴加BaCl2溶液和稀HNO3,生成白色沉淀,该溶液中一定含有 |
| D.检验溶液含有Cl-,加稀盐酸除去OH-,再加AgNO3溶液,生成白色沉淀,证明含有Cl- |
| 序号 | 物质 | 杂质 | 除杂应选用的试剂或操作方法 |
| ① | NaNO3溶液 | NaOH | 加入FeCl3溶液,并过滤 |
| ② | FeCl2溶液 | CuCl2 | 加入过量铁粉,并过滤 |
| ③ | H2 | CO2 | 通过盛NaOH溶液的洗气瓶,并干燥 |
| ④ | BaCO3粉末 | BaCl2 | 溶解、过滤、蒸发 |
| A.②③ |
| B.②③④ |
| C.①③④ |
| D.①②③④ |
【知识点】 物质的分离、提纯
| A.1LH2O中溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5mol•L﹣1 |
| B.从1L1mol•L﹣1蔗糖(C12H22O11)溶液中取出100mL溶液,其物质的量的浓度仍为1mol•L﹣1 |
| C.0.5mol•L﹣1的NaOH溶液中,含有0.5molNa+ |
| D.1L H2SO4溶液中含有98g H2SO4,则该溶液的物质的量浓度为98g•L﹣1 |
【知识点】 物质的量浓度
| A.0.1mol·L−1 |
| B.0.2mol·L−1 |
| C.0.3mol·L−1 |
| D.0.4mol·L−1 |
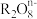 离子在一定条件下可将
离子在一定条件下可将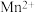 离子氧化成
离子氧化成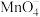 离子。若反应后
离子。若反应后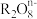 变成
变成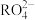 ,又知反应中氧化剂和还原剂的个数之比是5∶2,则n值为
,又知反应中氧化剂和还原剂的个数之比是5∶2,则n值为| A.1 | B.2 | C.3 | D.4 |
四、未知 添加题型下试题
五、单选题 添加题型下试题
| A.氧气是还原产物 |
| B.还原剂与氧化剂的物质的量之比为1:1 |
| C.反应物中有水,且反应方程式中水的化学计量数为2 |
| D.若生成4.48L(标准状况下)O2,则反应转移0.8mol电子 |
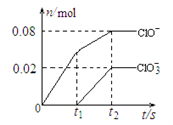
| A.苛性钾溶液中KOH的质量是5.6 g |
| B.反应中转移电子的物质的量是0.18mol |
| C.在酸性条件下 ClO- 和ClO3-可生成Cl2 |
| D.一定有3.136 L氯气参与反应 |
| A.0.1mol·L−1 |
| B.0.15mol·L−1 |
| C.0.2mol·L−1 |
| D.0.6mol·L−1 |
【知识点】 物质的量浓度的计算
| A.1:2:3 | B.3:2:1 | C.6:3:2 | D.1:1:1 |
【知识点】 物质的量浓度的计算 依据物质的量浓度公式的基础计算解读
A.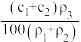 | B.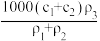 | C.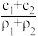 | D.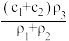 |
六、解答题 添加题型下试题
(1)该反应的氧化剂是
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,最后加入一定量的苯振荡,这时候,观察到的现象是
(3)若采用下图实验装置将苯和I2的混合溶液分离。
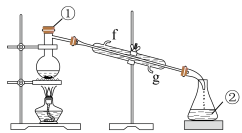
写出图中仪器的名称:①
(4)在容量瓶的使用方法中,下列操作正确的是
A.使用容量瓶前是否烘干
B.定容时,若加蒸馏水超过了刻度线,及时用胶头滴管吸出
C.配制溶液时,若药品是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,加水至刻度线1∼2cm处,用胶头滴管加蒸馏水至刻度线。
D.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(5)上面实验中用0.5mol/L的稀硫酸200mL,用浓硫酸配置稀硫酸时,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
(6)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解后马上转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视
D.用量筒量取浓硫酸时眼睛仰视
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
七、填空题 添加题型下试题
(1)现将少量Fe3O4粉末加入过量稀盐酸,发生反应的离子方程式
(2)取少量溶液于试管中,滴入NaOH溶液,观察到有红褐色沉淀生成,反应的离子方程式为
(3)取少量溶液于试管中,加入少量还原铁粉,振荡,铁粉逐渐溶解,溶液由黄色变为浅绿色,反应的离子方程式为
(4)取少量溶液与试管中,加入过量双氧水后,将所得的溶液蒸发后,请问是否能够得到FeCl3
晶体?
【知识点】 铁盐 Fe2+的鉴别及其应用解读 铁盐与亚铁盐鉴别试剂的选择解读
(1)请将上述反应改成离子方程式,并用单线桥法表示电子得失的方向和数目
(2)若生成448mL的NO(标准状况下),则该过程中转移的电子是
Ⅱ某反应体系有反应物和生成物共7种物质:C、H2SO4、K2CrO4、K2SO4、CO2、Cr2(SO4)3和H2O。已知该反应中发生如下过程:C→CO2。该反应的化学方程式:
试卷分析
试卷题型(共 33题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 实验安全 | |
| 2 | 0.85 | 交叉分类法 无机物质的分类 | |
| 3 | 0.85 | 胶体的性质和应用 四种基本反应类型 氧化还原反应基本概念 物质的分离、提纯 | |
| 4 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 5 | 0.65 | 常见无机物的制备 | |
| 6 | 0.85 | 一定物质的量浓度的溶液的配制 常用仪器及使用 化学实验基础操作 | |
| 7 | 0.94 | 物质分离、提纯的常见物理方法 | |
| 8 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 9 | 0.65 | 氧化还原反应基本概念 氧化还原反应在生活、生产中的应用 | |
| 10 | 0.65 | 物质的量及单位——摩尔 摩尔质量 气体摩尔体积 阿伏加德罗定律 | |
| 11 | 0.85 | 阿伏加德罗常数的求算 结合气体物质与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 12 | 0.85 | 阿伏加德罗定律 物质的量的含义 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 13 | 0.65 | 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 14 | 0.85 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 15 | 0.94 | 胶体的性质和应用 胶体的制备 | |
| 17 | 0.85 | 限定条件下的离子共存 | |
| 18 | 0.85 | 离子反应的发生及书写 | |
| 19 | 0.85 | 离子方程式的正误判断 | |
| 20 | 0.85 | 硫酸根离子的检验 离子的检验 常见阴离子的检验 | |
| 21 | 0.85 | 物质的分离、提纯 | |
| 22 | 0.4 | 物质的量浓度 | |
| 23 | 0.85 | 物质的量浓度的计算 物质的量浓度计算-溶液混合的有关计算 | |
| 24 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的规律 基于氧化还原反应守恒规律的计算 化学式与化合价 | |
| 26 | 0.4 | 氧化还原反应的几组概念 常见氧化剂与还原剂 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 27 | 0.4 | 氧化还原反应方程式的配平 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 28 | 0.65 | 物质的量浓度的计算 | |
| 29 | 0.85 | 物质的量浓度的计算 依据物质的量浓度公式的基础计算 | |
| 30 | 0.4 | 物质的量浓度的计算 物质的量浓度计算-溶液稀释的有关计算 物质的量浓度计算-溶液混合的有关计算 | |
| 二、多选题 | |||
| 16 | 0.65 | 电解质与非电解质 电解质的电离 物质水溶液的导电性 | |
| 三、未知 | |||
| 25 | 0.85 | 氧化性、还原性强弱的比较 氧化还原反应的应用 氧化还原反应的规律 | 未知 |
| 四、解答题 | |||
| 31 | 0.65 | 氧化还原反应有关计算 一定物质的量浓度的溶液的配制 物质的分离、提纯 常用仪器及使用 | 实验探究题 |
| 五、填空题 | |||
| 32 | 0.85 | 铁盐 Fe2+的鉴别及其应用 铁盐与亚铁盐鉴别试剂的选择 | |
| 33 | 0.65 | 单线桥、双线桥分析氧化还原反应 氧化还原反应有关计算 氧化还原反应的规律 | |



