1 . 实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。___________ ,则气密性良好。
(2)装置A中滴加硫酸的仪器名称为___________ 。
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有___________ (填“还原性”、“氧化性”或“漂白性”)。
(4)试管D中反应的离子方程式为___________ 。
(5)用下图所示装置验证H2SO3酸性比H2CO3强。
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
X为___________ ,Y为___________ ,Z为___________ 。
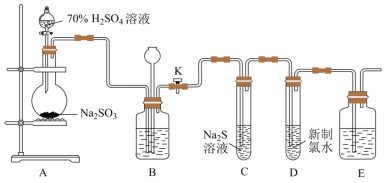
(2)装置A中滴加硫酸的仪器名称为
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)试管D中反应的离子方程式为
(5)用下图所示装置验证H2SO3酸性比H2CO3强。
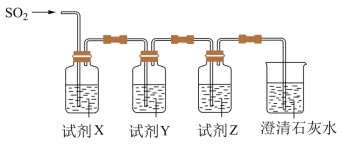
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3溶液 d.饱和NaHSO3溶液
X为
您最近半年使用:0次
名校
解题方法
2 . 化学是一门实验科学。下列实验操作错误的是
| A.滴定实验时,滴定管的尖嘴可以接触锥形瓶内壁 |
B.将碱式碳酸铜在坩埚中灼烧可得 |
C.给盛有 体积液体的试管加热 体积液体的试管加热 |
| D.用分液的方法分离乙醇和乙酸的混合物 |
您最近半年使用:0次
解题方法
3 . 某实验小组利用硫渣(主要成分为Sn,含少量CuS、Pb等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。
相关产物的熔沸点:
(1)仪器b的名称___________ ,为了使浓盐酸顺利滴入烧瓶中,可以将仪器a更换为___________ ,A中盛装试剂为二氧化锰时发生反应的化学方程式为___________ 。
(2)整套装置的连接顺序___________ 。(填写仪器下方字母)
(3)碱石灰的作用为___________ 。
(4)实验结束后,得到粗产品中常溶有少量SnCl2杂质,可用___________ 方法提纯。
(5)产品中含少量SnCl2,测定SnCl4纯度的方法:取2.00g产品溶于50.00mL的稀盐酸中,加入___________ 溶液作指示剂。用0.0100 mol/LKIO3标准溶液滴定至终点,消耗KIO3标准液20.00mL,反应原理为3SnCl2+KIO3+6HCl=3SnCl4+KI+3H2O, +5I-+6H+=3I2+3H2O,判断滴定终点的依据为
+5I-+6H+=3I2+3H2O,判断滴定终点的依据为___________ ,产品的纯度为___________ 。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl2 | PbCl2 | S |
| 熔点/℃ | -33 | 247 | 426 | 501 | 112 |
| 沸点/℃ | 114 | 623 | 1490 | 950 | 444 |
(1)仪器b的名称
(2)整套装置的连接顺序
(3)碱石灰的作用为
(4)实验结束后,得到粗产品中常溶有少量SnCl2杂质,可用
(5)产品中含少量SnCl2,测定SnCl4纯度的方法:取2.00g产品溶于50.00mL的稀盐酸中,加入
 +5I-+6H+=3I2+3H2O,判断滴定终点的依据为
+5I-+6H+=3I2+3H2O,判断滴定终点的依据为
您最近半年使用:0次
解题方法
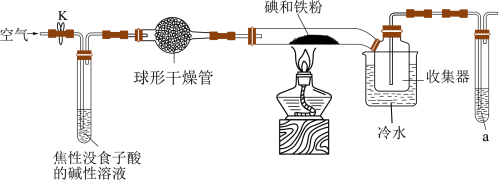
4 . 碘化亚铁( )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)_______ ,若无此装置,写出铁粉参与的副反应的化学方程式:_______ ,硬质玻璃管中制备碘化亚铁的化学方程式为_______ 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是_______ ,收集器浸泡在冷水中的原因是_______ 。
(3)试剂a的作用是_______ 。
(4)已知氧化性: 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:_______ 。
 )在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收
)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
)
(2)硬质玻璃管直接接入收集器而不用导管的原因是
(3)试剂a的作用是
(4)已知氧化性:
 。往含
。往含 的溶液中通入
的溶液中通入 标准状况下的氯气,充分反应,请写出该反应的离子方程式:
标准状况下的氯气,充分反应,请写出该反应的离子方程式:
您最近半年使用:0次
解题方法
5 . 下列仪器的名称及用途均正确的是
| 选项 | 仪器 | 名称 | 用途 |
| A |
| 溶量瓶 | 可用于精确配制一定浓度的溶液 |
| B |
| 蒸发皿 | 可在三脚架上直接加热,用于蒸发浓缩溶液 |
| C |
| 量筒 | 用来量取一定体积的液体的仪器 例如:可用  的量筒量取 的量筒量取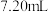 液体 液体 |
| D |
| 洗气瓶 | 可用于干燥气体或除去气体中的杂质, 例如:用饱和  溶液除去 溶液除去 中的 中的 气体 气体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
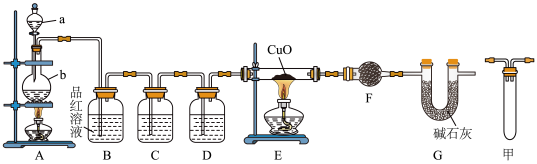
6 . 甲研究小组按如图装置进行实验,验证锌与浓硫酸反应生成物中的气体成分,取足量的Zn置于b中,向a中加入适量浓硫酸,经过一段时间的反应,Zn仍有剩余。______ ,仪器b的名称是_______ 。
(2)在反应初始阶段 ,装置A中发生的化学方程式为__________ 。
(3)装置C中若为酸性高锰酸钾溶液,则对应的离子方程式 为____________ 。
(4)装置F的名称为球形干燥管,其中加入的试剂是_______ ,作用为________ 。
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为________ 。
(2)在
(3)装置C中若为酸性高锰酸钾溶液,则对应的
(4)装置F的名称为球形干燥管,其中加入的试剂是
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为
您最近半年使用:0次
7 . 名称为“容量瓶”的仪器是
A.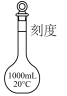 | B.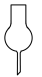 | C.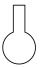 | D. |
您最近半年使用:0次
8 . 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
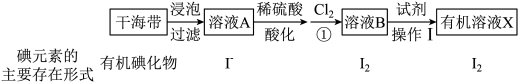
(1)提碘的原料一般选择海带或海藻,是因为___________ 。
(2)操作I中,实验室可用如图仪器将 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为___________ ,该步操作的名称为___________ ;下图所示的有机溶剂可以是___________ (填涂编号),选择依据是___________ ;分离液体时上层的溶液要从___________ 口(填“上”或者“下”)倒出在另一个烧杯中。

A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加___________ ,如出现___________ 现象,则证明 能代替氯水。
能代替氯水。

(1)提碘的原料一般选择海带或海藻,是因为
(2)操作I中,实验室可用如图仪器将
 富集到有机溶液X中,该仪器名称为
富集到有机溶液X中,该仪器名称为
A.酒精 B.醋酸 C.四氯化碳 D.苯
(3)为寻找反应①中氯水的替代品,某同学设计了如下实验来证明
 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加
溶液作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,滴加 能代替氯水。
能代替氯水。
您最近半年使用:0次
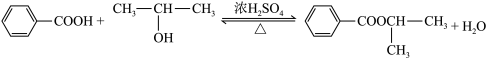
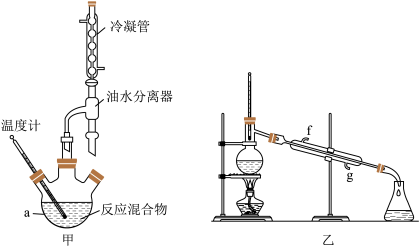
9 . 某化学兴趣小组设计图甲装置制备苯甲酸异丙酯,其反应原理如下:
实验步骤:
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸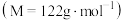 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
步骤ii.加热至70℃左右保持恒温半小时;
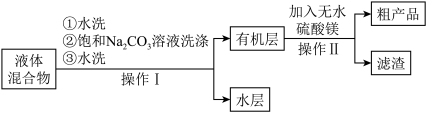
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
回答下列问题:
(1)图甲中仪器a的名称为___________ ,步骤i中选择的仪器a的容积大小为___________ (填标号)。
A. B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是___________ 。判断酯化反应接近反应限度的现象为___________ 。
(3)本实验一般可采用的加热方式为___________ 。
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是___________ ,操作Ⅱ中加入无水硫酸镁的作用为___________ 。
(5)步骤iv操作时应收集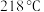 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为___________ (填物质名称)。
(6)如果得到的苯甲酸异丙酯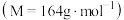 的质量为
的质量为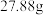 ,那么该实验的产率为
,那么该实验的产率为___________ %(保留3位有效数字)。
| 物质 | 相对分子质量 | 密度/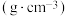 | 沸点/℃ | 水溶性 |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶 |
| 异丙醇 | 60 | 0.79 | 82 | 易溶 |
| 苯甲酸异丙酯 | 164 | 1.08 | 218 | 不溶 |
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸
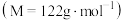 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;步骤ii.加热至70℃左右保持恒温半小时;
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
回答下列问题:
(1)图甲中仪器a的名称为
A.
 B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是
(3)本实验一般可采用的加热方式为
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是
(5)步骤iv操作时应收集
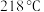 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为(6)如果得到的苯甲酸异丙酯
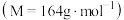 的质量为
的质量为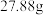 ,那么该实验的产率为
,那么该实验的产率为
您最近半年使用:0次
解题方法
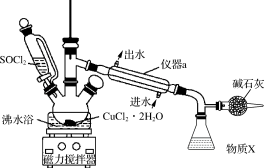
10 . 氯化铜在工农业生产中具有重要的用途。某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2,并回收过量的SOCl2。回答下列问题:
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。
(1)仪器a的名称是_______ ,锥形瓶中得到的物质X的化学式为_______ 。
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是_______
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①滴定到终点时溶液中的颜色变化是_______
②该试样中铜元素的百分含量为_______ 。
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2
 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。(1)仪器a的名称是
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O
 =S4O
=S4O +2I-)。
+2I-)。①滴定到终点时溶液中的颜色变化是
②该试样中铜元素的百分含量为
您最近半年使用:0次