解题方法
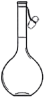
1 . 下列仪器的名称及用途均正确的是
| 选项 | 仪器 | 名称 | 用途 |
| A |
| 溶量瓶 | 可用于精确配制一定浓度的溶液 |
| B |
| 蒸发皿 | 可在三脚架上直接加热,用于蒸发浓缩溶液 |
| C |
| 量筒 | 用来量取一定体积的液体的仪器 例如:可用  的量筒量取 的量筒量取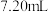 液体 液体 |
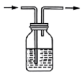
| D |
| 洗气瓶 | 可用于干燥气体或除去气体中的杂质, 例如:用饱和  溶液除去 溶液除去 中的 中的 气体 气体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
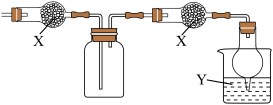
选项 | 试剂X | 收集气体 | 试剂Y |
A. | 碱石灰 | 氯化氢 | 水 |
B. | 碱石灰 | 氨气 | 水 |
C. | 五氧化二磷 | 二氧化硫 | 氢氧化钠溶液 |
D. | 氯化钙 | 一氧化氮 | 氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 . 下列装置可以用于相应实验的是
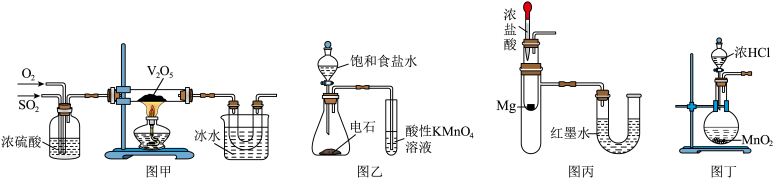
| A.图甲制取并收集SO3 | B.图乙检验乙炔具有还原性 |
| C.图丙中红墨水左高右低 | D.图丁装置制取Cl2 |
您最近半年使用:0次
昨日更新
|
215次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
4 . 实验室制备下列气体所选试剂、制备装置及收集方法均正确的是

| 气体 | 试剂 | 制备装置 | 收集方法 | |
| A | NH3 | NH4Cl | a | e |
| B | Cl2 | MnO2 + 浓盐酸 | c | d |
| C | SO2 | Cu + 浓硫酸 | b | d |
| D | NO2 | Cu + 浓硝酸 | b | f |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . 下列实验装置使用不正确 的是
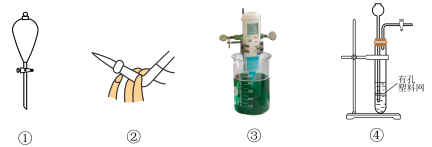
| A.图①装置可用于分离溴苯和水的混合物,且溴苯从下口放出 |
| B.可用图②方法排出碱式滴定管下端的气泡 |
| C.图③装置是用pH计测定溶液pH值,使用前pH计需洗涤和校正 |
| D.图④装置用于电石与水制取乙炔 |
您最近半年使用:0次
名校
解题方法
6 . 在实验室做H2在氯气中燃烧实验中,下列标志的要求不需要的是
A. | B. | C. | D. |
您最近半年使用:0次
名校
解题方法
7 . 下列实验项目所选用的主要实验仪器里,不合理的是
选项 | 实验项目 | 主要实验仪器 |
A | 验证镁与盐酸反应为放热反应 | 试管、温度计 |
B | 探究二氧化硫的漂白作用 | 试管、酒精灯、胶头滴管 |
C | 蒸发精制氯化钠溶液制精盐 | 坩埚、酒精灯、坩埚钳、陶土网 |
D | 配制一定物质的量浓度的硫酸 | 烧杯、量筒、玻璃棒、容量瓶、胶头滴管 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
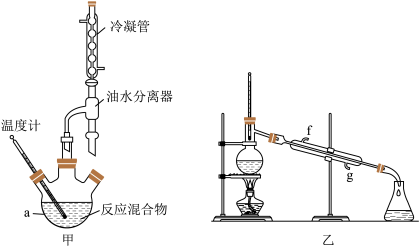
8 . 某化学兴趣小组设计图甲装置制备苯甲酸异丙酯,其反应原理如下:
实验步骤:
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸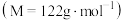 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
步骤ii.加热至70℃左右保持恒温半小时;
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
回答下列问题:
(1)图甲中仪器a的名称为___________ ,步骤i中选择的仪器a的容积大小为___________ (填标号)。
A. B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是___________ 。判断酯化反应接近反应限度的现象为___________ 。
(3)本实验一般可采用的加热方式为___________ 。
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是___________ ,操作Ⅱ中加入无水硫酸镁的作用为___________ 。
(5)步骤iv操作时应收集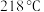 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为___________ (填物质名称)。
(6)如果得到的苯甲酸异丙酯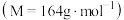 的质量为
的质量为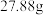 ,那么该实验的产率为
,那么该实验的产率为___________ %(保留3位有效数字)。
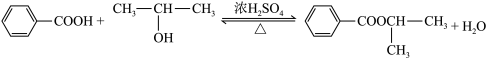
| 物质 | 相对分子质量 | 密度/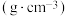 | 沸点/℃ | 水溶性 |
| 苯甲酸 | 122 | 1.27 | 249 | 微溶 |
| 异丙醇 | 60 | 0.79 | 82 | 易溶 |
| 苯甲酸异丙酯 | 164 | 1.08 | 218 | 不溶 |
步骤i.在图甲干燥的仪器a中加入24.4g苯甲酸
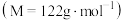 、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;
、20mL异丙醇和10mL浓硫酸,再加入几粒沸石;步骤ii.加热至70℃左右保持恒温半小时;
步骤iii.将图甲的仪器a中的液体混合物进行如下操作得到粗产品:
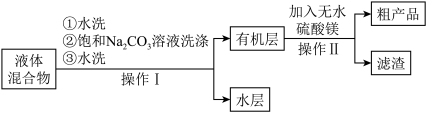
回答下列问题:
(1)图甲中仪器a的名称为
A.
 B.
B. C.
C. D.
D.
(2)实验中,加入的异丙醇需过量,其目的是
(3)本实验一般可采用的加热方式为
(4)操作Ⅰ中饱和碳酸钠溶液洗涤的目的是
(5)步骤iv操作时应收集
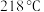 的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为
的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为(6)如果得到的苯甲酸异丙酯
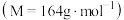 的质量为
的质量为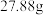 ,那么该实验的产率为
,那么该实验的产率为
您最近半年使用:0次
解题方法
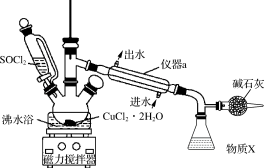
9 . 氯化铜在工农业生产中具有重要的用途。某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2,并回收过量的SOCl2。回答下列问题:
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。
(1)仪器a的名称是_______ ,锥形瓶中得到的物质X的化学式为_______ 。
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是_______
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①滴定到终点时溶液中的颜色变化是_______
②该试样中铜元素的百分含量为_______ 。
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2
 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。(1)仪器a的名称是
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O
 =S4O
=S4O +2I-)。
+2I-)。①滴定到终点时溶液中的颜色变化是
②该试样中铜元素的百分含量为
您最近半年使用:0次
名校
解题方法
10 . 实验是化学探究的一种重要途径。下列有关实验的描述正确的是
A.用干燥的红色石蕊试纸检验 |
| B.在中和热测定的实验中,做三次平行实验最少要使用6次温度计 |
| C.进行焰色试验时,可用玻璃棒替代铂丝 |
D.称取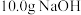 固体配制 固体配制 溶液 溶液 |
您最近半年使用:0次
7日内更新
|
144次组卷
|
2卷引用:2024届黑龙江省绥化市高三下学期3月联考模拟检测化学试卷