解题方法
1 . 某同学为了获取在 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
Ⅰ.向三颈瓶中加入饱和 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);
Ⅱ.打开磁力搅拌器,立即加入 溶液;
溶液;
Ⅲ.采集三颈瓶内空气中 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。
实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
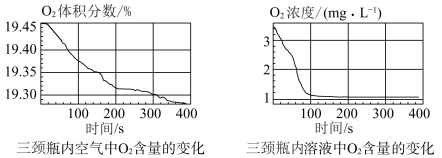
实验数据:
(1)搅拌的目的是___________ 。
(2)生成白色絮状沉淀的离子方程式为___________ 。
(3)沉淀由白色变为红褐色发生反应的化学方程式为___________ 。
(4)通过上述实验,可得到“在 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是___________ 。
(5)结合上述实验,提出制备 过程中应注意的事项
过程中应注意的事项___________ (回答一项即可)。
 制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。
制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图示装置进行了如下实验。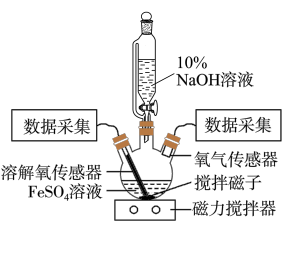
Ⅰ.向三颈瓶中加入饱和
 溶液,按图示连接装置(夹持装置已略去,气密性已检查);
溶液,按图示连接装置(夹持装置已略去,气密性已检查);Ⅱ.打开磁力搅拌器,立即加入
 溶液;
溶液;Ⅲ.采集三颈瓶内空气中
 体积分数和溶液中
体积分数和溶液中 浓度的数据。
浓度的数据。实验现象:
三颈瓶中生成白色絮状沉淀,沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:
(1)搅拌的目的是
(2)生成白色絮状沉淀的离子方程式为
(3)沉淀由白色变为红褐色发生反应的化学方程式为
(4)通过上述实验,可得到“在
 制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是(5)结合上述实验,提出制备
 过程中应注意的事项
过程中应注意的事项
您最近半年使用:0次
解题方法
2 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是___________ ;分别向新制取的 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是___________ 氢氧化物,其中 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为___________ 。
(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。
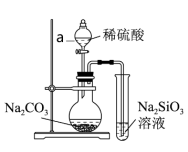
①图中仪器a的名称是___________ ,圆底烧瓶中发生反应的离子方程式为___________ 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是___________ ,该实验能证明非金属性强弱,依据的原理是___________ 。
(1)将大小相同的钠、镁、铝(除去氧化膜)分别投入到冷水中,反应最剧烈的是
 沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明
沉淀中滴加稀盐酸和氢氧化钠溶液,结果沉淀都溶解,说明 是
是 与氢氧化钠溶液反应的离子方程式为
与氢氧化钠溶液反应的离子方程式为(2)利用如图装置验证碳、硅、硫三种元素的非金属性强弱。

①图中仪器a的名称是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
您最近半年使用:0次
解题方法
3 . 某同学设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。下列说法错误的是
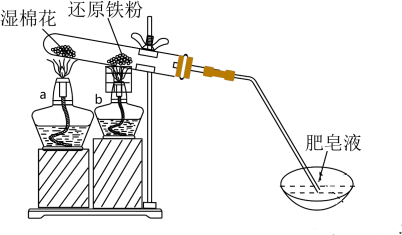
| A.试管中发生的是置换反应 |
| B.湿棉花的作用是提供水蒸气 |
C.点燃酒精灯的顺序是先 后 后 |
| D.加热时试管内生成红色物质,点燃肥皂泡可听到爆鸣声 |
您最近半年使用:0次
名校
解题方法
4 . 如下图所示,某同学利用 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。____________ 。
(2)装置C中的实验现象是____________ ,该实验现象说明 具有
具有______ 性。
(3)能验证 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是____________ 。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:____________ 。
(5)甲同学设计下图装置甲来制备 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题:____________ 。
②乙同学检验产物中有 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→______ →B(按顺序填各接口字母,装置可重复使用)。
③可以证明产物中含有 的实验现象是:
的实验现象是:____________ ,乙中澄清石灰水变浑浊。
 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。
(2)装置C中的实验现象是
 具有
具有(3)能验证
 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是(4)装置E的目的是探究
 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:(5)甲同学设计下图装置甲来制备
 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题: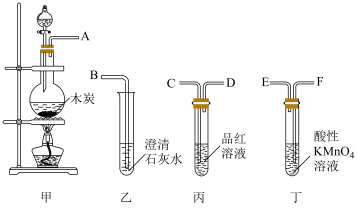
②乙同学检验产物中有
 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→③可以证明产物中含有
 的实验现象是:
的实验现象是:
您最近半年使用:0次
名校
解题方法
5 . 下列由实验现象推出的实验结论正确的是
| 选项 | 实验过程 | 实验现象 | 实验结论 |
| A | 将少量的硝酸铜受热分解 (产物为CuO、NO2、O2) | 收集气体后,用带火星的木条检验,木条复燃 | NO2支持燃烧 |
| B | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| C | 将AgCl固体加入水中,再向其中滴入几滴HI | 固体由白色变为黄色 | HI酸性强 |
| D | 把NaClO溶液滴到pH试纸上 | 测得pH=10 | NaClO溶液水解显碱性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
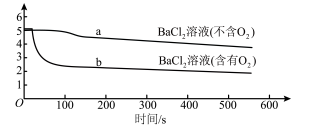
6 . 分别向等体积的不含O2、含有O2的0.1mol/L BaCl2溶液中通入SO2,探究体系中物质间的相互作用,实验记录如下。(已知:pH越小,溶液酸性越强)
下列说法不正确的是
下列说法不正确的是
pH变化 |
|
溶液中是否产生沉淀 | 不含O2的BaCl2溶液中没有白色沉淀, 含有O2的BaCl2溶液中产生白色沉淀。 |
| A.a所示溶液的pH降低的原因:SO2与H2O反应生成H2SO3,溶液的c(H+)增大 |
B.b所示溶液中发生反应: |
| C. SO2通入不含O2的BaCl2溶液后,再加入NaOH溶液,产生BaSO3沉淀 |
D.b比a所示溶液的pH小的原因: |
您最近半年使用:0次
解题方法
7 . 已知: ;
; 熔点为16.8℃、沸点为44.8℃。用如图所示装置设计实验检验
熔点为16.8℃、沸点为44.8℃。用如图所示装置设计实验检验 分解产物,下列说法正确的是
分解产物,下列说法正确的是
 ;
; 熔点为16.8℃、沸点为44.8℃。用如图所示装置设计实验检验
熔点为16.8℃、沸点为44.8℃。用如图所示装置设计实验检验 分解产物,下列说法正确的是
分解产物,下列说法正确的是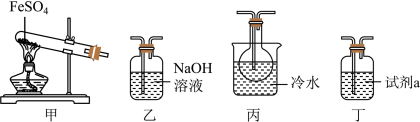
| A.实验前应先检查装置的气密性 | B.装置连接顺序是甲→丁→丙→乙 |
| C.分解所得红棕色固体溶于KSCN溶液 | D.丁中溴水褪色表明 有漂白性 有漂白性 |
您最近半年使用:0次
名校
解题方法
8 . 甲研究小组按如图装置进行实验,验证锌与浓硫酸反应生成物中的气体成分,取足量的Zn置于b中,向a中加入适量浓硫酸,经过一段时间的反应,Zn仍有剩余。______ ,仪器b的名称是_______ 。
(2)在反应初始阶段 ,装置A中发生的化学方程式为__________ 。
(3)装置C中若为酸性高锰酸钾溶液,则对应的离子方程式 为____________ 。
(4)装置F的名称为球形干燥管,其中加入的试剂是_______ ,作用为________ 。
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为________ 。
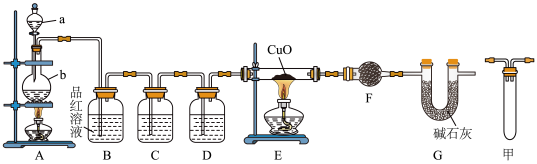
(2)在
(3)装置C中若为酸性高锰酸钾溶液,则对应的
(4)装置F的名称为球形干燥管,其中加入的试剂是
(5)有同学认为A、B间应增加图中的甲装置,该装置的作用为
您最近半年使用:0次
名校
解题方法
9 . 自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题: 对应图1中物质的化学式为
对应图1中物质的化学式为___________ 。
(2)将一定量的 气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
(3) 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为___________ 。
(4)铜和 的浓溶液反应生成
的浓溶液反应生成 的化学方程式为
的化学方程式为___________ ;若要证明该反应产物有 ,需要采取的操作是
,需要采取的操作是___________ 。
(5)为了验证木炭与浓硫酸反应放出的气体是 和
和 和少量
和少量 。回答下列问题:
。回答下列问题: 的名称是
的名称是___________ 洗气瓶①②中溶液褪色,体现二氧化硫的性质依次为___________ (填序号)。
A.氧化性、还原性 B.漂白性、还原性 C.漂白性、氧化性 D.还原性、漂白性
②洗气瓶②中酸性高锰酸钾溶液不能用足量的新制氯水代替的原因是___________ 。
③上述实验证明木炭与浓硫酸反应放出的气体中有少量 的实验现象是
的实验现象是___________ 。
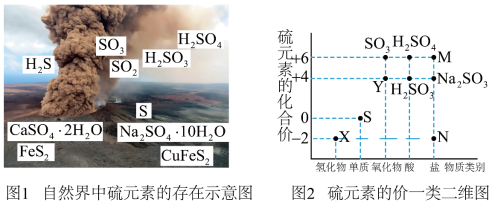
 对应图1中物质的化学式为
对应图1中物质的化学式为(2)将一定量的
 气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。
气体通入下列溶液中,能观察到白色沉淀现象的是___________(填标号)。A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(3)
 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为(4)铜和
 的浓溶液反应生成
的浓溶液反应生成 的化学方程式为
的化学方程式为 ,需要采取的操作是
,需要采取的操作是(5)为了验证木炭与浓硫酸反应放出的气体是
 和
和 和少量
和少量 。回答下列问题:
。回答下列问题: 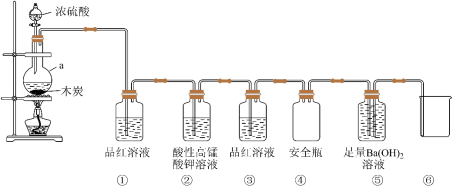
 的名称是
的名称是A.氧化性、还原性 B.漂白性、还原性 C.漂白性、氧化性 D.还原性、漂白性
②洗气瓶②中酸性高锰酸钾溶液不能用足量的新制氯水代替的原因是
③上述实验证明木炭与浓硫酸反应放出的气体中有少量
 的实验现象是
的实验现象是
您最近半年使用:0次
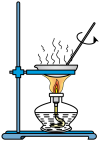
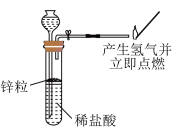
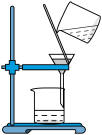
10 . 应用下列装置能达到实验目的的是
| A | B | |
| 装置 |
|
|
| 目的 | 从 溶液中制得 溶液中制得 晶体 晶体 | 可用于制备并检验氢气的可燃性 |
| C | D | |
| 装置 |
|
|
| 目的 | 除去 中的HCl并干燥 中的HCl并干燥 | 分离 胶体与NaCl溶液 胶体与NaCl溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次