1 . 下列实验操作能达到对应的实验目的的是
实验目的 | 实验操作 | |
A | 除去苯中混有的少量苯酚 | 加入适量的浓溴水,过滤 |
B | 制乙炔并证明其具有还原性 | 向电石中滴入饱和食盐水,将产生的气体通过 溶液后通入酸性 溶液后通入酸性 溶液 溶液 |
C | 证明纤维素发生水解反应生成还原性糖 | 将少量脱脂棉与稀硫酸混合加热,冷却后取少量溶液于试管中,加入新制的 |
D | 证明木炭与浓硫酸反应生成 | 木炭与浓硫酸混合加热,将产生的气体通入澄清石灰水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 某研究小组在实验室进行硫的化合物系列实验。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。________ 。
(2)当观察到________ ,即证明H2SO3的酸性比H2CO3强。
Ⅱ.研究铁与硫酸的反应。
已知:浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
(3)上述实验中,铁丝绕成螺旋状的目的是________ 。
(4)实验1中,铁与稀硫酸反应的离子方程式为________ 。
(5)实验2中的现象常被称为________ 。
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。________ ;检测装置A的溶液中含有Fe3+的试剂是_______ 。
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有________ 。
Ⅰ.验证H2SO3的酸性比H2CO3强,甲同学设计下图装置。
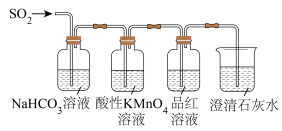
(2)当观察到
Ⅱ.研究铁与硫酸的反应。
已知:浓H2SO4的沸点为338.2℃。
a.乙同学设计如下表所示的实验1、2:
| 实验 | 试剂 | 现象 | |
| 1 | 螺旋状铁丝、稀硫酸 | 铁丝表面有大量气体产生。 |
| 2 | 螺旋状铁丝、浓硫酸 | 铁丝表面迅速发黑(Fe3O4),有少量气体产生,反应很快停止。 | |
(3)上述实验中,铁丝绕成螺旋状的目的是
(4)实验1中,铁与稀硫酸反应的离子方程式为
(5)实验2中的现象常被称为
b.丙同学设计如图所示装置的实验3:
加热试管A,温度保持在250℃~300℃,产生大量气体,B中品红褪色,D处始终未检测到可燃性气体,实验结束后,检验到A的溶液中既有Fe3+又有Fe2+。
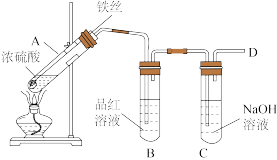
(7)分析实验1、2、3,可知影响铁和硫酸反应产物多样性的因素有
您最近半年使用:0次
名校
3 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,E是水晶的主要成分,化合物c是一种形成酸雨的大气污染物。___________ 。
(2)反应①的化学方程式是___________ 。反应②的离子方程式是___________ 。
(3)写出G的一种用途是___________ ,其与氢氧化钠溶液反应的化学方程式为___________ 。
(4)反应③的化学方程式是___________ 。
(5)下列溶液中能用来区分 和
和 气体的是
气体的是___________ (填序号)。
①澄清石灰水 ② 溶液 ③酸性
溶液 ③酸性 溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液

(2)反应①的化学方程式是
(3)写出G的一种用途是
(4)反应③的化学方程式是
(5)下列溶液中能用来区分
 和
和 气体的是
气体的是①澄清石灰水 ②
 溶液 ③酸性
溶液 ③酸性 溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
您最近半年使用:0次
名校
解题方法
4 . 如下图所示,某同学利用 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。____________ 。
(2)装置C中的实验现象是____________ ,该实验现象说明 具有
具有______ 性。
(3)能验证 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是____________ 。
(4)装置E的目的是探究 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:____________ 。
(5)甲同学设计下图装置甲来制备 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题:____________ 。
②乙同学检验产物中有 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→______ →B(按顺序填各接口字母,装置可重复使用)。
③可以证明产物中含有 的实验现象是:
的实验现象是:____________ ,乙中澄清石灰水变浑浊。
 和浓
和浓 制取
制取 并探究其性质。
并探究其性质。
(2)装置C中的实验现象是
 具有
具有(3)能验证
 具有酸性氧化物的通性的实验现象是
具有酸性氧化物的通性的实验现象是(4)装置E的目的是探究
 与品红作用的可逆性,请写出实验操作及现象:
与品红作用的可逆性,请写出实验操作及现象:(5)甲同学设计下图装置甲来制备
 ,但乙同学提出:甲同学制得的
,但乙同学提出:甲同学制得的 中可能含有
中可能含有 ,并用下图的甲、乙、丙、丁装置来检验产物中是否有
,并用下图的甲、乙、丙、丁装置来检验产物中是否有 和
和 。回答下列问题:
。回答下列问题: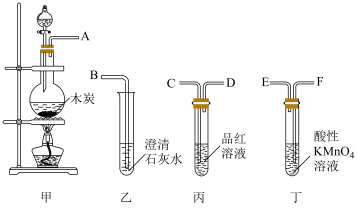
②乙同学检验产物中有
 和
和 ,按气流由左向右流向,连接上述装置的正确顺序是A→
,按气流由左向右流向,连接上述装置的正确顺序是A→③可以证明产物中含有
 的实验现象是:
的实验现象是:
您最近半年使用:0次
名校
解题方法
5 . 能用于鉴别 和
和 的溶液是
的溶液是
 和
和 的溶液是
的溶液是| A.澄清石灰水 | B.酸性高锰酸钾溶液 | C.酚酞溶液 | D. 溶液 溶液 |
您最近半年使用:0次
6 . 下列实验操作不能实现预期目的的是
| 选项 | 实验操作 | 预期目的 |
| A | 向含有酚酞试液的 溶液中逐滴滴加足量 溶液中逐滴滴加足量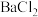 溶液 溶液 | 验证 能水解 能水解 |
| B | 将含有少量 的 的 气体一次通过饱和 气体一次通过饱和 溶液、浓硫酸 溶液、浓硫酸 | 提纯 |
| C | 向 溶液中滴入硫酸酸化的 溶液中滴入硫酸酸化的 溶液 溶液 | 验证氧化性: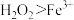 |
| D | 向浓度均为 的 的 和 和 溶液中分别滴加酚酞, 溶液中分别滴加酚酞, 溶液不变色, 溶液不变色, 溶液变成红色 溶液变成红色 | 证明非金属性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 下列物质中,不能用于鉴别 的是
的是
 的是
的是| A.酸性高锰酸钾溶液 | B.品红溶液 | C. 溶液 溶液 | D.氯水 |
您最近半年使用:0次
8 . 以黄铁矿(主要成分FeS2)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。

(1)黄铁矿中硫元素的化合价为_______ 。
(2)由炉渣制备还原铁粉的化学方程式为_______ 。
(3)欲得到更纯的NaHSO3,反应①应通入_______ (填 “过量”或“不足量”)的气体。
(4)因为Na2S2O5具有_______ 性, 长期放置会导致商品Na2S2O5中不可避免地存在_______ 杂质,检验杂质的方法是_______ 。
(5)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的亚铁离子,反应离子方程式如下 。
。
某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为_______ %(精确到小数点后两位)。(假设杂质中无铁元素,杂质也不与标准重铬酸钾溶液反应,铁的相对原子质量为56)

(1)黄铁矿中硫元素的化合价为
(2)由炉渣制备还原铁粉的化学方程式为
(3)欲得到更纯的NaHSO3,反应①应通入
(4)因为Na2S2O5具有
(5)一般用K2Cr2O7滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的亚铁离子,反应离子方程式如下
 。
。某次实验称取0.2800 g样品,滴定时消耗浓度为0.03000 mol·L-1的K2Cr2O7溶液25.10 mL,则样品中铁含量为
您最近半年使用:0次
解题方法
9 . 下列实验正确的是
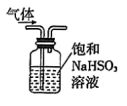 |  | 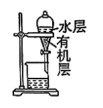 |  |
A.除去 气体中少量的 气体中少量的 | B.分离固体 和 和 | C.用苯萃取碘水中的 | D.模拟工业制备 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
10 . 硫代硫酸钠( ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
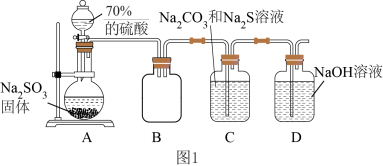
已知: 在酸性溶液中发生反应:
在酸性溶液中发生反应: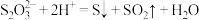
(1)实验室制备 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是_______ 。图1装置B的作用是________ 。
(2)图1装置C中发生反应生成 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是_____ 。
(3)某同学用图2中装置验证装置C中生成了 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是_______ 。
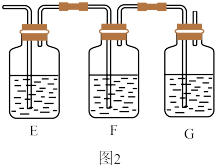
A.品红、 溶液、澄清石灰水
溶液、澄清石灰水
B.酸性 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
C. 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
(4)从装置C中所得溶液经过结晶等操作获得的 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体,________ ,离心沉降,过滤,_______ ,若有白色沉淀生成,则原晶体中含有 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
 ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
已知:
 在酸性溶液中发生反应:
在酸性溶液中发生反应: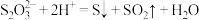
(1)实验室制备
 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是(2)图1装置C中发生反应生成
 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是(3)某同学用图2中装置验证装置C中生成了
 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
A.品红、
 溶液、澄清石灰水
溶液、澄清石灰水 B.酸性
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水C.
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水(4)从装置C中所得溶液经过结晶等操作获得的
 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体, 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
您最近半年使用:0次




