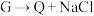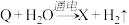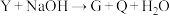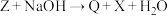吉林省长春市第二实验中学2020-2021学年高一上学期期中考试化学试题
吉林
高一
期中
2020-12-09
384次
整体难度:
较易
考查范围:
认识化学科学、化学实验基础、化学反应原理、常见无机物及其应用、物质结构与性质
一、单选题 添加题型下试题
| A.无水酒精 | B.熔融的氯化钠 | C.纯铝导线 | D.氢氧化钠晶体 |
【知识点】 电解质的电离
| A.复分解反应 | B.蒸发结晶 |
| C.离子反应 | D.氧化还原反应 |
A.H2SO3 2H++SO 2H++SO |
B.NaHCO3 Na++HCO Na++HCO |
C.NH3•H2O NH NH +OH- +OH- |
D.NaHSO4 Na++HSO Na++HSO |
【知识点】 电离方程式解读 弱电解质的电离方程式解读
| A.物质所含元素化合价变化是判断氧化还原反应的依据 |
| B.在氧化还原反应中,金属单质只体现还原性,金属阳离子只体现氧化性 |
| C.在一个氧化还原反应中,有一种元素被氧化,必有另一种元素被还原 |
| D.某元素在反应中由化合物转化为单质,该元素一定被氧化 |
【知识点】 氧化还原反应基本概念 氧化还原反应的定义及实质 氧化还原反应的应用
| A.用浸有水的毛巾捂住口鼻 | B.将人群逆风向疏散 |
| C.将人群向低处疏散 | D.向泄漏地点撒一些石灰 |
| A.固体NaCl不存在阴阳离子,不导电 |
| B.Na2O、Fe2O3、Na2O2均属于碱性氧化物 |
| C.硫酸钡溶液几乎不导电,但硫酸钡属于电解质 |
| D.金刚石和石墨是同素异形体,化学性质不同,物理性质相同 |
| 酸性氧化物 | 酸 | 盐 | 混合物 | 电解质 | |
| A | SiO2 | HClO | 烧碱 | CuSO4·5H2O | CO2 |
| B | Na2O2 | HNO3 | NaHSO4 | 漂白粉 | Mg |
| C | SO3 | H2SiO3 | 纯碱 | 氯水 | NaCl |
| D | NO | Al(OH)3 | BaCO3 | 盐酸 | NH3 |
| A.A | B.B | C.C | D.D |
| A.氢氧化铁胶体具有吸附性,能吸附水中的悬浮颗粒沉降,因而常用于净水 |
| B.实验室中可用丁达尔效应区分胶体和溶液 |
| C.胶体区别于其他分散系的本质是有丁达尔效应 |
| D.云、烟、雾等都是胶体 |
| A.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe2+ |
| C.氢氧化镁溶于盐酸:Mg(OH)2+H+=Mg2++H2O |
D.Cu(OH)2与稀硫酸反应: |
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO =BaSO4↓+H2O =BaSO4↓+H2O |
B.Ca(HCO3)2与过量NaOH溶液反应:Ca2++HCO +OH-=CaCO3↓+H2O +OH-=CaCO3↓+H2O |
C.NaOH溶液中通入少量CO2:2OH-+CO2=CO +H2O +H2O |
| D.CH3COOH溶液与NaOH溶液反应:H++OH-=H2O |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| 实验目的 | 实验操作 | |
| A | 证明某溶液中含有K+ | 用洁净的铂丝蘸取待测液在酒精灯的火焰上灼烧 |
| B | 证明某溶液中含有Cl- | 向溶液中滴入硝酸酸化的AgNO3溶液 |
| C | 实验室制Cl2 | 向MnO2中加入稀盐酸并加热 |
| D | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到热NaOH溶液中 |
| A.A | B.B | C.C | D.D |
| A.将过量Na2O2粉末加入紫色石蕊试液中振荡,溶液变为蓝色,且有气泡产生 |
| B.将过量Na2O2粉末加入FeCl3溶液中并振荡,产生红褐色沉淀,且有气泡产生 |
| C.凡是有Na2O2参与的反应,均能产生O2 |
| D.Na2O2粉末在空气中长期放置不变质 |
| A.次氯酸中氯元素呈 -1 价 |
| B.次氯酸既不是电解质,也不是非电解质 |
| C.新制氯水长期放置后仍可用于自来水的消毒 |
| D.往氯水中加入 AgNO3 溶液产生白色沉淀,说明氯水中有 Cl-存在 |
| A.钠熔成小球 | B.钠剧烈燃烧 |
| C.产生刺激性气味气体 | D.生成淡黄色固体 |
【知识点】 钠的化学性质
| A.Ca(ClO)2 | B.CaCl2 | C.Ca(ClO)2和CaCl2 | D.HClO |
【知识点】 漂白粉和漂粉精 漂白粉和漂粉精的用途解读
| A.加入澄清石灰水 | B.分别加热 | C.加NaOH | D.加CaCl2溶液 |
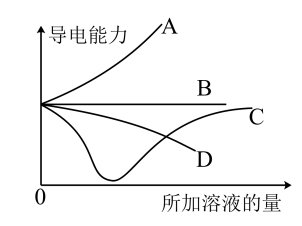
| A.曲线A表示NaOH溶液中滴加稀盐酸 |
| B.曲线B表示CH3COOH溶液中滴加KOH溶液 |
| C.曲线C表示Ba(OH)2溶液中滴加稀硫酸 |
D.曲线D表示Cu(OH)2悬浊液中滴加 溶液 溶液 |
【知识点】 物质水溶液的导电性解读 离子反应的发生及书写 弱电解质的电离平衡
A.无色溶液:Na+、Cu2+、Cl-、 、 、 | B.酸性溶液: 、Fe3+、S2−、 、Fe3+、S2−、 |
C.遇酚酞变红的溶液:Na+、K+、 、 、 | D.碱性溶液:K+、Al3+、 、 、 |
二、未知 添加题型下试题
三、单选题 添加题型下试题
| 序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
| ① | NaCl | BaCl2 | 加入过量的 K2CO3 溶液,过滤,再加适量的盐酸并加 热 |
| ② | FeSO4 溶液 | CuSO4 | 加入过量 Fe 粉,过滤 |
| ③ | Cl2 | HCl | 通过盛 NaOH 溶液洗气瓶 |
| ④ | NaHCO3 | Na2CO3 | 加热法 |
| A.①③④ | B.②③④ | C.②④ | D.② |
| A.1.6gO2和O3的混合物含有氧原子的数目为0.1NA |
| B.欲配制1.00L1.00mol·L−1的NaCl溶液,可将58.5gNaCl溶于1.00L水中 |
| C.标准状况下,22.4LH2中的原子数为NA |
| D.11.2LCO2所含有的碳原子数为0.5NA |
【知识点】 阿伏加德罗常数的求算解读
| A.78gNa2O2中含有的离子个数为3NA |
| B.17g氨气所含质子数目为11NA |
| C.标准状况下22.4L的H2O,含有H2O分子数为NA |
| D.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为1NA |
| A.分子数目比为7:11 | B.原子数目比为11:7 |
| C.体积比为7:11 | D.密度比为7:11 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读
| A.25mL0.2mol/L的NaCl溶液 | B.100mL0.1mol/L的NaCl溶液 |
| C.25mL0.2mol/L的Na2SO4溶液 | D.10mL0.5mol/L的Na2CO3溶液 |
| A.KClO3在反应中是还原剂 |
| B.1molKClO3参加反应,能得到44.8L气体 |
| C.在反应中H2C2O4 既不是氧化剂也不是还原剂 |
| D.1molKClO3参加反应有1mol电子转移 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
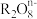 离子在一定条件下可将
离子在一定条件下可将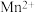 离子氧化成
离子氧化成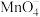 离子。若反应后
离子。若反应后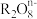 变成
变成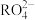 ,又知反应中氧化剂和还原剂的个数之比是5∶2,则n值为
,又知反应中氧化剂和还原剂的个数之比是5∶2,则n值为| A.1 | B.2 | C.3 | D.4 |
 通入KOH溶液中,反应后得到KCl、KClO、
通入KOH溶液中,反应后得到KCl、KClO、 的混合液,经测定,
的混合液,经测定, 和
和 的物质的量之比为1∶3,则
的物质的量之比为1∶3,则 与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )
与KOH溶液反应时,被还原的氯原子与被氧化的氯原子的物质的量之比为( )| A.2∶5 | B.11∶3 | C.3∶1 | D.4∶1 |
四、计算题 添加题型下试题
(1)在标准状况下,有物质①44.8LH2,②4gCH4,③1molH2O,④3.01×1023个HCl,含氢原子数由多到少的顺序是
(2)标准状况下,34gNH3和22.4LCO2的物质的量之比为
(3)5.85g氯化钠配制成500mL溶液,其物质的量浓度为
(4)已知R是一种金属,106.5gR(NO3)3中含有9.03×1023个硝酸根离子,则该硝酸盐的摩尔质量为
(5)88gA和98gB恰好完全反应生成152gC和一定量的气体D。若D的相对分子质量为34,则标准状况下D的体积为
五、填空题 添加题型下试题
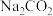 、
、 和食盐等是生活中常见的钠盐。
和食盐等是生活中常见的钠盐。(1)写出苏打与少量醋酸反应的离子方程式
(2)小苏打常用于治疗胃酸过多,写出相应的离子方程
(3)写出实验室检验氯化钠溶液中Cl-的离子方程式
(4)漂白液光照会产生无色无味气体。写出生成气体的离子方程式
(5)氯水与SO2均有漂白性,二者混合则失去漂白性,请写出发生的离子方程式
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①
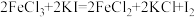
②

③
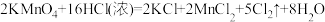
六、解答题 添加题型下试题
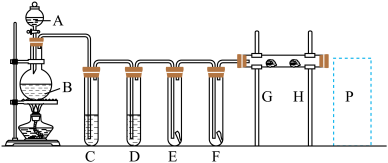
(1)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C为
(2)G是浸有淀粉KI溶液的棉花球,G处现象是
(3)P处应放氢氧化钠溶液吸收尾气,用离子方程式表示所发生的反应
(4)用酸性高锰酸钾和浓盐酸也可以制备氯气,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,当有7.9gKMnO4完全反应时,生成氯气的体积为
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解质的电离 | |
| 2 | 0.94 | 四种基本反应类型 四种基本反应类型与氧化还原反应的关系 蒸发与结晶 | |
| 3 | 0.65 | 电离方程式 弱电解质的电离方程式 | |
| 4 | 0.85 | 氧化还原反应基本概念 氧化还原反应的定义及实质 氧化还原反应的应用 | |
| 5 | 0.94 | 氯气的物理性质 氯气与水的反应 | |
| 6 | 0.94 | 氯水的成分及检验 氯水的性质 | |
| 7 | 0.85 | 单质和化合物 酸、碱、盐、氧化物的概念及其相互联系 电解质与非电解质 几组常见同素异形体 | |
| 8 | 0.94 | 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 非电解质、电解质物质类别判断 | |
| 9 | 0.85 | 胶体的定义及分类 胶体的性质和应用 | |
| 10 | 0.65 | 电离方程式 离子反应的发生条件 离子方程式的书写 离子方程式的正误判断 | |
| 11 | 0.94 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 12 | 0.65 | 胶体的制备 氯气的实验室制法 焰色试验 常见阴离子的检验 | |
| 13 | 0.85 | 氯气与金属单质的反应 镁的结构与化学性质 铁与非金属单质反应 铜与非金属单质反应 | |
| 14 | 0.85 | 过氧化钠 过氧化钠的物理性质、组成、结构及用途 过氧化钠的强氧化性 | |
| 15 | 0.65 | 氯水 次氯酸及其性质 氯水的成分及检验 | |
| 16 | 0.94 | 钠的化学性质 | |
| 17 | 0.94 | 焰色试验 | |
| 18 | 0.94 | 漂白粉和漂粉精 漂白粉和漂粉精的用途 | |
| 19 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 碳酸钠与碳酸氢钠鉴别的实验 | |
| 20 | 0.65 | 物质水溶液的导电性 离子反应的发生及书写 弱电解质的电离平衡 | |
| 21 | 0.94 | 离子反应的发生条件 离子共存 物质共存 限定条件下的离子共存 | |
| 23 | 0.85 | 物质分离、提纯的常见化学方法 物质分离、提纯综合应用 | |
| 24 | 0.85 | 阿伏加德罗常数的求算 | |
| 25 | 0.85 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 26 | 0.85 | 阿伏加德罗定律 阿伏加德罗定律及其推论 | |
| 27 | 0.85 | 物质的量浓度概念、含义 某溶液与物质的量浓度相关的物理量的判断 | |
| 28 | 0.65 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 29 | 0.65 | 氧化还原反应的几组概念 氧化还原反应的规律 基于氧化还原反应守恒规律的计算 化学式与化合价 | |
| 30 | 0.65 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 基于氧化还原反应守恒规律的计算 | |
| 二、未知 | |||
| 22 | 0.85 | 氧化还原反应的规律 | 未知 |
| 三、计算题 | |||
| 31 | 0.65 | 物质的量有关计算 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 | |
| 四、填空题 | |||
| 32 | 0.65 | 离子方程式的书写 漂白粉和漂粉精 碳酸氢钠 常见阴离子的检验 | |
| 33 | 0.65 | 氧化还原反应的几组概念 氧化还原反应定义、本质及特征 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 五、解答题 | |||
| 34 | 0.85 | 氯气的实验室制法 氯气与还原性化合物的反应 氯气与碱溶液反应 化学实验探究 | 实验探究题 |

 溶液
溶液 溶液
溶液 溶液
溶液