按要求填空。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为不可能实现的是___________ (填序号)。
(3)下列三个氧化还原反应中,氧化性最强的物质是___________ 。若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可用反应中的___________ 作氧化剂。
①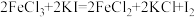
②
③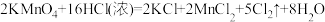
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①
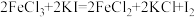
②

③
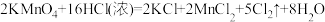
2014高三·全国·专题练习 查看更多[18]
河南省虞城县高级中学2021-2022学年高一上学期中考试化学试题(已下线)易错专题08 氧化还原反应规律的应用及相关计算-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)河南省商丘名校2021-2022学年高一上学期期中联考化学试题(已下线)周末培优1 离子反应的应用 氧化还原反应基本规律-2021-2022学年高一化学课后培优练(人教版2019必修第一册)吉林省长春市第二实验中学2020-2021学年高一上学期期中考试化学试题天津市耀华中学2020-2021学年高一上学期第一次月考化学试题(已下线)第二章 化学物质及其变化(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)第4单元 氧化还原反应(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷山东省滨州市邹平双语学校2019年高一上学期《氧化还原专题》检测浙江省温州市求知中学2018-2019学年高一下学期第二次月考化学试题云南省彝良县一中2018-2019学年高一上学期12月考试化学试题2018-2019学年鲁科版高一化学必修1《氧化剂和还原剂》同步练习题2018年高一化学(人教版)必修1综合题型练习卷:氧化还原反应【全国百强校】黑龙江省牡丹江市第一高级中学2017-2018学年高二下学期期末考试化学试题高中化学人教版 必修1 第二章 化学物质及其变化 3.氧化还原反应 氧化剂和还原剂(已下线)2.3.2 氧化剂和还原剂2016-2017学年吉林长春外国语学校高一上月考二化学卷(已下线)2014年高考化学苏教版一轮复习2-3-1氧化还原反应概念和规律练习卷
更新时间:2021-11-17 19:11:07
|
相似题推荐
【推荐1】在工业上,次磷酸 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: 。
。
请回答下列问题:
(1) 中,P元素的化合价为
中,P元素的化合价为_______ ;该反应中, 被
被_____ (填“氧化”或“还原”)。
(2)配平该离子方程式:___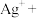 __
__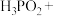 __
__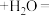 ____Ag↓+___
____Ag↓+___ ____
____ ;
;______ 。
(3) 是一元弱酸,写出其与足量NaOH溶液反应的化学反应方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学反应方程式:_____________ 。
(4)若该反应有5a个电子转移,则镀件镀上银的质量为______________ g。(已知每个银原子质量为bg)
 常用于化学镀银,发生的反应如下:
常用于化学镀银,发生的反应如下: 。
。请回答下列问题:
(1)
 中,P元素的化合价为
中,P元素的化合价为 被
被(2)配平该离子方程式:___
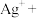 __
__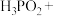 __
__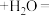 ____Ag↓+___
____Ag↓+___ ____
____ ;
;(3)
 是一元弱酸,写出其与足量NaOH溶液反应的化学反应方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学反应方程式:(4)若该反应有5a个电子转移,则镀件镀上银的质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钠(Na2FeO4)是水处理过程中的一种新型的绿色多功能净水剂。其净水过程中所发生的化学反应主要为4Na2FeO4+10H2O=4Fe(OH)3(胶体)+3O2↑+8NaOH。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
(1)高铁酸钠(Na2FeO4)属于____ (“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为____ 价;与O2互为同素异形体的物质的化学式为_____ 。
(2)将上述反应的化学方程式改写成离子方程式:____ ,该反应中的氧化剂是____ ,氧化剂具有_____ 性。
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴_____ (填化学式)饱和溶液,继续煮沸至____ ,停止加热。
(1)高铁酸钠(Na2FeO4)属于
(2)将上述反应的化学方程式改写成离子方程式:
(3)实验室制备Fe(OH)3胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下面小题。
(1)有以下转化关系:
反应①:___________
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是___________ (填序号)。
(2) 。该反应中,生成物M是
。该反应中,生成物M是___________ (填化学式)。
(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是___________ (填序号,下同)。
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为___________ 。
(5) 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:___________ 。
(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平___________ 。
(1)有以下转化关系:

反应①:
 在上述有序号的反应中,除了①⑥外,需用氧化剂的是
在上述有序号的反应中,除了①⑥外,需用氧化剂的是(2)
 。该反应中,生成物M是
。该反应中,生成物M是(3)针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2↑+H2O
C.H2O2→H2O+O2↑
D.H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
H2O2仅作氧化剂的反应是
(4)取少量NaH放入水中,剧烈反应放出一种无色、无味的气体,并形成一种碱性溶液。NaH与水反应的化学方程式为
(5)
 与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:
与H+或OH-在溶液都不能大量共存,试用离子方程式说明与OH-不共存的原因:(6)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药是将硫磺、木炭、硝酸钾按照一定比例混合,在发生爆炸时,没有产生污染性物质。请书写出该反应方程式并配平
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行深入的研究。物质分类及转化思想贯穿整个化学科学习的始终。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:_______ 。
(2)现有:①KCl晶体②稀盐酸③氨气④熔融NaCl⑤蔗糖⑥铜⑦CO2;其中能导电的是_______ (填序号,下同);属于电解质的是_______ ;属于非电解质的是_______ 。
(3)有下列六个反应:
A.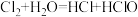
B.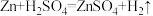
C.
D.
E.
F.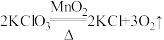
其中属于置换反应的是_______ ,既属于分解反应又属于氧化还原反应的是_______ (填字母)。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①KCl晶体②稀盐酸③氨气④熔融NaCl⑤蔗糖⑥铜⑦CO2;其中能导电的是
(3)有下列六个反应:
A.
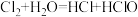
B.
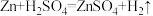
C.

D.

E.

F.
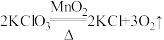
其中属于置换反应的是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有以下反应:
A.3Fe+2O2 Fe3O4 B.2KMnO4
Fe3O4 B.2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C.Zn+H2SO4=ZnSO4+H2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑
E.CH4+2O2 CO2+2H2O F.3O2
CO2+2H2O F.3O2 2O3
2O3
G.CuO+H2 Cu+H2O H.H2SO4+Ba(OH)2=BaSO4↓+2H2O
Cu+H2O H.H2SO4+Ba(OH)2=BaSO4↓+2H2O
(1)将符合反应类型的反应的序号填在下列分类方法后的横线上。(填字母)
①属于化合反应的是___ 。
②属于分解反应的是___ 。
③属于复分解反应的是___ 。
④属于置换反应的是___ 。
(2)以上属于离子反应的是___ ,属于氧化还原反应的是___ 。
(3)A反应中氧化剂是___ ,还原剂是___ ;B反应中氧化剂是___ ,还原剂是___ 。
(4)写出C反应的离子方程式___ 。写出D反应的离子方程式___ 。写出H反应的离子方程式___ 。
A.3Fe+2O2
 Fe3O4 B.2KMnO4
Fe3O4 B.2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑C.Zn+H2SO4=ZnSO4+H2↑ D.CaCO3+2HCl=CaCl2+H2O+CO2↑
E.CH4+2O2
 CO2+2H2O F.3O2
CO2+2H2O F.3O2 2O3
2O3G.CuO+H2
 Cu+H2O H.H2SO4+Ba(OH)2=BaSO4↓+2H2O
Cu+H2O H.H2SO4+Ba(OH)2=BaSO4↓+2H2O(1)将符合反应类型的反应的序号填在下列分类方法后的横线上。(填字母)
①属于化合反应的是
②属于分解反应的是
③属于复分解反应的是
④属于置换反应的是
(2)以上属于离子反应的是
(3)A反应中氧化剂是
(4)写出C反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】① Cu ② CO2 ③液氨 ④H2SO4 ⑤ 酒精 ⑥NaCl溶液 ⑦水 ⑧CaCO3固体
(1)上述物质中属于电解质的是_____ (填序号,下同),属于非电解质是_____ 。
(2)常温下,② ⑦ ⑧这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应____ (填“是”或“不是”)氧化还原反应。
(3)写出④和⑧分别在水溶液中的电离方程式。______________________________________ 、_____________________________________
(1)上述物质中属于电解质的是
(2)常温下,② ⑦ ⑧这三种物质相互作用可生成一种新物质Ca(HCO3)2,该反应
(3)写出④和⑧分别在水溶液中的电离方程式。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(一)3.01×1023个OH﹣的物质的量为________ ,含有电子的物质的量为________ ,这些OH﹣和________ g 的Na+含有的电子数相同。
(二)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣ , 测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1, 则c(SO42﹣)=________ 。
(三))在标准状况下,8.96L的XH3气体含有a个氢原子,则阿伏加德罗常数可表示为________ (用含a的式子表示);若其质量为13.6g,则X的相对原子质量为________
(四)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)请将上述化学方程式改写为离子方程式:_____________________________________ 。
(2)浓盐酸在反应中显示出来的性质是________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是________ (填化学式),还原性Cl-_____ Mn2+(填>、<或=)。
(4)用双线桥法表示该反应电子转移的方向和数目:_______________________________________ 。
(二)某盐混合溶液中含有离子:Na+、Mg2+、Cl﹣、SO42﹣ , 测得Na+、Mg2+和Cl﹣的物质的量浓度依次为:0.2mol•L﹣1、0.25mol•L﹣1、0.4mol•L﹣1, 则c(SO42﹣)=
(三))在标准状况下,8.96L的XH3气体含有a个氢原子,则阿伏加德罗常数可表示为
(四)实验室可用KMnO4和浓盐酸反应制取氯气。其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)请将上述化学方程式改写为离子方程式:
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)此反应中氧化产物是
(4)用双线桥法表示该反应电子转移的方向和数目:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原是常见的反应类型,根据信息回答以下问题:
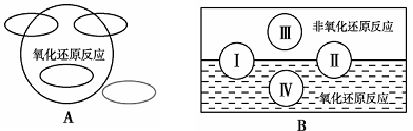
1、A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:Cl2+ 2NaBr = 2NaCl + Br2 所属的区域_____________ 。
2、“四种基本反应类型与氧化还原反应的关系”也可用B图表达。①其中Ⅰ为化合反应,则Ⅱ为___________________ 反应。②写出一个有水生成的符合反应类型Ⅲ的化学方程式:__________________ 。③写出一个有水参加的符合反应类型Ⅳ的化学方程式________________________________ ,其中水作为_____________ 剂。(填氧化剂、还原剂等)
3、用“单线桥”分析下列氧化还原反应的电子转移方向及数目,并填空。
(1)2HClO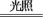 2HCl + O2↑
2HCl + O2↑_____ 氧化产物_____ 被还原的元素_______
(2)2NaCl + 2H2O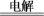 2NaOH + Cl2↑ + H2↑
2NaOH + Cl2↑ + H2↑_____
4、有F-、Cl-、I-、Br2、I2五种粒子,其中氧化性最强的是_______ ,还原性最强的是____ ,用离子方程式表示氧化性强弱的事实:____________________________________ 。

1、A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:Cl2+ 2NaBr = 2NaCl + Br2 所属的区域
2、“四种基本反应类型与氧化还原反应的关系”也可用B图表达。①其中Ⅰ为化合反应,则Ⅱ为
3、用“单线桥”分析下列氧化还原反应的电子转移方向及数目,并填空。
(1)2HClO
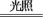 2HCl + O2↑
2HCl + O2↑(2)2NaCl + 2H2O
 2NaOH + Cl2↑ + H2↑
2NaOH + Cl2↑ + H2↑4、有F-、Cl-、I-、Br2、I2五种粒子,其中氧化性最强的是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ. (主要指
(主要指 和
和 )是大气主要污染物之一、有效去除大气中的
)是大气主要污染物之一、有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)在催化剂作用下, 可与
可与 发生如下反应:
发生如下反应: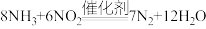
①该反应的氧化剂是___________ (填化学式)。
②用双线桥表示该反应中电子转移的方向和数目___________ 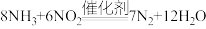
(2)已知 具有氧化性,能够和氨气反应,产物中含有两种单质,请写出在加热条件下
具有氧化性,能够和氨气反应,产物中含有两种单质,请写出在加热条件下 和
和 反应的化学方程式
反应的化学方程式___________ 。
Ⅱ.二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备 的反应原理:
的反应原理: 。
。
(3)①该反应中,被氧化与被还原的氯原子之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为
___________ (填“>”“<”或“=”) 。
。
② 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中,可将
除去,下列试剂中,可将 转化为
转化为 的是
的是___________ (填字母)。
A. B.
B. C.
C. D.
D.
③在一定条件下, 和
和 可发生如下反应:
可发生如下反应: ,由以上反应可知在上述过程中
,由以上反应可知在上述过程中 被
被___________ (填“氧化”或“还原”) 中元素R的化合价是
中元素R的化合价是___________ 。
 (主要指
(主要指 和
和 )是大气主要污染物之一、有效去除大气中的
)是大气主要污染物之一、有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。(1)在催化剂作用下,
 可与
可与 发生如下反应:
发生如下反应: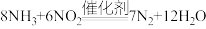
①该反应的氧化剂是
②用双线桥表示该反应中电子转移的方向和数目
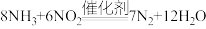
(2)已知
 具有氧化性,能够和氨气反应,产物中含有两种单质,请写出在加热条件下
具有氧化性,能够和氨气反应,产物中含有两种单质,请写出在加热条件下 和
和 反应的化学方程式
反应的化学方程式Ⅱ.二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备
 的反应原理:
的反应原理: 。
。(3)①该反应中,被氧化与被还原的氯原子之比为

 。
。②
 在杀菌消毒过程中会产生副产物亚氯酸盐(
在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为
),需将其转化为 除去,下列试剂中,可将
除去,下列试剂中,可将 转化为
转化为 的是
的是A.
 B.
B. C.
C. D.
D.
③在一定条件下,
 和
和 可发生如下反应:
可发生如下反应: ,由以上反应可知在上述过程中
,由以上反应可知在上述过程中 被
被 中元素R的化合价是
中元素R的化合价是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有 Fe2+ ,故现榨的苹果汁在空气中会发生由淡绿色的Fe2+变为棕黄色的Fe3+的变色过程。上述变色过程中Fe2+__ (填“被氧化”或“被还原”)。若在榨汁加入适量的维生素C,则可有效防止这种现象的发生。这说明维生素 C 具有______ (填字母代号)。
a.氧化性 b.还原性 c.酸性 d.碱性
(2)某学生实验要使用 450mL0.1mol/L 的 CuSO4溶液,需称取______ gCuSO4·5H2O行精确配制,配制过程除了托盘天平、玻璃棒、烧杯、胶头滴管、试剂瓶,还需要用到的玻璃仪器为______ 。
(3)NO2与水反应,标准状况下,67.2L NO2与水反应,转移电子____ mol。
a.氧化性 b.还原性 c.酸性 d.碱性
(2)某学生实验要使用 450mL0.1mol/L 的 CuSO4溶液,需称取
(3)NO2与水反应,标准状况下,67.2L NO2与水反应,转移电子
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“价一类”二维图是预测物质性质的重要思维工具。如图是硫元素的常见化合价与部分物质类别的对应关系:
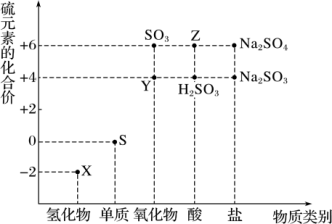
(已知:氢化物是氢与其他元素形成的二元化合物,命名为某化氢)
(1)图中X、Y、Z三种物质中,属于电解质的是_______ 、_______ (用化学式表示)。
(2)Na2SO4的电离方程式为_______ 。
(3)硫代硫酸钠(Na2S2O3)俗称海波。从类别的角度分析,其属于_______ (填标号)。
A.盐 B.碱 C.酸 D.氧化物
从价态的角度分析,Na2S2O3_______ (填标号)
A.只有氧化性 B.既有氧化性又有还原性 C.只有还原性
(4)从物质的性质角度分析,Y不可用_______ (填标号)进行干燥。
A.浓硫酸 B.碱石灰 C.P2O5固体
(5)写出Y通过化合反应一步生成Z的化学方程式:_______ 。

(已知:氢化物是氢与其他元素形成的二元化合物,命名为某化氢)
(1)图中X、Y、Z三种物质中,属于电解质的是
(2)Na2SO4的电离方程式为
(3)硫代硫酸钠(Na2S2O3)俗称海波。从类别的角度分析,其属于
A.盐 B.碱 C.酸 D.氧化物
从价态的角度分析,Na2S2O3
A.只有氧化性 B.既有氧化性又有还原性 C.只有还原性
(4)从物质的性质角度分析,Y不可用
A.浓硫酸 B.碱石灰 C.P2O5固体
(5)写出Y通过化合反应一步生成Z的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有NO等氮氧化物的尾气,反应方程式如下:NaClO + NO + H2O —— NaCl + HNO3 (未配平)。完成下列填空。
(1)氯在元素周期表中的位置是______________________________ ,其所在主族的元素中,最高价氧化物对应的水化物酸性最强的是_______________ (填化学式)。
(2)配平上述反应方程式_______ 。
每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为____________ L。
(3)NaClO溶液中存在如下关系:c(OH-)_____ c(HClO)(填“>”、“=”、或“<”)。
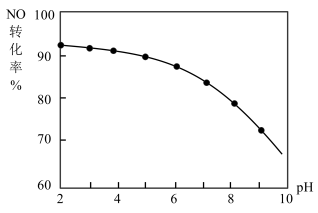
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。
(4)NaClO溶液的初始pH越大,NO的转化率越________________ (填“高”或“低”),其原因是_____________________ 。取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
(5)取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
请将表格填写完整。
(1)氯在元素周期表中的位置是
(2)配平上述反应方程式
每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为
(3)NaClO溶液中存在如下关系:c(OH-)
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。

(4)NaClO溶液的初始pH越大,NO的转化率越
(5)取少量NaClO溶液和KClO3溶液,分别置于A试管和B试管,滴加试剂,观察现象,记录于下表。
请将表格填写完整。
滴加KI溶液 | 再滴加CCl4,振荡、静置 | 结论 | |
A试管 | 溶液变为棕黄色 | 溶液分层,下层显 | 氧化性强弱:(填“>”或“<”) KClO3 |
B试管 | 无现象 | 溶液分层,均无色 |
您最近半年使用:0次



