名校
1 . 已知: ,某MOFs多孔材料孔径大小和形状恰好将
,某MOFs多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
“固定”,能高选择性吸附 。废气中的
。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。
 ,某MOFs多孔材料孔径大小和形状恰好将
,某MOFs多孔材料孔径大小和形状恰好将 “固定”,能高选择性吸附
“固定”,能高选择性吸附 。废气中的
。废气中的 被吸附后,经处理能全部转化为
被吸附后,经处理能全部转化为 。原理示意图如下。
。原理示意图如下。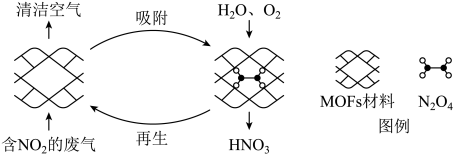
A.废气中的 如果不处理直接排放到空气中会形成酸雨,酸雨的pH值小于5.6 如果不处理直接排放到空气中会形成酸雨,酸雨的pH值小于5.6 |
B.含 的废气进入MOFs多孔材料被吸附后生成 的废气进入MOFs多孔材料被吸附后生成 “固定”,促进 “固定”,促进 的吸收 的吸收 |
C.转化为 的反应是 的反应是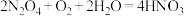 |
D.每获得0.4mol  时,转移电子的数目为 时,转移电子的数目为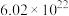 |
您最近半年使用:0次
名校
解题方法
2 . 二氧化硫是最常见、最简单、有刺激性的硫氧化物,大气主要污染物之一,火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。SO2在生活、生产中有重要用途,使用不当会造成环境污染。
(1)某同学利用如图所示装置研究二氧化硫的性质。___________ ,加入药品前需要___________ 。
②实验开始前先通入一段时间N2,此操作的目的是___________ 。
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有___________ 性。
④装置c中的溶液___________ (填能或不能)用澄清石灰水替换,理由是___________ 。
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。___________ 。该空气中二氧化硫的体积分数为___________ 。
(1)某同学利用如图所示装置研究二氧化硫的性质。

②实验开始前先通入一段时间N2,此操作的目的是
③装有Na2S溶液的球形干燥管中出现淡黄色浑浊,说明二氧化硫具有
④装置c中的溶液
(2)某兴趣小组用如图所示装置测定某硫酸厂附近空气中二氧化硫的含量。

您最近半年使用:0次
名校
解题方法
3 . V2O5(五氧化二钒)可作化学工业中的催化剂。为回收利用含钒催化剂,研制了一种利用废催化剂(含有V2O5、VOSO4、不溶性硅酸盐)回收V2O5的新工艺流程如下:
②部分含钒物质常温下在水中的溶解性如表所示:
③ +2OH-
+2OH-
 +H2O
+H2O
回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为___________ 。
(2)在第Ⅱ步中需要加入氨水,请结合 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为___________ 。
(3)需在流动空气中加热NH4VO3的原因可能是___________ 。
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为___________ (保留4位有效数字)。(已知:I2+2 Na2S2O3= Na2S4O6+2NaI,写出计算过程)

②部分含钒物质常温下在水中的溶解性如表所示:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
 +2OH-
+2OH-
 +H2O
+H2O回答下列问题:
(1)在滤渣1中加入Na2SO3和过量H2SO4溶液发生反应生成VOSO4的化学方程式为
(2)在第Ⅱ步中需要加入氨水,请结合
 +2OH-
+2OH-
 +H2O,用平衡移动原理解释加入氨水的作用为
+H2O,用平衡移动原理解释加入氨水的作用为(3)需在流动空气中加热NH4VO3的原因可能是
(4)将0.250g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中的还原产物为V3+离子,滴加指示剂,用0.250mol/LNa2S2O3溶液滴定,达到终点时消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为
您最近半年使用:0次
名校
4 . 4NH3+5O2 4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
 4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是A.中子数为10的氧原子: |
| B.沸点:PH3>NH3 |
| C.4molNH3完全反应,转移5mol电子 |
| D.该反应为复分解反应 |
您最近半年使用:0次
解题方法
5 . 已知:将 通入适量的浓
通入适量的浓 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入浓
通入浓 溶液的产物中可能有
溶液的产物中可能有 、
、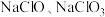 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的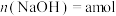 时,下列说法错误的是
时,下列说法错误的是
 通入适量的浓
通入适量的浓 溶液中,反应会放热,当温度升高后会发生如下反应:
溶液中,反应会放热,当温度升高后会发生如下反应: 。则
。则 通入浓
通入浓 溶液的产物中可能有
溶液的产物中可能有 、
、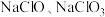 中的两种或三种,且
中的两种或三种,且 的值与温度高低有关。当参与反应的
的值与温度高低有关。当参与反应的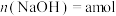 时,下列说法错误的是
时,下列说法错误的是A.与碱的反应中, 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
B.参加反应的 物质的量为 物质的量为 |
C.若某温度下,反应后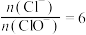 ,则溶液中 ,则溶液中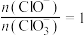 |
D.改变温度,反应中转移电子的物质的量可能为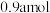 |
您最近半年使用:0次
6 . Ⅰ.某无色透明溶液中可能大量存在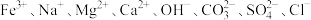 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。
(1)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
Ⅱ.次磷酸 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。
(2)写出白磷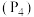 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:_______ ,反应中每消耗 ,转移的电子数为
,转移的电子数为_______ 。
(3)写出 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)工业上利用 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为_______ 。
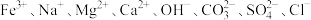 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。(1)根据上述实验现象可知,原溶液中一定存在的离子是
Ⅱ.次磷酸
 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。(2)写出白磷
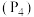 与
与 溶液反应的化学方程式:
溶液反应的化学方程式: ,转移的电子数为
,转移的电子数为(3)写出
 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(4)工业上利用
 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为
您最近半年使用:0次
7 . 铅与碳是同族元素,有 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是
 两种价态,铅的氧化物均难溶于水,已知有下列两个反应:①
两种价态,铅的氧化物均难溶于水,已知有下列两个反应:① ;②
;② 。下列有关叙述不正确的是
。下列有关叙述不正确的是A. 可写成 可写成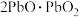 的形式 的形式 |
B.反应②中 是氧化产物 是氧化产物 |
C.生成相同质量的 ,反应①②转移电子数之比为 ,反应①②转移电子数之比为 |
D.根据反应可推测在题给条件下氧化性: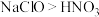 |
您最近半年使用:0次
8 . 工业上,接触法制备硫酸的原理如下:
① ;②
;②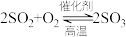 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。
设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
①
 ;②
;②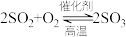 ;③
;③ 的浓硫酸吸收。
的浓硫酸吸收。设
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.①中每生成 时转移电子数为 时转移电子数为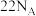 |
B.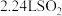 含原子数为 含原子数为 |
C.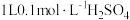 溶液含氧原子总数为 溶液含氧原子总数为 |
D.②中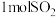 和 和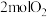 反应生成的 反应生成的 分子数为 分子数为 |
您最近半年使用:0次
9 . 工业上,可用纯碱溶液吸收硝酸厂排放的尾气中的 ,并实现资源再利用。有关反应如下:
,并实现资源再利用。有关反应如下:
①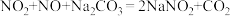
②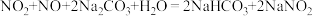
③
下列叙述正确的是
 ,并实现资源再利用。有关反应如下:
,并实现资源再利用。有关反应如下:①
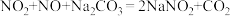
②
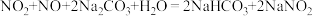
③

下列叙述正确的是
A.常温下溶解度: |
B. 和 和 的混合气体一定能被 的混合气体一定能被 溶液完全吸收 溶液完全吸收 |
C.用澄清石灰水可以区分 和 和 溶液 溶液 |
D.①、②、③中氧化剂与还原剂的物质的量之比均为 |
您最近半年使用:0次
名校
解题方法
10 . 以硫铁矿(主要成分为 ,还有少量
,还有少量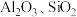 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如图所示,下列说法错误的是
的工艺流程如图所示,下列说法错误的是
 ,还有少量
,还有少量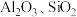 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体 的工艺流程如图所示,下列说法错误的是
的工艺流程如图所示,下列说法错误的是
A.滤渣X的成分为 |
B.“焙烧”硫铁矿的主要反应中,还原剂与氧化剂的物质的量之比为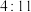 |
| C.“过滤”中分离操作所用的玻璃仪器有(普通)漏斗、玻璃棒和烧杯 |
D.“还原”中试剂Y可能为 |
您最近半年使用:0次



