名校
解题方法
1 . 足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况) 与NO的混合气体,这些气体与一定体积的
与NO的混合气体,这些气体与一定体积的 混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入
混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入 溶液,
溶液, 恰好沉淀完全。下列说法正确的是
恰好沉淀完全。下列说法正确的是
 与NO的混合气体,这些气体与一定体积的
与NO的混合气体,这些气体与一定体积的 混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入
混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入 溶液,
溶液, 恰好沉淀完全。下列说法正确的是
恰好沉淀完全。下列说法正确的是| A.此反应过程中转移了0.5mol的电子 |
| B.消耗氧气的体积为1.12L(标准状况) |
C.参加反应的 是0.6mol 是0.6mol |
D.混合气体中含 (标准状况) (标准状况) |
您最近半年使用:0次
2 . 下列反应的离子方程式表示正确的是
A.向 溶液中加入足量 溶液中加入足量 粉,溶液颜色逐渐消失: 粉,溶液颜色逐渐消失: |
B.向 溶液中通入 溶液中通入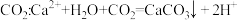 |
C. 与稀硝酸反应: 与稀硝酸反应: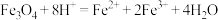 |
D.碳酸氢钠溶液与少量石灰水反应: |
您最近半年使用:0次
2024高三·全国·专题练习
3 . 含氮化合物(NOx、NO 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。___________ 。用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程式为___________ 。
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图:___________ 。酸化废水与铁粉反应的离子方程式是___________ 。
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是___________ 。
 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
已知:3Fe2++ +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。
(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、___________ 。
(5)加入稀硫酸的作用是___________ 。
(6)水样中NO 的含量为
的含量为___________ mol·L-1(用含c1、c2、V1、V2、V的代数式表示)。
 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。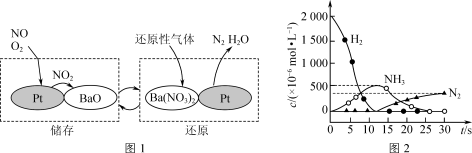
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图: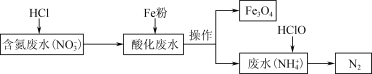
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除
 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。已知:3Fe2++
 +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、
(5)加入稀硫酸的作用是
(6)水样中NO
 的含量为
的含量为
您最近半年使用:0次
名校
4 . 下列各组中的两种物质作用时,反应条件温度、反应物用量、反应物浓度等改变,不会引起产物改变的是
A.S和 | B.NaOH和 | C.Na和 | D.Cu和 |
您最近半年使用:0次
解题方法
5 . 能正确表示下列反应的离子方程式是
A.氢氧化钡溶液与稀硫酸:H++ +Ba2++OH-=BaSO4+H2O +Ba2++OH-=BaSO4+H2O |
B.氯气与水反应:Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
C.已经通入了过量CO2后的石灰水与过量的NaOH溶液反应:Ca2++2 +2OH-=CaCO3 +2OH-=CaCO3 +2H2O+ +2H2O+ |
D.稀硝酸与过量的铁屑反应:Fe+4H++ =Fe3++2NO =Fe3++2NO +2H2O +2H2O |
您最近半年使用:0次
6 . 某同学研究浓硝酸的氧化性,做了如下实验:
资料:
i. 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。
ii. 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式______ 。
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了 ,其理论依据是
,其理论依据是______ 。
甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ: 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了______ (填化学式)。推测红棕色气体是______ (填化学式)。
(4)研究 的转化产物:
的转化产物:
实验Ⅳ:
a.将实验Ⅲ 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。
溶液,不褪色。
c.另取少量实验Ⅲ中反应后的溶液,加入 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。
①通过 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是______ 。
② 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是______ 。
③由上述实验现象可知: 转化的最终产物中一定有
转化的最终产物中一定有______ 。
序号 | 实验Ⅰ | 实验Ⅱ |
操作 | 1:2 | 1:2 |
实验现象 | 铜片迅速溶解,产生大量红棕色气体,溶液变成绿色 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色。 |
i.
 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。ii.
 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了
 ,其理论依据是
,其理论依据是甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ:
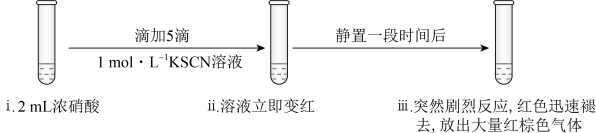
 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了(4)研究
 的转化产物:
的转化产物:实验Ⅳ:
a.将实验Ⅲ
 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。
溶液,不褪色。c.另取少量实验Ⅲ中反应后的溶液,加入
 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。①通过
 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是②
 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是③由上述实验现象可知:
 转化的最终产物中一定有
转化的最终产物中一定有
您最近半年使用:0次
名校
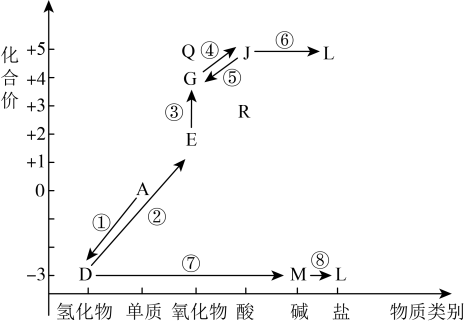
7 . 从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法.以下是氮元素形成物质的价类二维图及氮的循环的部分信息.____________ 。
(2) 与J的浓溶液反应的化学方程式是:
与J的浓溶液反应的化学方程式是:______________ ,该反应实验现象为:___________________ 。
(3)D在一定条件下可以将G转化为对环境无害的物质,请写出相关方程式:__________ ,请写出D的另一种用途___________________ 。
(4)L在水体中过多蓄积会导致水体富营养化.将水体调节为酸性后加入适量 ,可将L中的阳离子转化为无污染气体后去除.写出L与
,可将L中的阳离子转化为无污染气体后去除.写出L与 反应的离子方程式:
反应的离子方程式:__________ 。
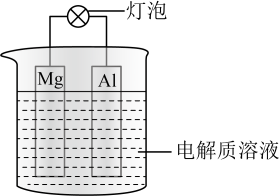
(5)如图所示装置可构成原电池.试回答下列问题: 电极反应式为:
电极反应式为:________________ ;
②电解质溶液为 溶液时,灯泡发亮,则
溶液时,灯泡发亮,则 电极反应式为:
电极反应式为:________________ 。
(2)
 与J的浓溶液反应的化学方程式是:
与J的浓溶液反应的化学方程式是:(3)D在一定条件下可以将G转化为对环境无害的物质,请写出相关方程式:
(4)L在水体中过多蓄积会导致水体富营养化.将水体调节为酸性后加入适量
 ,可将L中的阳离子转化为无污染气体后去除.写出L与
,可将L中的阳离子转化为无污染气体后去除.写出L与 反应的离子方程式:
反应的离子方程式:(5)如图所示装置可构成原电池.试回答下列问题:
 电极反应式为:
电极反应式为:②电解质溶液为
 溶液时,灯泡发亮,则
溶液时,灯泡发亮,则 电极反应式为:
电极反应式为:
您最近半年使用:0次
名校
解题方法
8 . 下列解释事实的方程式不正确的是
A.打磨过的镁条放入沸水中: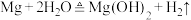 |
B.碳酸亚铁溶于足量稀硝酸: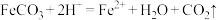 |
C.浓硝酸用棕色瓶装: |
D.打磨过的铝片与 溶液反应产生气体: 溶液反应产生气体: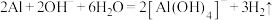 |
您最近半年使用:0次
名校
解题方法
9 . 下列说法正确的是
A.过量的 使紫色石蕊试液先变红后褪色,说明 使紫色石蕊试液先变红后褪色,说明 具有酸性和漂白性 具有酸性和漂白性 |
| B.浓硝酸在光照下颜色变黄,说明浓硝酸具有不稳定性 |
| C.向金属铜与浓硫酸反应后混合液中直接加入蒸馏水,变蓝色证明混合液中含有铜离子 |
| D.纯锌与稀硫酸反应制氢气比粗锌慢,因为粗锌中含有比锌稳定的金属杂质使锌作正极 |
您最近半年使用:0次
名校
解题方法
10 . 对于下列事实的解释错误的是
| A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B.浓硫酸能够干燥氯气、氢气等气体,说明浓硫酸具有吸水性 |
| C.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不及应 |
| D.汽车尾气中排放的氮氧化物主要是由游离态氮转化来的 |
您最近半年使用:0次



