解题方法
1 . 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用生成1mol氧气所转移的电子数为___________ 。
(3)次氯酸钠氧化法___________ 。
②副产品的成分为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法
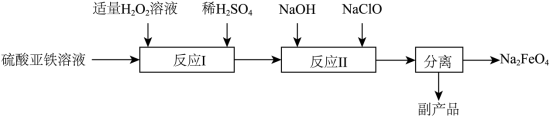
②副产品的成分为
您最近半年使用:0次
名校
解题方法
2 . 工业废水中的氨氮(以 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。
(1)微生物法:酸性废水中的部分 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。
① 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
② 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为_______ 。
(2)次氯酸钠氧化法:向氨氮废水中加入 ,氨氮转化为
,氨氮转化为 而除去。
而除去。
① 氧化
氧化 的离子方程式为
的离子方程式为_______ 。
②一定 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。 :
: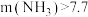 时,总氮的去除率随
时,总氮的去除率随 :
: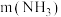 的增大不升反降的原因是
的增大不升反降的原因是_______ 。
(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,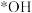 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。_______ 。
②其它条件不变调节废水的 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是_______ 。 晶体进行纯度测定:
晶体进行纯度测定:
a.称取 样品,将其配成
样品,将其配成 溶液。
溶液。
b.先向锥形瓶内加入一定浓度的 溶液,加热至
溶液,加热至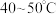 。冷却后再向其中加入
。冷却后再向其中加入
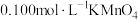 溶液,充分混合。
溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液 。
。
(NaNO2与 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)
通过计算,该样品中 的质量分数是
的质量分数是_______ 。(写出计算过程)
 形式存在),可通过微生物法或氧化法处理,转化为
形式存在),可通过微生物法或氧化法处理,转化为 ,使水中氨氮达到国家规定的排放标准。
,使水中氨氮达到国家规定的排放标准。(1)微生物法:酸性废水中的部分
 在硝化细菌的作用下被氧气氧化为
在硝化细菌的作用下被氧气氧化为 或
或 或
或 再与
再与 作用生成
作用生成 。
。①
 转化为
转化为 的离子方程式为
的离子方程式为②
 与
与 在转化为
在转化为 的反应中消耗
的反应中消耗 与
与 的物质的量之比为
的物质的量之比为(2)次氯酸钠氧化法:向氨氮废水中加入
 ,氨氮转化为
,氨氮转化为 而除去。
而除去。①
 氧化
氧化 的离子方程式为
的离子方程式为②一定
 下,
下, 的投加量对污水中氨氮去除率的影响如图所示。
的投加量对污水中氨氮去除率的影响如图所示。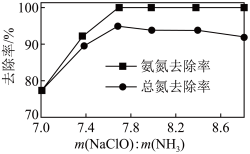
 :
: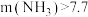 时,总氮的去除率随
时,总氮的去除率随 :
: 的增大不升反降的原因是
的增大不升反降的原因是(3)活性炭-臭氧氧化法:活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,
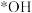 为羟基自由基,其氧化性比
为羟基自由基,其氧化性比 更强。
更强。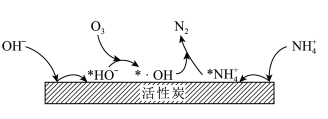
②其它条件不变调节废水的
 ,废水中氨氮去除率随
,废水中氨氮去除率随 的变化如下图所示。随
的变化如下图所示。随 增大氨氮去除率先明显增大,后变化较小,可能的原因是
增大氨氮去除率先明显增大,后变化较小,可能的原因是
 晶体进行纯度测定:
晶体进行纯度测定:a.称取
 样品,将其配成
样品,将其配成 溶液。
溶液。b.先向锥形瓶内加入一定浓度的
 溶液,加热至
溶液,加热至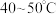 。冷却后再向其中加入
。冷却后再向其中加入
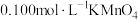 溶液,充分混合。
溶液,充分混合。c.最后用待测的样品溶液与之恰好完全反应,消耗样品溶液
 。
。(NaNO2与
 反应的关系式为:2KMnO4~5NaNO2)
反应的关系式为:2KMnO4~5NaNO2)通过计算,该样品中
 的质量分数是
的质量分数是
您最近半年使用:0次
3 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:___________ 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
4 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。 的一种制备方法如下图所示:
的一种制备方法如下图所示: 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 的一种制备方法如下图所示:
的一种制备方法如下图所示:
 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
5 . 草酸钻可用于指示剂和催化剂。工业上用水钻矿(主要成分为 ,含少量
,含少量 、
、 、MnO、MgO、CaO、
、MnO、MgO、CaO、 等)制取
等)制取 的工艺流程如图所示:
的工艺流程如图所示: 、
、 、
、 、
、 、
、 、
、 、
、 等;
等;
②酸性条件下, 不会氧化
不会氧化 ,
,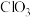 转化为
转化为 ;
;
③部分阳离子的氢氧化物沉淀时溶液的pH如下表:
(1)浸出过程中加入 的主要目的是
的主要目的是_______ , 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(2)向浸出液中加入 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
 ,含少量
,含少量 、
、 、MnO、MgO、CaO、
、MnO、MgO、CaO、 等)制取
等)制取 的工艺流程如图所示:
的工艺流程如图所示: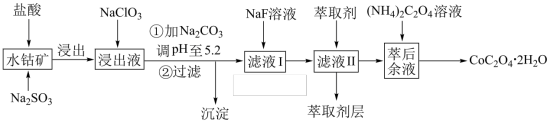
 、
、 、
、 、
、 、
、 、
、 、
、 等;
等;②酸性条件下,
 不会氧化
不会氧化 ,
,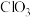 转化为
转化为 ;
;③部分阳离子的氢氧化物沉淀时溶液的pH如下表:
| 沉淀物 |  |  |  |  |  |
| 开始沉淀 | 2.7 | 7.6 | 4.0 | 7.6 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 5.2 | 9.2 | 9.8 |
 的主要目的是
的主要目的是 发生反应的离子方程式为
发生反应的离子方程式为(2)向浸出液中加入
 发生反应的离子方程式为
发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
6 . 锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为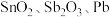 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体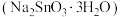 的工艺流程如下:
的工艺流程如下:
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ 。
(2)“高温真空蒸发”控制温度在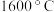 左右,目的是
左右,目的是___________ 。
(3)“高温碱熔”时,单质 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(4)已知“溶浸”后溶液中的阴离子主要为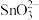 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为___________ 。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、___________ (填试剂名称)洗涤、___________ (填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为___________  。
。
 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为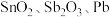 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体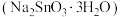 的工艺流程如下:
的工艺流程如下: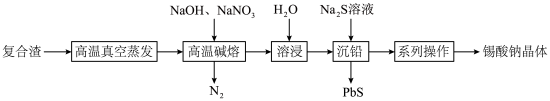
| 物质 |  |  |  |  |
沸点 | 1800 | 2260 | 1550 | 1740 |
回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)“高温真空蒸发”控制温度在
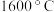 左右,目的是
左右,目的是(3)“高温碱熔”时,单质
 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(4)已知“溶浸”后溶液中的阴离子主要为
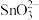 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、
(6)利用焦炭在
 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为 。
。
您最近半年使用:0次
2024-04-19更新
|
187次组卷
|
2卷引用:云南省昆明市2024届高三“三诊一模”教学质量检测(二模)理综-化学试题
7 . 氨的常见氢化物有氨 和肼
和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。
。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。 与水反应可生成
与水反应可生成 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生氢气。
、K)反应产生氢气。 中一个H被
中一个H被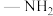 取代,可得
取代,可得 。尿素
。尿素 、
、 和
和 溶液一起反应可制得
溶液一起反应可制得 。下列化学反应表示正确的是
。下列化学反应表示正确的是
 和肼
和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。
。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。 与水反应可生成
与水反应可生成 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生氢气。
、K)反应产生氢气。 中一个H被
中一个H被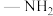 取代,可得
取代,可得 。尿素
。尿素 、
、 和
和 溶液一起反应可制得
溶液一起反应可制得 。下列化学反应表示正确的是
。下列化学反应表示正确的是A.金属钠和液氨反应: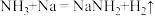 |
B.过量氨水和 反应: 反应: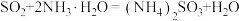 |
C. 与水反应可生成 与水反应可生成 : :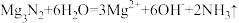 |
D.尿素、 和 和 溶液制得 溶液制得 : : |
您最近半年使用:0次
解题方法
8 . 在催化剂作用下,肼蒸气受热可分解生成N2和一种能使湿润红色石蕊试纸变蓝的气体。写出该反应的化学方程式:_____________ 。
您最近半年使用:0次
解题方法
9 . 三氯化锑( )用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
)用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有 、
、 、
、 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图: 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;
②常温下, 、
、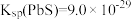 ;
;
③溶液中离子浓度小于或等于 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。
回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有___________ (填一条即可)。
(2)“滤渣1”的主要成分有___________ (写化学式)。
(3)“浸出液”中加入适量 的目的是
的目的是___________ (填化学方程式)。
(4)当 、
、 共沉淀时,溶液中
共沉淀时,溶液中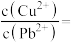
___________ (保留两位有效数字)。
(5)“除砷”时,氧化产物为 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为___________ 。
(6)已知:“电解” 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有___________ 。
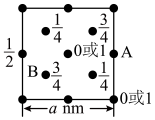
(7) 晶体中
晶体中 原子沿z轴方向在
原子沿z轴方向在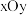 平面的投影图(即俯视图)如图,其中O原子略去,
平面的投影图(即俯视图)如图,其中O原子略去, 原子旁标注的数字表示每个
原子旁标注的数字表示每个 原子位于z轴的高度,则
原子位于z轴的高度,则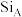 位于晶胞的
位于晶胞的___________ (填“面心”或“棱心”),晶体的密度为___________  。
。
 )用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为
)用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为 ,还含有
,还含有 、
、 、
、 和
和 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
 具有强氧化性,“浸出液”主要含盐酸和
具有强氧化性,“浸出液”主要含盐酸和 ,还含
,还含 、
、 、
、 和
和 等杂质;
等杂质;②常温下,
 、
、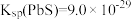 ;
;③溶液中离子浓度小于或等于
 时,认为该离子沉淀完全。
时,认为该离子沉淀完全。回答下列问题:
(1)除将辉锑矿粉碎外,还能加快辉锑矿“酸浸”速率的措施有
(2)“滤渣1”的主要成分有
(3)“浸出液”中加入适量
 的目的是
的目的是(4)当
 、
、 共沉淀时,溶液中
共沉淀时,溶液中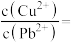
(5)“除砷”时,氧化产物为
 ,则
,则 (可溶于水)与
(可溶于水)与 反应的离子方程式为
反应的离子方程式为(6)已知:“电解”
 溶液时有
溶液时有 生成。则上述流程中可循环利用的物质有
生成。则上述流程中可循环利用的物质有(7)
 晶体中
晶体中 原子沿z轴方向在
原子沿z轴方向在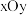 平面的投影图(即俯视图)如图,其中O原子略去,
平面的投影图(即俯视图)如图,其中O原子略去, 原子旁标注的数字表示每个
原子旁标注的数字表示每个 原子位于z轴的高度,则
原子位于z轴的高度,则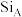 位于晶胞的
位于晶胞的 。
。
您最近半年使用:0次
10 . 选择性催化还原法(SCR)是指在一定温度和催化剂下,适当通入空气,以氨为还原剂,将氮氧化物转化为无毒气体。_____ 。
2.此法仅限于低硫煤烟气脱硝,中高硫煤产生的高浓度二氧化硫会影响脱硝速率,可能的原因是_____ 。

2.此法仅限于低硫煤烟气脱硝,中高硫煤产生的高浓度二氧化硫会影响脱硝速率,可能的原因是
您最近半年使用:0次



