高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用生成1mol氧气所转移的电子数为___________ 。
(3)次氯酸钠氧化法___________ 。
②副产品的成分为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法
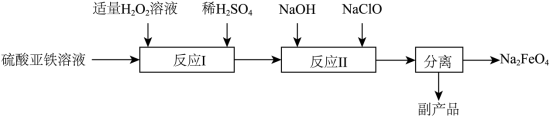
②副产品的成分为
更新时间:2024-04-28 10:39:54
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
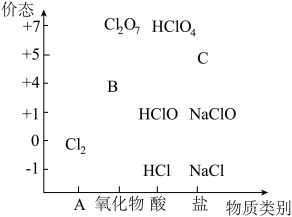
请回答下列问题:
(1)二维图中类别A是_______ ;B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是_______ (填化学式,下同);C的焰色试验呈黄色,则C是_______ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与_______ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_______ 性,可能与(填序号)_______ 发生反应。
(3)实验室常用 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的_______ (填“A”或“B”)作为发生装置,反应的离子方程式为_______ 。

(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。
①该反应说明氧化性:NaClO_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②用单线桥法表示该反应电子转移的方向和数目:________ 。
(5)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为_______ 。

请回答下列问题:
(1)二维图中类别A是
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)实验室常用
 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的
(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。①该反应说明氧化性:NaClO
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②用单线桥法表示该反应电子转移的方向和数目:
(5)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】以黄铜矿[主要成分是二硫化亚铁铜( )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
Ⅰ.火法炼铜: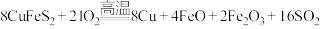
(1)反应中被还原的元素是_______ (填元素符号),氧化产物有_______ (填化学式)。
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为_______ ,冶炼过程中产生大量 ,下列处理方案中合理的是
,下列处理方案中合理的是_______ (填字母)。
A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(3)配平该反应方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______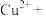 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是_______ 。
 )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。Ⅰ.火法炼铜:
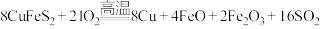
(1)反应中被还原的元素是
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为
 ,下列处理方案中合理的是
,下列处理方案中合理的是A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(3)配平该反应方程式:
_______
 _______
_______ _______
_______ _______
_______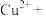 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】某汽车安全气囊的产气药主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
回答下列问题:
(1) 、
、 、
、 、
、 四种物质中,属于氧化物的是
四种物质中,属于氧化物的是___________ 。
(2) 是助氧化剂,其中氯元素的化合价为
是助氧化剂,其中氯元素的化合价为___________ 。
(3) 是主氧化剂,与
是主氧化剂,与 发生置换反应,还原产物为
发生置换反应,还原产物为___________ 。
(4) 是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为___________ 。
(5) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和
和 ,
, 和
和 的物质的量之比为
的物质的量之比为___________ 。
(6) 上述产气药产生的气体通过碱石灰后得到
上述产气药产生的气体通过碱石灰后得到 (标准状况)。
(标准状况)。
①用碱石灰除去的物质为___________ ;
②该产气药中 的质量分数为
的质量分数为___________ 。
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。回答下列问题:
(1)
 、
、 、
、 、
、 四种物质中,属于氧化物的是
四种物质中,属于氧化物的是(2)
 是助氧化剂,其中氯元素的化合价为
是助氧化剂,其中氯元素的化合价为(3)
 是主氧化剂,与
是主氧化剂,与 发生置换反应,还原产物为
发生置换反应,还原产物为(4)
 是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为(5)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和
和 ,
, 和
和 的物质的量之比为
的物质的量之比为(6)
 上述产气药产生的气体通过碱石灰后得到
上述产气药产生的气体通过碱石灰后得到 (标准状况)。
(标准状况)。①用碱石灰除去的物质为
②该产气药中
 的质量分数为
的质量分数为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】SO2在生产、生活中具有重要的作用,据所学知识回答相关问题。
(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有___________ (填“酸性”、“氧化性”、“还原性”或“漂白性”,下同),SO2通入品红溶液中,品红溶液褪色,说明SO2具有___________ 。
(2)已知SO2通入FeCl3溶液会发生反应,还原产物为___________ (填化学式,下同),氧化产物为___________ 。
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4。
①该反应的化学方程式为___________ ,若反应中有0.1mol电子转移,则生成ZnS2O4___________ g。
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为___________ 。
(4)已知室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水。ZnO水悬浊液常用于吸收烟气中的SO2。向ZnO水悬浊液中缓慢匀速通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH的变化如图。0~20min内,溶液pH几乎不变的原因是___________ ,SO2吸收率在30min后迅速降低,其原因是___________ 。

(1) SO2通入Na2CO3溶液中有CO2生成,说明H2SO3具有
(2)已知SO2通入FeCl3溶液会发生反应,还原产物为
(3)向含锌粉的悬浊液中通入SO2可制备ZnS2O4。
①该反应的化学方程式为
②向反应后的溶液中加入过量盐酸,溶液出现黄色浑浊,且有刺激性气体产生,反应的化学方程式为
(4)已知室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水。ZnO水悬浊液常用于吸收烟气中的SO2。向ZnO水悬浊液中缓慢匀速通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH的变化如图。0~20min内,溶液pH几乎不变的原因是

您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在肉制品加工中,常使用来硝酸钠作发色剂,但必须严格控制亚硝酸钠的用量,以确保使用安全。亚硝酸钠也是一种常见的水污染物,在工业废水中亚硝酸盐的含量较高,如不做处理排放在环境中,对人体、水生物有毒害作用。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂__________ 。
(2)写出该反应的化学方程式_____________________________________ ,该反应中,氧化剂和氧化产物的微粒数之比为_____________ ,当有n个氧化产物生成时,转移电子数为____ e-。
(3)HI在上述反应中表现出的性质是____________________ 。
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是_________ 。
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式________________________________________ 。
Ⅰ.某一反应体系中反应物和生成物共六种:NaNO2 、H2O、NO 、I2、NaI、HI。已知该反应中 NaNO2只发生还原反应。
(1)该反应的还原剂
(2)写出该反应的化学方程式
(3)HI在上述反应中表现出的性质是
(4)误食 NaNO2 会导致血红蛋白中 Fe2+转化 Fe3+而中毒,服用维生素 C 可以解除 NaNO2
引起的中毒。下列关于上述中毒、解毒过程的说法中正确的是
A.中毒过程NaNO2 是还原剂 B.解毒过程维生素 C 是还原剂
C.解毒过程,维生素 C 能把 Fe2+氧化 Fe3+ D.中毒时亚硝酸盐发生还原反应
Ⅱ.工业废水中亚硝酸盐的处理这一研究已有很久的历史了,传统常见的方法有离子交换法、反渗透法、电渗析法、生物及反硝化法、化学还原法和化学催化硝化法,其中化学还原法是利用加NH4Cl进行处理含亚硝酸盐的废水,转化为无污染的物质进行排放。
(5)写出该处理方法的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为________ 。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4_______
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:_________________ 。
②若起始时有1 mol P4参加反应,则整个工业流程中共生成________ mol PH3。
II. 、
、 、
、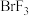 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是__________ 。
(2)溴化碘( )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为_______ ;
(3)已知某些离子的还原性强弱顺序为 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象_________ ;
(1)AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
_______CuSO4+_______PH3+_______H2O=_______Cu3P↓+_______H3PO4+_______H2SO4
(3)工业制备PH3的流程如图所示。

①白磷和烧碱溶液反应的化学方程式为:
②若起始时有1 mol P4参加反应,则整个工业流程中共生成
II.
 、
、 、
、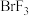 等称之为卤素互化物,
等称之为卤素互化物, 、
、 、
、 等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。
等称之为拟卤素,它们的化学性质与卤素单质相似,请回答下列问题。(1)有一种碘的氧化物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,则这种化合物的化学式是
(2)溴化碘(
 )具有强氧化性,能与
)具有强氧化性,能与 溶液发生反应,发生反应的离子方程式为
溶液发生反应,发生反应的离子方程式为(3)已知某些离子的还原性强弱顺序为
 。现将几滴
。现将几滴 溶液滴入到含少量
溶液滴入到含少量 的溶液中,溶液立即变红,向其中逐滴滴入酸性
的溶液中,溶液立即变红,向其中逐滴滴入酸性 溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
溶液,观察到红色逐渐褪去,请利用平衡移动原理解释这一现象
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 (高铁酸钾,暗紫色)是一种新型绿色氧化剂,既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反应过程为:
(高铁酸钾,暗紫色)是一种新型绿色氧化剂,既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反应过程为:
(1)配平上述方程式:_______ 。
(2)每生成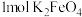 ,转移的电子数目为
,转移的电子数目为_______ 。
(3)取少量 于试管中,加硫酸酸化并堵住试管口,观察到溶液中有细微的小气泡产生,溶液紫色逐渐褪去,伸入一根带火星的木条,木条复燃;再向溶液中加入
于试管中,加硫酸酸化并堵住试管口,观察到溶液中有细微的小气泡产生,溶液紫色逐渐褪去,伸入一根带火星的木条,木条复燃;再向溶液中加入 溶液,溶液变为血红色。则
溶液,溶液变为血红色。则 酸化时发生反应的离子方程式为
酸化时发生反应的离子方程式为_______ 。
 (高铁酸钾,暗紫色)是一种新型绿色氧化剂,既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反应过程为:
(高铁酸钾,暗紫色)是一种新型绿色氧化剂,既能杀菌消毒、又能絮凝净水的水处理剂。其工业制备反应过程为:
(1)配平上述方程式:
(2)每生成
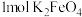 ,转移的电子数目为
,转移的电子数目为(3)取少量
 于试管中,加硫酸酸化并堵住试管口,观察到溶液中有细微的小气泡产生,溶液紫色逐渐褪去,伸入一根带火星的木条,木条复燃;再向溶液中加入
于试管中,加硫酸酸化并堵住试管口,观察到溶液中有细微的小气泡产生,溶液紫色逐渐褪去,伸入一根带火星的木条,木条复燃;再向溶液中加入 溶液,溶液变为血红色。则
溶液,溶液变为血红色。则 酸化时发生反应的离子方程式为
酸化时发生反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】浩瀚的大海具有丰富的化学资源可以开发和利用,回答下列相关问题:
(1)纯碱是人类最早制取和使用的化学物质之一,其属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。我国化学家侯德榜发明了联合制碱法,制取方法是向饱和食盐水先通入足量 ,再通入过量
,再通入过量 ,得到
,得到_______ (填化学式)晶体,过滤,再由该晶体制得纯碱的化学方程式为_______ 。
(2)日前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,该反应的还原产物为
,该反应的还原产物为_______ ,若制得1mol  ,转移电子的数目为
,转移电子的数目为_______ 。
(3)金属钠可用于生产汽车安全气囊中的气体发生剂 ,某汽车安全气囊中含
,某汽车安全气囊中含 、
、 和
和 等物质。
等物质。
①当汽车发生较严重的碰撞时, 受热分解为Na和
受热分解为Na和 ,其化学方程式为
,其化学方程式为_______ 。
②气囊中产生的Na立即与 反应生成
反应生成 与另一种单质,该反应属于四种基本反向类型中的
与另一种单质,该反应属于四种基本反向类型中的_______ 反应。
(1)纯碱是人类最早制取和使用的化学物质之一,其属于
 ,再通入过量
,再通入过量 ,得到
,得到(2)日前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,该反应的还原产物为
,该反应的还原产物为 ,转移电子的数目为
,转移电子的数目为(3)金属钠可用于生产汽车安全气囊中的气体发生剂
 ,某汽车安全气囊中含
,某汽车安全气囊中含 、
、 和
和 等物质。
等物质。①当汽车发生较严重的碰撞时,
 受热分解为Na和
受热分解为Na和 ,其化学方程式为
,其化学方程式为②气囊中产生的Na立即与
 反应生成
反应生成 与另一种单质,该反应属于四种基本反向类型中的
与另一种单质,该反应属于四种基本反向类型中的
您最近半年使用:0次


 =6,则FexOy的化学式为
=6,则FexOy的化学式为

