以黄铜矿[主要成分是二硫化亚铁铜( )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
Ⅰ.火法炼铜: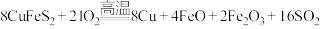
(1)反应中被还原的元素是_______ (填元素符号),氧化产物有_______ (填化学式)。
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为_______ ,冶炼过程中产生大量 ,下列处理方案中合理的是
,下列处理方案中合理的是_______ (填字母)。
A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有 生成。
生成。
(3)配平该反应方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______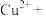 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是_______ 。
 )]为主要原料的炼铜方法有火法炼铜、氧化浸出等。
)]为主要原料的炼铜方法有火法炼铜、氧化浸出等。Ⅰ.火法炼铜:
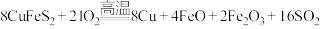
(1)反应中被还原的元素是
(2)用此法炼铜,每制得32t铜会产生污染气体二氧化硫的质量为
 ,下列处理方案中合理的是
,下列处理方案中合理的是A.高空排放 B.制备硫酸 C.用氨水吸收
Ⅱ.氧化浸出:在硫酸介质中用双氧水将黄铜矿氧化,测得有
 生成。
生成。(3)配平该反应方程式:
_______
 _______
_______ _______
_______ _______
_______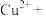 _______
_______ _______
_______ _______
_______
(4)该反应在25~50℃下进行,实际生产中双氧水的消耗量要远远高于理论值,除温度较高双氧水分解之外,还可能的原因是
更新时间:2022-11-06 09:35:22
|
相似题推荐
【推荐1】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(K2FeO4)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH,使高铁酸钾析出。
(1)方法一:
可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的氧化剂是___________ ,每消耗1mol Na2O2转移___________ mol电子。
(2)方法二:
反应:Fe(OH)3+ClO﹣+OH﹣= +Cl﹣+H2O(未配平)
+Cl﹣+H2O(未配平)
①配平离子反应方程式:___________
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为___________ mol。
(3)向Na2FeO4溶液中加入适量饱和的KOH溶液,有K2FeO4析出,请写出该反应的化学方程式:___________ 。
(1)方法一:
可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
该反应中的氧化剂是
(2)方法二:
反应:Fe(OH)3+ClO﹣+OH﹣=
 +Cl﹣+H2O(未配平)
+Cl﹣+H2O(未配平)①配平离子反应方程式:
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为
(3)向Na2FeO4溶液中加入适量饱和的KOH溶液,有K2FeO4析出,请写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列有关氧化还原的问题。
(1)下列微粒:①S② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 。在化学反应中只能被氧化的是
。在化学反应中只能被氧化的是______ (填序号,下同),只能表现出氧化性的是______ 。
(2)将 溶液滴加到酸性
溶液滴加到酸性 溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是
溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是______ ,这样推测的理由是______ 。
(3)自来水中的 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:
①方案a:碱性条件下用 还原
还原 ,产物为
,产物为 。生成1个
。生成1个 分子的同时会生成
分子的同时会生成______ 个 。
。
②方案b:碱性条件下用 粉还原
粉还原 ,产物是
,产物是 发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目______ 。

(4)设计实验验证亚硫酸钠具有还原性。
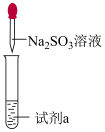
试剂a:______ 现象:______ 。
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
 。试通过计算和推理完成下面的问题:
。试通过计算和推理完成下面的问题:
①A物质可以导致酸雨的形成。A应该属于______ (用字母代号填写)。
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
② 物质可以使酸性
物质可以使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式______ 。此反应中每个 分子
分子______ (填“得到”或“失去”)______ 个电子,发生______ 反应(填“氧化反应”或“还原反应”)。
(1)下列微粒:①S②
 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ 。在化学反应中只能被氧化的是
。在化学反应中只能被氧化的是(2)将
 溶液滴加到酸性
溶液滴加到酸性 溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是
溶液混合,溶液由紫色褪至无色。反应结束后,推测硫元素在反应后的化合价是(3)自来水中的
 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中 的浓度,某研究人员提出两种方案:
的浓度,某研究人员提出两种方案:①方案a:碱性条件下用
 还原
还原 ,产物为
,产物为 。生成1个
。生成1个 分子的同时会生成
分子的同时会生成 。
。②方案b:碱性条件下用
 粉还原
粉还原 ,产物是
,产物是 发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
发生的反应可表示如下,完成方程式配平并用双线桥标出电子转移的方向和数目
(4)设计实验验证亚硫酸钠具有还原性。

试剂a:
(5)已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
 。试通过计算和推理完成下面的问题:
。试通过计算和推理完成下面的问题:①A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
②
 物质可以使酸性
物质可以使酸性 溶液褪色,写出反应的离子方程式
溶液褪色,写出反应的离子方程式 分子
分子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)有下列离子:K+、Na+、 、
、 、
、 、Mg2+、Cl-、Cu2+。
、Mg2+、Cl-、Cu2+。
①在某无色溶液中肯定不能大量存在的离子是______________ 。
②在某酸性溶液中肯定不能大量存在的离子是______________ 。
③在某碱性溶液中肯定不能大量存在的离子是______________ 。
(2)亚硝酸钠(NaNO2)外观酷似食盐,但它是一种有毒的物质。误食亚硝酸钠会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。转化过程可表示为: 。转化1中,氧化剂是
。转化1中,氧化剂是_____ ,转化2中,Fe3+作_____ 剂,维生素C表现_____ 性。
 、
、 、
、 、Mg2+、Cl-、Cu2+。
、Mg2+、Cl-、Cu2+。①在某无色溶液中肯定不能大量存在的离子是
②在某酸性溶液中肯定不能大量存在的离子是
③在某碱性溶液中肯定不能大量存在的离子是
(2)亚硝酸钠(NaNO2)外观酷似食盐,但它是一种有毒的物质。误食亚硝酸钠会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。转化过程可表示为:
 。转化1中,氧化剂是
。转化1中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】针对以下A~D四个涉及H2O2的反应(未配平)填空:
A.
B.
C.
D.
(1)H2O2仅体现氧化性的反应是___________ (填序号,下同),H2O2仅体现还原性的反应是___________ ,H2O2既体现氧化性又体现还原性的反应是___________ ,H2O2既不作氧化剂又不作还原剂的反应是___________ 。
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向和数目:□H2O2+□Cr2(SO4)3+□KOH=□K2CrO4+□K2SO4+□H2O,___________
A.

B.

C.

D.

(1)H2O2仅体现氧化性的反应是
(2)请将D反应配平,并用单线桥标出D反应中电子转移的方向和数目:□H2O2+□Cr2(SO4)3+□KOH=□K2CrO4+□K2SO4+□H2O,
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列十种物质:①铝 ②蔗糖 ③ ④
④ ⑤酒精水溶液 ⑥氢氧化铁胶体 ⑦
⑤酒精水溶液 ⑥氢氧化铁胶体 ⑦ ⑧酸性高锰酸钾溶液 ⑨
⑧酸性高锰酸钾溶液 ⑨  ⑩
⑩
(1)上述物质中属于非电解质的有____ 。(填序号)
(2)⑨在水中的电离方程式为_______ 。
(3)向⑥中逐渐滴加⑦的溶液,看到的现象是_______ 。
(4)上述物质中有两种物质在水溶液中发生反应,其离子方程式可表示为: ,则该反应的化学方程式为
,则该反应的化学方程式为____ 。
(5)二氧化硫通入⑧溶液中,溶液会褪色。写出并配平反应的离子方程式:____ 。
 ④
④ ⑤酒精水溶液 ⑥氢氧化铁胶体 ⑦
⑤酒精水溶液 ⑥氢氧化铁胶体 ⑦ ⑧酸性高锰酸钾溶液 ⑨
⑧酸性高锰酸钾溶液 ⑨  ⑩
⑩
(1)上述物质中属于非电解质的有
(2)⑨在水中的电离方程式为
(3)向⑥中逐渐滴加⑦的溶液,看到的现象是
(4)上述物质中有两种物质在水溶液中发生反应,其离子方程式可表示为:
 ,则该反应的化学方程式为
,则该反应的化学方程式为(5)二氧化硫通入⑧溶液中,溶液会褪色。写出并配平反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(2)工业废水中含有的重铬酸根离子(Cr2O )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是___________ (填离子符号,下同),氧化剂是___________ 。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是___________ (填化学式,下同),氧化剂是___________ 。
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:________
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是___________ (填化学式,下同),被还原的是___________ 。
(1)平常我们食用的水果中含有丰富的维生素C,维生素C又被称为“抗坏血酸”,在人体内有重要的功能,例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(2)工业废水中含有的重铬酸根离子(Cr2O
 )有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O
)有毒,必需处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2+ + Cr2O + 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是
+ 14H+ = 6Fe3+ + 2Cr3+ + 7H2O,在该反应中,还原剂是(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S + 2KNO3 + 3C = K2S + N2↑+ 3CO2↑,在该反应中,还原剂是
(4)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石烙化成团。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)
①请完成上述火法炼锌反应的化学方程式:
ZnCO3 +___________ = ___________ +___________ CO↑。
②在该反应中,还原剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫及其化合物的“价-类”二维图体现了化学变化之美。

(1)自然界中有斜方硫和单斜硫,它们的关系是_______ ,二者转化属于_______ 变化。
(2)如图中属于酸性氧化物的物质是_______ (用化学式表示)。
(3)不同价态的硫元素可以相互转化,请写出以下转化:
①反应前后存在3种价态的硫元素,写出反应的离子方程式_______ ;
②反应前后存在4种价态的硫元素,写出反应的化学方程式_______ 。
(4)如果有反应Z M,H2S
M,H2S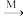 N,M是下列物质中的
N,M是下列物质中的_______ (填字母序号)
a.Na2SO4 b.CuSO4 c.FeSO4 d.Fe2(SO4)3
写出H2S生成N的离子方程式为_______ ;Q可以是_______ (用化学式表示,写出至少3类物质)。

(1)自然界中有斜方硫和单斜硫,它们的关系是
(2)如图中属于酸性氧化物的物质是
(3)不同价态的硫元素可以相互转化,请写出以下转化:
①反应前后存在3种价态的硫元素,写出反应的离子方程式
②反应前后存在4种价态的硫元素,写出反应的化学方程式
(4)如果有反应Z
 M,H2S
M,H2S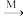 N,M是下列物质中的
N,M是下列物质中的a.Na2SO4 b.CuSO4 c.FeSO4 d.Fe2(SO4)3
写出H2S生成N的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)由5.6gCO、4.4gCO2及0.4gH2组成的混合气体的平均摩尔质量是____________ ;该混合气体相对于O2的密度为_________ ;该混合气体中CO的物质的量分数是__________ 。
(2)焦亚硫酸钠(Na2S2O5)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。Na2S2O5中硫元素的化合价是_________ ,焦亚硫酸钠在空气中久置会被氧化生成连二硫酸钠(Na2S2O6),写出该反应的化学方程式__________________________________________ 。
(3)葡萄酒中的 Na2S2O5的使用量是以游离的 SO2 来计算的。我国规定每升葡萄酒中SO2的最高含量是 0.25g,则一瓶 800mL 的葡萄酒中 SO2的物质的量不能超过______ (精确到 0.001 )。
(2)焦亚硫酸钠(Na2S2O5)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。Na2S2O5中硫元素的化合价是
(3)葡萄酒中的 Na2S2O5的使用量是以游离的 SO2 来计算的。我国规定每升葡萄酒中SO2的最高含量是 0.25g,则一瓶 800mL 的葡萄酒中 SO2的物质的量不能超过
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫、氮、氯其化合物在生产生活中应用广泛。请回答:
(1)将SO2通入品红溶液中,现象为品红溶液___________ ,加热后溶液颜色___________ 。将Cl2和SO2以1:1通入品红中,不能增强漂白性,用化学用语解释原因___________
(2)工业生产漂白粉有关反应的化学方程式:___________
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式___________ 。
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是___________
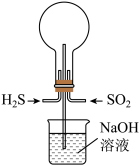
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是___________ 。
(1)将SO2通入品红溶液中,现象为品红溶液
(2)工业生产漂白粉有关反应的化学方程式:
(3)在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式
(4)0.3mol的钠镁铝分别投入100mL 1mol/L的硫酸中,相同条件下产生H2的体积比是
(5)用如图所示装置做实验:常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久烧瓶中能观察到的现象是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】利用 与
与 合成甲醇涉及的主要反应如下:
合成甲醇涉及的主要反应如下:
a.
b.
一定条件下向某刚性容器中充入物质的量之比为1∶3的 和
和 发生上述反应,在不同催化剂(Cat.1,Cat.2)下经相同反应时间,
发生上述反应,在不同催化剂(Cat.1,Cat.2)下经相同反应时间, 的转化率和甲醇的选择性[甲醇的选择性
的转化率和甲醇的选择性[甲醇的选择性 ]随温度的变化如图所示:
]随温度的变化如图所示:

(1)由图可知,催化效果Cat.1____________ (填“>”“<”或“=”)Cat.2。
(2)在 间,
间, 的选择性随温度的升高而下降,可能的原因为
的选择性随温度的升高而下降,可能的原因为________________________ (写出一条即可)。
 与
与 合成甲醇涉及的主要反应如下:
合成甲醇涉及的主要反应如下:a.

b.

一定条件下向某刚性容器中充入物质的量之比为1∶3的
 和
和 发生上述反应,在不同催化剂(Cat.1,Cat.2)下经相同反应时间,
发生上述反应,在不同催化剂(Cat.1,Cat.2)下经相同反应时间, 的转化率和甲醇的选择性[甲醇的选择性
的转化率和甲醇的选择性[甲醇的选择性 ]随温度的变化如图所示:
]随温度的变化如图所示:
(1)由图可知,催化效果Cat.1
(2)在
 间,
间, 的选择性随温度的升高而下降,可能的原因为
的选择性随温度的升高而下降,可能的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
I.将水蒸气通过红热的炭即可产生水煤气。反应为:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
(1)能使化学反应速率加快的措施有________ (填序号)。
①升高反应温度②增加C的物质的量③密闭定容容器中充入CO(g)
II.工业上用CO生产燃料甲醇,一定条件下发生反应CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。

(2)图1是表示一定温度下,在体积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=__________________ ;
(3)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。请结合图象解释催化剂加快化学反应速率的原因_______________________________ ,该反应消耗1molCO时,______ (填“放出”或“吸收”)__________ KJ热量。
I.将水蒸气通过红热的炭即可产生水煤气。反应为:C(s)+H2O(g)
 CO(g)+H2(g)
CO(g)+H2(g)(1)能使化学反应速率加快的措施有
①升高反应温度②增加C的物质的量③密闭定容容器中充入CO(g)
II.工业上用CO生产燃料甲醇,一定条件下发生反应CO(g)+2H2(g)
 CH3OH(g)。
CH3OH(g)。
(2)图1是表示一定温度下,在体积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)=
(3)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。请结合图象解释催化剂加快化学反应速率的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某储氢合金(M)的储氢机理简述如下:合金吸附H2→氢气解离成氢原子→形成含氢固溶体MHx( 相)→形成氢化物MHy(
相)→形成氢化物MHy( 相)。已知:
相)。已知: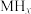 (
( 相)与MHy(
相)与MHy( 相)之间可建立平衡:
相)之间可建立平衡:

请回答下列问题:
(1)上述平衡中化学计量数k=________ (用含x、y的代数式表示)。
(2)t℃时,向体积恒定的密闭容器中加入一定量的储氢合金(M),随充入H2量的改变,固相中氢原子与金属原子个数比(H/M)与容器中H2的平衡压强p的变化关系如图所示。
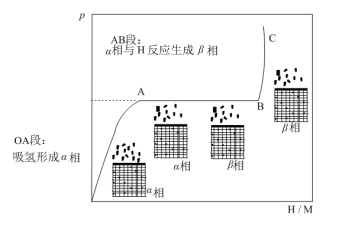
①在________ 温________ 压强下有利于该储氢合金(M)储存H2(填“低”或“高”)。
②若6g该储氢合金(M)在10 s内吸收的H2体积为24 mL,吸氢平均速率v=________ mL/(g∙s)。
③关于该储氢过程的说法错误的是________ 。
a.OA段:其他条件不变时,适当升温能提升形成 相的速率
相的速率
b.AB段:由于H2的平衡压强p未改变,故AB段过程中无H2充入
c.BC段:提升H2压力能大幅提高 相中氢原子物质的量
相中氢原子物质的量
(3)实验表明,H2中常含有O2、CO2、 、H2O等杂质,必须经过净化处理才能被合金储存,原因是
、H2O等杂质,必须经过净化处理才能被合金储存,原因是___________ 。
(4)有资料显示,储氢合金表面氢化物的形成会阻碍储氢合金吸附新的氢气分子,若把储氢合金制成纳米颗粒,单位时间内储氢效率会大幅度提高,可能的原因是________________ 。
(5)某镁系储氢合金的晶体结构如图所示:
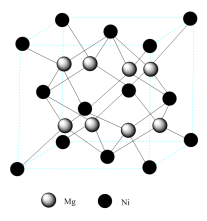
该储氢合金的化学式为________ 。若储氢后每个Mg原子都能结合2个氢原子,则该储氢合金的储氢容量为________ mL/g(储氢容量用每克合金结合标准状况下的氢气体积来表示,结果保留到整数)。
 相)→形成氢化物MHy(
相)→形成氢化物MHy( 相)。已知:
相)。已知: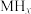 (
( 相)与MHy(
相)与MHy( 相)之间可建立平衡:
相)之间可建立平衡:
请回答下列问题:
(1)上述平衡中化学计量数k=
(2)t℃时,向体积恒定的密闭容器中加入一定量的储氢合金(M),随充入H2量的改变,固相中氢原子与金属原子个数比(H/M)与容器中H2的平衡压强p的变化关系如图所示。

①在
②若6g该储氢合金(M)在10 s内吸收的H2体积为24 mL,吸氢平均速率v=
③关于该储氢过程的说法错误的是
a.OA段:其他条件不变时,适当升温能提升形成
 相的速率
相的速率b.AB段:由于H2的平衡压强p未改变,故AB段过程中无H2充入
c.BC段:提升H2压力能大幅提高
 相中氢原子物质的量
相中氢原子物质的量(3)实验表明,H2中常含有O2、CO2、
 、H2O等杂质,必须经过净化处理才能被合金储存,原因是
、H2O等杂质,必须经过净化处理才能被合金储存,原因是(4)有资料显示,储氢合金表面氢化物的形成会阻碍储氢合金吸附新的氢气分子,若把储氢合金制成纳米颗粒,单位时间内储氢效率会大幅度提高,可能的原因是
(5)某镁系储氢合金的晶体结构如图所示:

该储氢合金的化学式为
您最近一年使用:0次



