1 . 某实验小组探究外界条件对化学反应速率的影响,进行了以下实验。
Ⅰ.探究温度、浓度对硫代硫酸钠与稀硫酸反应速率的影响
(1)写出Na2S2O3与H2SO4反应的离子方程式_______ 。
(2)该小组同学设计了如下表所示系列实验:
①实验①和②目的是探究温度对该反应速率的影响,则实验②中,t1=_______ (填“20℃”或“60℃”)、V2= _______ mL。
②若V4=10.0 V5=6.0,则t2=_______ (填“20℃”或“60℃”),实验①和③的实验目的是_______ 。
Ⅱ.探究催化剂对H2O2分解速率的影响_______ ,为此须用到实验器材为_______ 。
Ⅲ.探究催化剂对H2O2分解速率的影响
(4)若仍用上图中的装置,探究MnO2对H2O2分解的催化作用,则此时注射器中应加入的试剂是_______ ,写出该反应的化学方程式_______ 。
Ⅰ.探究温度、浓度对硫代硫酸钠与稀硫酸反应速率的影响
(1)写出Na2S2O3与H2SO4反应的离子方程式
(2)该小组同学设计了如下表所示系列实验:
实验序号 | 反应温度/℃ | Na2S2O3溶液 | H2SO4稀溶液 | H2O | ||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
② | t1 | V1 | 0.10 | V2 | 0.50 | V3 |
③ | t2 | V4 | 0.10 | V5 | 0.50 | V6 |
②若V4=10.0 V5=6.0,则t2=
Ⅱ.探究催化剂对H2O2分解速率的影响
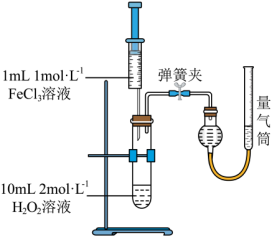
Ⅲ.探究催化剂对H2O2分解速率的影响
(4)若仍用上图中的装置,探究MnO2对H2O2分解的催化作用,则此时注射器中应加入的试剂是
您最近一年使用:0次
2 . 丙酮与碘在盐酸催化下发生取代反应,碘水颜色逐渐褪去生成碘化丙酮(反应及机理如下):

| 组别 |  标准盐酸溶液 标准盐酸溶液 |  标准丙酮溶液 标准丙酮溶液 |  碘水溶液 碘水溶液 | 蒸馏水 |
 |  |  |  | 0 |
 |  |  | 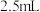 | 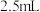 |

A.甲基上的 能与碘发生取代的原因是其受到了羰基官能团的影响 能与碘发生取代的原因是其受到了羰基官能团的影响 |
| B.在反应过程中丙酮的浓度、盐酸的浓度可视为恒定 |
| C.两组实验的碘水取代反应都是匀速反应且两组速率相等 |
| D.综合分析可知总反应速率由反应③决定的 |
您最近一年使用:0次
3 . 在密闭系统中发生反应: ,下列措施不能使反应速率加快的是
,下列措施不能使反应速率加快的是
 ,下列措施不能使反应速率加快的是
,下列措施不能使反应速率加快的是| A.通过减小容器体积增大压强 | B.增加炭的质量 |
| C.升高温度 | D.恒容通入 |
您最近一年使用:0次
23-24高一下·全国·期末
4 . 回答下列问题:
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有______________ (写一种)。
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_______________ 等。
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是________________ 。
(1)用20% H2SO4浸取软锰矿(主要成分为MnO2、SiO2等)制备高纯MnO2,酸浸时,通常加入FeSO4作催化剂加快反应速率。为提高酸浸速率,还可以采取的措施有
(2)工业上用稀硫酸浸取碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)生产锰酸锂(LiMn2O4),为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③
(3)用NaOH熔盐高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)制备白色颜料TiO2,为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是
您最近一年使用:0次
名校
解题方法
5 . 下列方案设计、现象和结论都正确的是
| 选 项 | 目的 | 方案设计 | 现象和结论 |
| A | 比较AgI和AgCl 的Ksp大小 | 向盛有2mL0.1mol/LAgNO3溶液的试管中滴加2滴0.1mol/LNaCl溶液,振荡试管,然后向其中滴加4滴0.1mol/LKI溶液 | 先产生白色沉淀,后产生黄色沉淀,则证明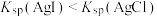 |
| B | 探究化学反应速率的影响因素 | 常温时,在试管A、B中分别加入2mL0.1mol/LNa2S2O3溶液,在A中加入2mL0.1mol/LH2SO4溶液,在B中加入1mL0.1mol/LH2SO4溶液和1mL水 | A试管中先出现浑浊,则证明相同条件下,反应物浓度越大,反应速率越快 |
| C | 制备硫酸四氨合铜晶体 | 向盛有4mL0.1mol/LCuSO4溶液的试管里滴加几滴0.1mol/L氨水 | 生成了难溶物为深蓝色,则制得了[Cu(NH3)4]SO4·H2O晶体 |
| D | 探究苯与液溴的反应类型 | 将苯、液溴、铁粉混合后产生的气体通入AgNO3溶液中 | 溶液中产生淡黄色沉淀,则说明苯与液溴发生了取代反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列措施中,不能增大化学反应速率的是
A.Al在 中燃烧生成 中燃烧生成 ,用铝粉代替铝片 ,用铝粉代替铝片 |
B.Zn与稀硫酸反应制取 时,加入蒸馏水 时,加入蒸馏水 |
C.石灰石与稀盐酸反应生成 时,适当提高温度 时,适当提高温度 |
D.用 固体分解制取 固体分解制取 时,添加少量 时,添加少量 |
您最近一年使用:0次
解题方法
7 . 利用环戊二烯( )加氢制备环戊烯(
)加氢制备环戊烯( ),按
),按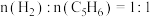 加入恒压密闭容器中,若仅发生如下反应:
加入恒压密闭容器中,若仅发生如下反应:
①  ②
②

A. 时, 时, 的转化率为87.4% 的转化率为87.4% |
B.由图可知,反应的活化能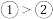 |
C.相同条件下,若增大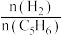 , , 选择性提高 选择性提高 |
D.升高温度, 生成速率增大, 生成速率增大, 生成速率减小 生成速率减小 |
您最近一年使用:0次
名校
8 . 向 恒容密闭的催化反应器中充入
恒容密闭的催化反应器中充入 和
和 ,发生反应:
,发生反应:
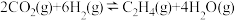 ,测得温度对
,测得温度对 的平衡转化率和催化剂催化效率的影响如下图所示。下列说法正确的是
的平衡转化率和催化剂催化效率的影响如下图所示。下列说法正确的是
 恒容密闭的催化反应器中充入
恒容密闭的催化反应器中充入 和
和 ,发生反应:
,发生反应: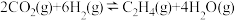 ,测得温度对
,测得温度对 的平衡转化率和催化剂催化效率的影响如下图所示。下列说法正确的是
的平衡转化率和催化剂催化效率的影响如下图所示。下列说法正确的是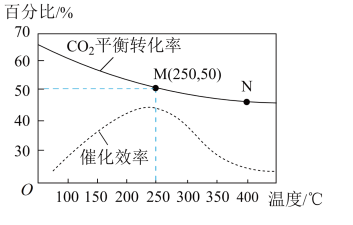
A.生成 的速率:M点一定小于N点 的速率:M点一定小于N点 |
| B.容器内气体平均分子量不变说明反应达到平衡状态 |
C.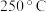 反应达到平衡状态, 反应达到平衡状态, 的体积分数是 的体积分数是 |
| D.升高温度,催化剂的催化效率降低 |
您最近一年使用:0次
名校
解题方法
9 . 密闭容器中发生的反应
 ,其他条件相同时,改变一个因素对化学反应速率的影响,下列说法不正确的是
,其他条件相同时,改变一个因素对化学反应速率的影响,下列说法不正确的是

 ,其他条件相同时,改变一个因素对化学反应速率的影响,下列说法不正确的是
,其他条件相同时,改变一个因素对化学反应速率的影响,下列说法不正确的是| A.加入碳的量,化学反应速率不变 |
| B.升高温度,化学反应速率增大 |
| C.缩小体积,化学反应速率增大 |
D.保持压强不变,充入一定量的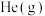 ,化学反应速率不变 ,化学反应速率不变 |
您最近一年使用:0次
解题方法
10 . 某化学兴趣小组为探究影响KI溶液与双氧水反应速率的因素,设计如下系列实验.用 计测量反应过程中溶液
计测量反应过程中溶液 的变化,当
的变化,当 不变时,视为反应终点,记录此时的时间为t.所用试剂为
不变时,视为反应终点,记录此时的时间为t.所用试剂为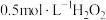 溶液、
溶液、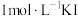 溶液、
溶液、 硫酸溶液、蒸馏水.请回答下列问题:
硫酸溶液、蒸馏水.请回答下列问题:
(1)实验1、2的目的是研究_______ 对反应速率的影响;
________ .
(2)通过对比实验______________ (填标号),可研究温度对反应速率的影响;实验3不在更高温度下进行的原因可能是______________ .
(3)实验1中反应的离子方程式为_____________________ ; 末,溶液中
末,溶液中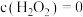 ,不考虑其他副反应,
,不考虑其他副反应, 内实验1的平均反应速率
内实验1的平均反应速率
________  .
.
(4)实验结束后,指导老师指出KI溶液对 的分解具有催化作用,反应历程可简化为反应i(
的分解具有催化作用,反应历程可简化为反应i( )和反应ii.
)和反应ii. 中共价键的类型为
中共价键的类型为______________________________ ;反应ⅱ的离子方程式为___________________ 。
 计测量反应过程中溶液
计测量反应过程中溶液 的变化,当
的变化,当 不变时,视为反应终点,记录此时的时间为t.所用试剂为
不变时,视为反应终点,记录此时的时间为t.所用试剂为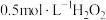 溶液、
溶液、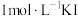 溶液、
溶液、 硫酸溶液、蒸馏水.请回答下列问题:
硫酸溶液、蒸馏水.请回答下列问题:| 实验序号 |  溶液体积/ 溶液体积/  | KI溶液体积/ | 硫酸溶液体积/ | 水的体积/ | 温度/℃ |  |
| 1 | 20 | 20 | 10 | 0 | 25 |  |
| 2 | 10 | 20 | a | b | 25 |  |
| 3 | 10 | 20 | 10 | c | 28 |  |

(2)通过对比实验
(3)实验1中反应的离子方程式为
 末,溶液中
末,溶液中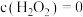 ,不考虑其他副反应,
,不考虑其他副反应, 内实验1的平均反应速率
内实验1的平均反应速率
 .
.(4)实验结束后,指导老师指出KI溶液对
 的分解具有催化作用,反应历程可简化为反应i(
的分解具有催化作用,反应历程可简化为反应i( )和反应ii.
)和反应ii. 中共价键的类型为
中共价键的类型为
您最近一年使用:0次



