某汽车安全气囊的产气药主要含有 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
回答下列问题:
(1) 、
、 、
、 、
、 四种物质中,属于氧化物的是
四种物质中,属于氧化物的是___________ 。
(2) 是助氧化剂,其中氯元素的化合价为
是助氧化剂,其中氯元素的化合价为___________ 。
(3) 是主氧化剂,与
是主氧化剂,与 发生置换反应,还原产物为
发生置换反应,还原产物为___________ 。
(4) 是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为___________ 。
(5) 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和
和 ,
, 和
和 的物质的量之比为
的物质的量之比为___________ 。
(6) 上述产气药产生的气体通过碱石灰后得到
上述产气药产生的气体通过碱石灰后得到 (标准状况)。
(标准状况)。
①用碱石灰除去的物质为___________ ;
②该产气药中 的质量分数为
的质量分数为___________ 。
 、
、 、
、 、
、 等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,产气药产生大量气体使气囊迅速膨胀,从而起到保护作用。回答下列问题:
(1)
 、
、 、
、 、
、 四种物质中,属于氧化物的是
四种物质中,属于氧化物的是(2)
 是助氧化剂,其中氯元素的化合价为
是助氧化剂,其中氯元素的化合价为(3)
 是主氧化剂,与
是主氧化剂,与 发生置换反应,还原产物为
发生置换反应,还原产物为(4)
 是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为(5)
 是气体发生剂,受热分解产生
是气体发生剂,受热分解产生 和
和 ,
, 和
和 的物质的量之比为
的物质的量之比为(6)
 上述产气药产生的气体通过碱石灰后得到
上述产气药产生的气体通过碱石灰后得到 (标准状况)。
(标准状况)。①用碱石灰除去的物质为
②该产气药中
 的质量分数为
的质量分数为
更新时间:2023-01-05 12:48:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:

(1)物质①与水反应的离子方程式为_______ ,所以通常将其保存在_______ 中。
(2)用双线桥法分析淡黄色固体②与二氧化碳的反应:_______ 。
(3)从物质类别的视角看,NaOH属于_______ (填编号,下同)类物质,一般能与下列_______ 类别的物质发生反应。
①非金属单质②碱性氧化物③酸④碱
(4)从核心元素价态的视角看,NaH中H元素的化合价为_______ ,从H元素的价态分析,NaH常用作_______ (填“氧化剂”或“还原剂”)。已知NaH与水的反应为: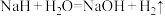 ,则标准状况下生成4480mL
,则标准状况下生成4480mL 时转移电子物质的量是
时转移电子物质的量是_______ 。
(5)某化学小组设计了下列实验方案鉴别 和
和 两种白色粉末,其中不能达到预期目的的是
两种白色粉末,其中不能达到预期目的的是_______ (填编号)。
①分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
②分别向等量的白色粉末中加少量等体积的水,比较固体温度的变化
③分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
④分别将等量的白色粉末加热(如图所示),比较澄清石灰水是否变浑浊


(1)物质①与水反应的离子方程式为
(2)用双线桥法分析淡黄色固体②与二氧化碳的反应:
(3)从物质类别的视角看,NaOH属于
①非金属单质②碱性氧化物③酸④碱
(4)从核心元素价态的视角看,NaH中H元素的化合价为
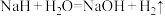 ,则标准状况下生成4480mL
,则标准状况下生成4480mL 时转移电子物质的量是
时转移电子物质的量是(5)某化学小组设计了下列实验方案鉴别
 和
和 两种白色粉末,其中不能达到预期目的的是
两种白色粉末,其中不能达到预期目的的是①分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
②分别向等量的白色粉末中加少量等体积的水,比较固体温度的变化
③分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
④分别将等量的白色粉末加热(如图所示),比较澄清石灰水是否变浑浊

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】观察氧化物和酸碱盐的关系:
回答下列问题:
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往___________ 性越强; 元素有
元素有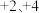 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是___________ (填化学式)。
(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应生成盐时,酸性氧化物提供盐中___________ (填字母,下同),碱性氧化物提供盐中___________ 。
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)已知 为紫红色。将
为紫红色。将 放入
放入 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性: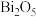
___________ ,
___________ 。
(4)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是___________ 。
②上述物质中既不是电解质也不是非电解质的是___________ 。
(5)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来。

①加水的烧杯为___________ (填字母)。
② 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( )。已知:
)。已知: 与
与 反应只生成
反应只生成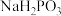 和
和 两种盐。那么
两种盐。那么 为
为___________ (填“正盐”或“酸式盐”);写出 (弱酸)与少量
(弱酸)与少量 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
| 氧化物 |  |  |  |  |  |  | 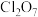 |
| 性质 | 强碱性 | 中强碱性 | 两性 | 弱酸性 | 中强酸性 | 强酸性 | 更强酸性 |
| 对应碱 |  |  |  | ||||
| 对应酸 | 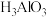 |  |  |  |  | ||
| 对应盐 |  |  | 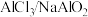 |  |  |  | 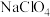 |
(1)横向从价态的视角,发现氧化物的中心元素价态越高,往往
 元素有
元素有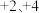 两种常见化合价,则对应氧化物碱性更强的是
两种常见化合价,则对应氧化物碱性更强的是(2)纵向从对应酸碱盐的视角,发现氧化物与酸或碱反应生成盐时,酸性氧化物提供盐中
A.金属阳离子 B.氢离子 C.含氧酸根离子 D.氯离子
(3)已知
 为紫红色。将
为紫红色。将 放入
放入 溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性:
溶液中,溶液变成紫红色。试分别判断下列氧化物的酸碱性: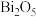

(4)化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
①从物质的分类角度看,不恰当的一种物质是
②上述物质中既不是电解质也不是非电解质的是
(5)在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来。

①加水的烧杯为
②
 是三元酸,能生成
是三元酸,能生成 、
、 两种酸式盐和
两种酸式盐和 一种正盐。磷还有一种含氧酸叫亚磷酸(
一种正盐。磷还有一种含氧酸叫亚磷酸( )。已知:
)。已知: 与
与 反应只生成
反应只生成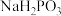 和
和 两种盐。那么
两种盐。那么 为
为 (弱酸)与少量
(弱酸)与少量 溶液反应的离子方程式
溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)下列每组物质中都有一种物质与其他物质在分类上不同。试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来。
①硫酸钡、氯化银、氯化钾、碳酸:____ 。
②磷酸、硝酸、盐酸、硫酸:____ 。
③浊液、溶液、胶体、水:____ 。
(2)有如下物质:①铁丝;②氢氧化钡溶液;③NaHCO3固体;④NH3;⑤酒精;⑥蒸馏水;⑦SO2;⑧熔融的Na2CO3;⑨氧化钙。回答下列问题:
已知蒸馏水有微弱的导电性,上述物质除⑥外,能导电的是:____ (填序号下同);属于电解质的是:____ ;属于非电解质的是:____ ;物质③溶于水能导电的原因为:____ (用必要的方程式表示)。
(1)下列每组物质中都有一种物质与其他物质在分类上不同。试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来。
①硫酸钡、氯化银、氯化钾、碳酸:
②磷酸、硝酸、盐酸、硫酸:
③浊液、溶液、胶体、水:
(2)有如下物质:①铁丝;②氢氧化钡溶液;③NaHCO3固体;④NH3;⑤酒精;⑥蒸馏水;⑦SO2;⑧熔融的Na2CO3;⑨氧化钙。回答下列问题:
已知蒸馏水有微弱的导电性,上述物质除⑥外,能导电的是:
您最近一年使用:0次
【推荐1】认识氧化还原反应,根据所学知识填空:
(1)氧化还原反应的特征是___________ ;氧化还原反应的本质是___________ 。
对于反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)MnO2中的Mn元素化合价___________ (填“升高”或“降低”),在反应中___________ 电子(填“得到”或“失去”),发生___________ 反应(填“氧化”或“还原”)。
(3)HCl中的Cl元素化合价___________ (填“升高”或“降低”),在反应中___________ 电子(填“得到”或“失去”),发生___________ 反应(填“氧化”或“还原”)。
(1)氧化还原反应的特征是
对于反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(2)MnO2中的Mn元素化合价
(3)HCl中的Cl元素化合价
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知有下列反应:
①2H2O+Cl2+SO2===H2SO4+2HCl
②2KMnO4+16HCl(浓) ===2KCl+2MnCl2+5Cl2↑+8H2O
根据上述两个反应回答:
(1)Cl2、KMnO4、H2SO4三者氧化性强弱顺序为______________ ,Cl-、SO2、Mn2+三者还原性强弱顺序为___________ 。
(2)反应①中氧化产物和还原产物的质量之比为________ 。
(3)反应②中浓盐酸表现出的性质是________ 。
A.还原性 B.酸性 C.氧化性
(4)用双线桥法标出反应②电子转移的方向和数目_________________
①2H2O+Cl2+SO2===H2SO4+2HCl
②2KMnO4+16HCl(浓) ===2KCl+2MnCl2+5Cl2↑+8H2O
根据上述两个反应回答:
(1)Cl2、KMnO4、H2SO4三者氧化性强弱顺序为
(2)反应①中氧化产物和还原产物的质量之比为
(3)反应②中浓盐酸表现出的性质是
A.还原性 B.酸性 C.氧化性
(4)用双线桥法标出反应②电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】KClO3和浓盐酸在一定温度下反应会生成易爆物二氧化氯,其变化可表述为:___________KClO3+___________HCl(浓)=___________KCl+___________ClO2↑+___________Cl2↑+ ___________H2O
(1)氧化剂是___________ ,还原剂是___________ ;氧化产物是___________ ,还原产物是___________ 。
(2)浓盐酸在反应中显示出来的性质是___________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)请配平上述化学方程式___________ 。
(1)氧化剂是
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)请配平上述化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献。以NaCl、 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,工业上由此方法制得的纯碱中含有少量的
,进而生产出纯碱,工业上由此方法制得的纯碱中含有少量的 杂质,某化学兴趣小组为验证
杂质,某化学兴趣小组为验证 杂质的存在并测定纯碱的纯度
杂质的存在并测定纯碱的纯度 进行如下实验:
进行如下实验:
(1)验证 杂质的存在
杂质的存在
取少量样品置于大试管中加热如图所示:

①大试管中发生化学反应方程式为______________________ .
②证明纯碱中含有 杂质的现象为
杂质的现象为______________ .
(2)方案一:沉淀法
取ag样品溶于水配成溶液,加入足量_______ 将样品充分反应,过滤、洗涤、干燥称量沉淀的质量为bg.由此计算混合物中 .
.
A.NaOH溶液B. 溶液C.
溶液C. 溶液
溶液
(3)方案二:量气法
取ag样品溶于水配成溶液,向其中逐滴滴入盐酸,产生 的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图.
的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图.

①加入盐酸 时发生的离子反应方程式为
时发生的离子反应方程式为_______________ .
②ag样品中 和
和 的个数比为
的个数比为_________ ,然后可求出 。
。
 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,工业上由此方法制得的纯碱中含有少量的
,进而生产出纯碱,工业上由此方法制得的纯碱中含有少量的 杂质,某化学兴趣小组为验证
杂质,某化学兴趣小组为验证 杂质的存在并测定纯碱的纯度
杂质的存在并测定纯碱的纯度 进行如下实验:
进行如下实验:(1)验证
 杂质的存在
杂质的存在取少量样品置于大试管中加热如图所示:

①大试管中发生化学反应方程式为
②证明纯碱中含有
 杂质的现象为
杂质的现象为(2)方案一:沉淀法
取ag样品溶于水配成溶液,加入足量
 .
.A.NaOH溶液B.
 溶液C.
溶液C. 溶液
溶液(3)方案二:量气法
取ag样品溶于水配成溶液,向其中逐滴滴入盐酸,产生
 的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图.
的体积(y轴)与所加入盐酸的体积(x轴)的关系如下图.
①加入盐酸
 时发生的离子反应方程式为
时发生的离子反应方程式为②ag样品中
 和
和 的个数比为
的个数比为 。
。
您最近一年使用:0次
【推荐2】(1)加热13.7g Na2CO3和NaHCO3的混合物至质量不再变化,恢复至室温,剩余固体的质量为10.6g,则混合物中NaHCO3的物质的量为___________ 。
(2)根据反应8NH3 + 3Cl2=N2+ 6NH4Cl,回答下列问题:
①该反应中______ 元素被还原,______ 元素被氧化;
②在该反应中,若有0.3mol电子发生转移,在标准状况下,可生成N2的体积为______ L。
(2)根据反应8NH3 + 3Cl2=N2+ 6NH4Cl,回答下列问题:
①该反应中
②在该反应中,若有0.3mol电子发生转移,在标准状况下,可生成N2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】钠单质性质活泼,钠有多种化合物。请回答下列问题:
(1) 能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:
能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:___________ 、___________ 。
(2)除去碳酸钠固体中混有的碳酸氢钠的方法为(用化学方程式表示):___________ 。
(3)某碳酸钠溶液中含有NaCl,验证该溶液中含有Cl-的实验操作和现象是:取少量待测液于试管中,___________ ,如果溶液出现白色沉淀,说明溶液中含有氯离子。
(4)已知碳酸钠可用于从海水提取溴,涉及的反应如下: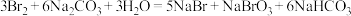
①该反应的离子方程式为___________ 。
②该反应中氧化剂与还原剂的质量之比是___________ 。
(1)
 能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:
能够用作呼吸面具中的供氧剂,用化学方程式说明主要原理:(2)除去碳酸钠固体中混有的碳酸氢钠的方法为(用化学方程式表示):
(3)某碳酸钠溶液中含有NaCl,验证该溶液中含有Cl-的实验操作和现象是:取少量待测液于试管中,
(4)已知碳酸钠可用于从海水提取溴,涉及的反应如下:
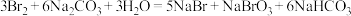
①该反应的离子方程式为
②该反应中氧化剂与还原剂的质量之比是
您最近一年使用:0次



