真题
解题方法
1 . 碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题:
(1) 的一种制备方法如下图所示:
的一种制备方法如下图所示: 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为_______ ;若反应物用量比 时,氧化产物为
时,氧化产物为_______ ;当 ,单质碘的收率会降低,原因是
,单质碘的收率会降低,原因是_______ 。
(2)以 为原料制备
为原料制备 的方法是:先向
的方法是:先向 溶液中加入过量的
溶液中加入过量的 ,生成碘化物;再向混合溶液中加入
,生成碘化物;再向混合溶液中加入 溶液,反应得到
溶液,反应得到 ,上述制备
,上述制备 的总反应的离子方程式为
的总反应的离子方程式为_______ 。
(3) 溶液和
溶液和 溶液混合可生成
溶液混合可生成 沉淀和
沉淀和 ,若生成
,若生成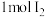 ,消耗的
,消耗的 至少为
至少为_______  。
。 在
在 溶液中可发生反应
溶液中可发生反应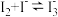 。实验室中使用过量的
。实验室中使用过量的 与
与 溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量
溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是
的原因是_______ 。
(1)
 的一种制备方法如下图所示:
的一种制备方法如下图所示: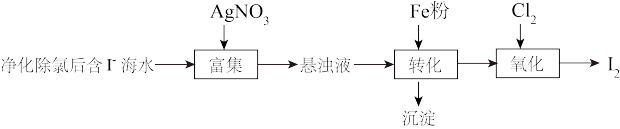
 粉进行转化反应的离子方程式为
粉进行转化反应的离子方程式为②通入
 的过程中,若氧化产物只有一种,反应的化学方程式为
的过程中,若氧化产物只有一种,反应的化学方程式为 时,氧化产物为
时,氧化产物为 ,单质碘的收率会降低,原因是
,单质碘的收率会降低,原因是(2)以
 为原料制备
为原料制备 的方法是:先向
的方法是:先向 溶液中加入过量的
溶液中加入过量的 ,生成碘化物;再向混合溶液中加入
,生成碘化物;再向混合溶液中加入 溶液,反应得到
溶液,反应得到 ,上述制备
,上述制备 的总反应的离子方程式为
的总反应的离子方程式为(3)
 溶液和
溶液和 溶液混合可生成
溶液混合可生成 沉淀和
沉淀和 ,若生成
,若生成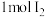 ,消耗的
,消耗的 至少为
至少为 。
。 在
在 溶液中可发生反应
溶液中可发生反应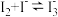 。实验室中使用过量的
。实验室中使用过量的 与
与 溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量
溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量 的原因是
的原因是
您最近半年使用:0次
2021-06-11更新
|
19867次组卷
|
28卷引用:2021年高考全国甲卷化学真题
2021年高考全国甲卷化学真题(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题讲座(二)陌生化学方程式书写(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向09 工艺流程初探-备战2022年高考化学一轮复习考点微专题天津市第一零二中学2022届高三上学期第一次月考化学试题(已下线)2021年高考全国甲卷化学试题变式题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题15 工艺流程综合题-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第27题 工业流程-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 氯及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)山东省威海乳山市银滩高级中学2022-2023学年高三9月月考化学试题山东省临沂市兰陵县第四中学2021-2022学年高三12月月考化学试题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)(已下线)微专题 陌生情景中反应方程式的书写(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第2讲 卤素及海水提溴、提碘(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省济源英才学校2023-2024学年高三上学期11月月考 化学试卷云南省大理州实验中学2021-2022学年高二上学期化学期末考试题
2 . 电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
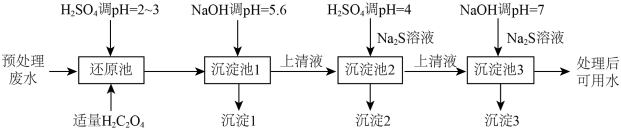
已知: Ksp(CuS)=6.3 ×10-36和Ksp(NiS)=3.0×10-19
回答下列问题:
(1) 中Cr元素的化合价为
中Cr元素的化合价为_______ 。
(2)还原池中有Cr3+生成,反应的离子方程式为_______ 。
(3)沉淀1为Cr(OH)3,其性质与Al(OH)3相似,则Cr(OH)3与NaOH溶液反应的化学方程式_______ 。
(4)Na2S溶液呈碱性的原因是_______ (用离子方程式表示),沉淀2为_______ 。
(5)若废水中还含有Cd2+,pH=4时Cd2+的浓度为_______ mol·L-1,用该结果说明Cd2+影响上述流程进行分离的原因是_______ (设H2S平衡浓度为1.0× 10-6mol·L-1。已知:H2S的K1=1.0×10-7,K2=7.0×10-15,Ksp(CdS)=7.0×10-27)
 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
已知: Ksp(CuS)=6.3 ×10-36和Ksp(NiS)=3.0×10-19
回答下列问题:
(1)
 中Cr元素的化合价为
中Cr元素的化合价为(2)还原池中有Cr3+生成,反应的离子方程式为
(3)沉淀1为Cr(OH)3,其性质与Al(OH)3相似,则Cr(OH)3与NaOH溶液反应的化学方程式
(4)Na2S溶液呈碱性的原因是
(5)若废水中还含有Cd2+,pH=4时Cd2+的浓度为
您最近半年使用:0次
2022-05-27更新
|
5719次组卷
|
4卷引用:重庆市2021年高考真题化学试题
名校
解题方法
3 . 工业上利用石煤矿粉(主要含 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:

已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为 、
、 、
、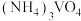 ;
;
②不同pH下,V(V)在溶液中的主要存在形式见下表:
③25℃时, 。
。
回答下列问题:
(1)“焙烧”时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(2)滤液Ⅰ的成分为_______ (填化学式);先“转沉”后“转化”的目的是_______ 。
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到_______ 操作单元中循环使用。
(4)“沉钒”中析出 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①_______ 。②_______ ;25℃时,测得“转化”后,滤液中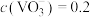 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少_______ mol·L 。
。
(5)“煅烧”时, 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为_______ 。
 及少量
及少量 、
、 )为原料生产
)为原料生产 ,工艺流程如下:
,工艺流程如下:
已知:①“水溶”、“转沉”、“转化”后,所得含钒物质依次为
 、
、 、
、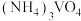 ;
;②不同pH下,V(V)在溶液中的主要存在形式见下表:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 。
。回答下列问题:
(1)“焙烧”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ的成分为
(3)“转化”时,滤渣Ⅱ经高温煅烧后水浸,所得物质可导入到
(4)“沉钒”中析出
 晶体时,需要加入过量
晶体时,需要加入过量 ,其原因是①
,其原因是①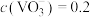 mol·L
mol·L ,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中
,为使“沉钒”时,钒元素的沉降率达到96%,应调节溶液中 至少
至少 。
。(5)“煅烧”时,
 制得产品
制得产品 。但反应体系中,若不及时分离气体Ⅱ,部分
。但反应体系中,若不及时分离气体Ⅱ,部分 会转化成
会转化成 ,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3∶2,该反应的化学方程式为
您最近半年使用:0次
2023-02-08更新
|
2112次组卷
|
4卷引用:山东省济南市2023届高三下学期学情检测(一模)化学试题
名校
解题方法
4 . 工业上以黄铁矿(主要成分为FeS2,含有少量NiS、CuS、SiO2等杂质)为原料制备K4[Fe(CN)6]•3H2O,工艺流程如图:
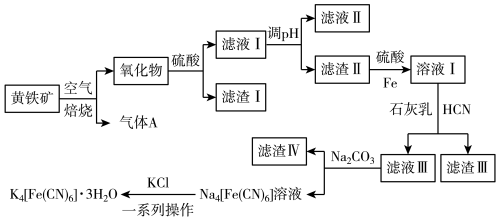
下列说法错误的是

下列说法错误的是
| A.“焙烧”时氧化产物有Fe2O3和SO2 |
| B.“调pH”分离Fe3+与Cu2+、Ni2+是利用了它们氢氧化物Ksp的不同 |
| C.“溶液Ⅰ”中主要反应的离子方程式为6OH-+6HCN+Fe2+=[Fe(CN)6]4-+6H2O |
| D.“一系列操作”为过滤、洗涤、干燥 |
您最近半年使用:0次
2022-03-22更新
|
2172次组卷
|
12卷引用:山东省济南市2022届高三3月高考模拟考试(一模)化学试题
山东省济南市2022届高三3月高考模拟考试(一模)化学试题湖北省枣阳市第一中学2022届高三下学期5月第三次模拟考试化学试题(已下线)专题13 物质的反应和转化-2022年高考真题模拟题分项汇编(已下线)2022年山东省高考真题变式题(不定项选择题)山东省济南第一中学2023届高三上学期开学考试化学试题湖南省湘西自治州古丈县第一中学2021-2022学年高三下学期第二次模拟化学试题湖南省邵阳市第二中学2022-2023学年高三上学期第五次月考化学试题湖南省怀化市会同县第一中学2021-2022学年高三下学期第二次调研考试化学试题湖南省怀化市沅陵县第二中学2021-2022学年高三下学期四月第一次调研考试化学试题(已下线)学科特色7 工艺流程推断(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(不定项选择题)湖南省衡阳市第一中学2023届高三下学期第四次月考化学试题
解题方法
5 . 下图是在Cu基分子筛表面用NH3处理 NO,污染物的一种反应机理。下列说法正确的是
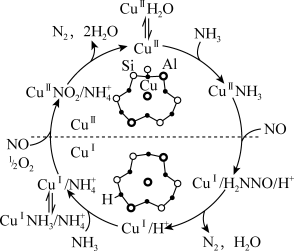
注:图中元素右上角的罗马数字表示化合价

注:图中元素右上角的罗马数字表示化合价
| A.该过程中化合价发生变化的只有N和O两种元素 |
| B.上述过程中催化剂首先吸附的是NO |
| C.该过程中氧化产物和还原产物只有N2 |
D.该过程的总反应为4NH3+4NO+O2 4N2+6H2O 4N2+6H2O |
您最近半年使用:0次
2022-05-22更新
|
1182次组卷
|
8卷引用:河南省郑州市2022届高三第三次质量预测理综化学试题
河南省郑州市2022届高三第三次质量预测理综化学试题(已下线)专题04氧化还原反应-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题04氧化还原反应-2022年高考真题+模拟题汇编(全国卷)(已下线)专题04氧化还原反应-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-2022年高考真题+模拟题汇编(全国卷)(已下线)第5讲 氮及其化合物
解题方法
6 . 《环境科学》刊发了我国科研部门采用零价铁活化过二硫酸钠(Na2S2O8) 去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。下列叙述不正确的是
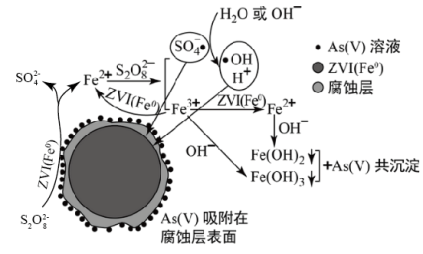

A.56gFe参加反应,消耗的S2O 大于1 mol 大于1 mol |
| B.过二硫酸钠(Na2S2O8) 中S的化合价为+6 |
| C.pH越大,越有利于去除废水中的正五价砷 |
D.碱性条件下,硫酸根自由基发生反应的方程式为:  +H2O= SO +H2O= SO + + +H+ +H+ |
您最近半年使用:0次
7 . 下列关于铁及其化合物之间转化反应的方程式书写正确的是
A. (g)通过灼热铁粉: (g)通过灼热铁粉: |
B.过量铁粉加入稀硝酸中: |
C.氢氧化铁中加入氢碘酸: |
D. 溶液中加入酸性 溶液中加入酸性 溶液: 溶液: |
您最近半年使用:0次
2023-04-19更新
|
1218次组卷
|
3卷引用:广东省广州市2023届高三二模考试化学试题
2023高三·全国·专题练习
解题方法
8 . 亚氯酸钠(NaClO2)和ClO2都是重要的漂白剂。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为_______ 。
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO 存在于中性溶液中):
存在于中性溶液中):
①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:_______ 。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是_______ mg·L-1。
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。
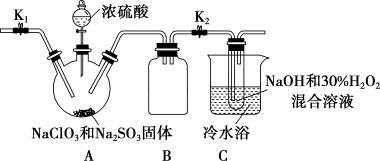
①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:_______ 。
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是_______ 。
(1)草酸(H2C2O4)是一种弱酸,利用硫酸酸化的草酸还原NaClO3,可较安全地生成ClO2,反应的离子方程式为
(2)自来水用ClO2处理后,有少量ClO2残留在水中,可用碘量法做如下检测(已知ClO2存在于pH为4~6的溶液中,ClO
 存在于中性溶液中):
存在于中性溶液中):①取0.50 L水样,加入一定量的碘化钾,用氢氧化钠溶液调至中性,再加入淀粉溶液,溶液变蓝。写出ClO2与碘化钾反应的化学方程式:
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4 mol·L-1的Na2S2O3溶液至恰好反应,消耗Na2S2O3溶液20.00 mL。该水样中ClO2的浓度是
(3)某学习小组设计如下装置制取亚氯酸钠(NaClO2)。

①装置A中产生的ClO2气体,在装置C中反应生成NaClO2,写出生成NaClO2的化学方程式:
②将NaClO2溶液在一定条件下处理即可得到NaClO2晶体。装置B的作用是
您最近半年使用:0次
解题方法
9 . 配平下列氧化还原反应的方程式。
(1)___________KMnO4+___________FeSO4+___________H2SO4=___________K2SO4+___________MnSO4+___________Fe2(SO4)3+___________H2O___________
(2)___________KI+___________KIO3+___________H2SO4=___________I2+___________K2SO4+___________H2O___________
(1)___________KMnO4+___________FeSO4+___________H2SO4=___________K2SO4+___________MnSO4+___________Fe2(SO4)3+___________H2O
(2)___________KI+___________KIO3+___________H2SO4=___________I2+___________K2SO4+___________H2O
您最近半年使用:0次
10 . CuCl为白色固体,微溶于水,不溶于酒精,在空气中能被迅速氧化,是重要的工业催化剂。某化学兴趣小组同学对其制备过程进行了实验探究。
I.小组同学首先用如图装置制备CuCl2。
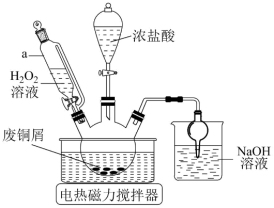
(1)仪器a的名称为_______ NaOH溶液的作用是_______ 。
(2)三颈烧瓶中发生反应的离子方程式为_______ 。
II.查阅资料后,小组同学用(NH4)2SO3还原CuCl2溶液来制备CuCl。
(3)制备反应的离子方程式为_______ 。
(4)将混合物过滤、洗涤、干燥可得CuCl产品。
①过滤操作最好采用抽滤法快速过滤,这样可避免_______ ;
②判断CuCl沉淀洗涤干净的实验方案是_______ 。
(5)研究发现,CuCl的产率与CuCl2起始浓度、溶液pH的关系如下图。
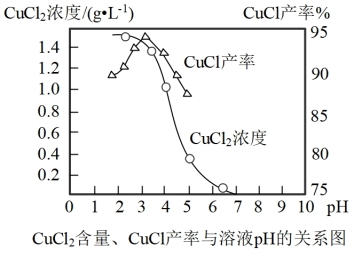
①随着pH增大,CuCl2浓度逐渐降低的原因是_______ ;
②控制溶液的pH在_______ 时,CuCl产率最高。
I.小组同学首先用如图装置制备CuCl2。

(1)仪器a的名称为
(2)三颈烧瓶中发生反应的离子方程式为
II.查阅资料后,小组同学用(NH4)2SO3还原CuCl2溶液来制备CuCl。
(3)制备反应的离子方程式为
(4)将混合物过滤、洗涤、干燥可得CuCl产品。
①过滤操作最好采用抽滤法快速过滤,这样可避免
②判断CuCl沉淀洗涤干净的实验方案是
(5)研究发现,CuCl的产率与CuCl2起始浓度、溶液pH的关系如下图。

①随着pH增大,CuCl2浓度逐渐降低的原因是
②控制溶液的pH在
您最近半年使用:0次



