23-24高一下·全国·课前预习
1 . 工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅,写出该反应的化学方程式___________ 。
您最近半年使用:0次
名校
解题方法
2 . 根据所学知识,回答下列问题。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:___________ 。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:___________ 。
(3)胶体和溶液的本质区别是___________ (填标号)。
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
(5)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下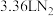 ,则转移的电子数目为
,则转移的电子数目为___________ 。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成
 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
(3)胶体和溶液的本质区别是
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
| A.熔融的NaCl | B.纯净的矿泉水 | C.某品牌的饮料 | D.熟石灰固体 |
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下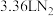 ,则转移的电子数目为
,则转移的电子数目为
您最近半年使用:0次
23-24高一下·全国·课前预习
3 . 氨可在加热条件下和氧化铜反应生成铜和氮气,反应的化学方程式为____ 。
您最近半年使用:0次
名校
解题方法
4 . 氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:
(1)NO2产生硝酸型酸雨的化学方程式为____________________ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为______ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:
①“催化氧化”的目的是____________________ 。
②图中产品中含硫成分为______ (填化学式)。
(4)为探究某种催化剂在有氧条件下用NH3还原NOx的最佳温度,将一定比例的O2、NH3和NOx混合,以一定的流速通过催化NOx还原反应器[如图(a)],反应相同时间后测得NOx的去除率随反应温度的变化曲线如图(b)所示。______________ 。
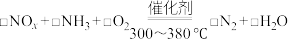
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是____________________ 。
(1)NO2产生硝酸型酸雨的化学方程式为
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

①“催化氧化”的目的是
②图中产品中含硫成分为
(4)为探究某种催化剂在有氧条件下用NH3还原NOx的最佳温度,将一定比例的O2、NH3和NOx混合,以一定的流速通过催化NOx还原反应器[如图(a)],反应相同时间后测得NOx的去除率随反应温度的变化曲线如图(b)所示。
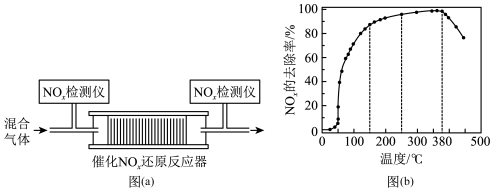
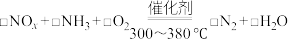
②当反应温度高于380℃时,NOx的去除率迅速下降的原因可能是
您最近半年使用:0次
2024-02-27更新
|
467次组卷
|
3卷引用: 河北郑口中学2023-2024学年高一下学期2月 作业检测考试 化学试题
名校
解题方法
5 . 我国古代四大发明之一的黑火药足由硫黄粉、硝酸钾和木炭粉按一定比例混台而成,爆炸时发生的反应为:S+2KNO3+3C=K2S+N2↑+3X↑。请回答:
(1)X的化学式是_______ ,按照物质的组成和性质分类,属于_______ (填字母)。
A.单质 B.酸性氧化物 C.电解质 D.盐
(2)在上述反应中,还原产物是(填化学式)_______ 。
(3)写出在NaOH溶液中通入过量的X气体发生反应的离子方程式_______ 。
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O,用单线桥标出上述方程式的电子转移方向和数目
+3Cl-+5H2O,用单线桥标出上述方程式的电子转移方向和数目_______ 。
(5)二氧化氯(ClO2)气体是一种常用的高效自来水消毒剂。KClO3和浓盐酸在一定温度下反应生成ClO2和Cl2,该反应的离子方程式为:_______ 。
(1)X的化学式是
A.单质 B.酸性氧化物 C.电解质 D.盐
(2)在上述反应中,还原产物是(填化学式)
(3)写出在NaOH溶液中通入过量的X气体发生反应的离子方程式
(4)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O,用单线桥标出上述方程式的电子转移方向和数目
+3Cl-+5H2O,用单线桥标出上述方程式的电子转移方向和数目(5)二氧化氯(ClO2)气体是一种常用的高效自来水消毒剂。KClO3和浓盐酸在一定温度下反应生成ClO2和Cl2,该反应的离子方程式为:
您最近半年使用:0次
2024-02-26更新
|
53次组卷
|
2卷引用:河北省石家庄市第一中学西校区2023-2024高一上学期期末考试化学试题
名校
6 . 按要求回答下列问题:
(1)胶体是一种常见的分散系,将饱和三氯化铁溶液滴入沸水时,得到的液体是______ 色,反应的化学方程式为_______ 。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的氧化剂是________ ,
②该反应中,发生还原反应的过程是___→_____,_____ 。
③写出该反应的化学方程式___________ 。
(1)胶体是一种常见的分散系,将饱和三氯化铁溶液滴入沸水时,得到的液体是
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的氧化剂是
②该反应中,发生还原反应的过程是___→_____,
③写出该反应的化学方程式
您最近半年使用:0次
解题方法
7 . 水体中氨氮含量超标会造成水体富营养化,用次氯酸钙除去氨氮的原理如图所示。下列说法不正确的是
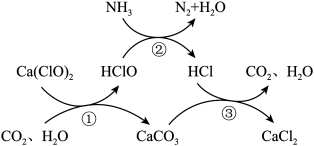

| A.①③属于复分解反应,②属于氧化还原反应 |
B. 三种物质可循环使用 三种物质可循环使用 |
C.每生成 ,转移 ,转移 电子 电子 |
D.除去氨氮的总反应方程式为 |
您最近半年使用:0次
名校
8 . 高铁酸钾是一种新型水处理剂,使用说明书如下。
回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在___________ (填“酸性”“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,错误的是
的说法中,错误的是___________ (填字母)。
a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4) 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为___________ ;该反应消耗 转移的电子数为
转移的电子数为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)消毒净化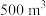 水,至少需要
水,至少需要 的质量为
的质量为___________  。
。
(6)产生 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是___________ 。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降。 减小,稳定性下降。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。 胶体,可除去水中细微的悬浮物,有净水作用。【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放 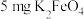 即可达到卫生标准 即可达到卫生标准 |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,错误的是
的说法中,错误的是a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)
 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为 转移的电子数为
转移的电子数为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)消毒净化
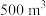 水,至少需要
水,至少需要 的质量为
的质量为 。
。(6)产生
 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是
您最近半年使用:0次
名校
解题方法
9 . NaClO、 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。
(1) 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为___________ (不考虑 的分解)。
的分解)。
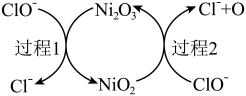
(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是___________ (填“氧化剂”或“还原剂”),当 和
和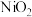 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为___________ 。
②NaClO可在碱性条件下将 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为___________ 。
(3)以氯酸钠、硫酸和二氧化硫为原料制备 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
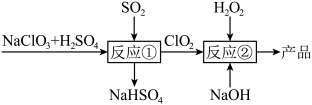
反应①的离子方程式为___________ ;理论上,该流程中参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。(1)
 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为 的分解)。
的分解)。(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收
 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是 和
和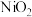 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
②NaClO可在碱性条件下将
 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为(3)以氯酸钠、硫酸和二氧化硫为原料制备
 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
反应①的离子方程式为
 与
与 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
名校
解题方法
10 . 氯是一种典型的非金属元素,具有多种化合价,可以形成食盐、漂白粉等多种含氯化合物。从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。以下是氯元素的“价类二维图”的部分信息。
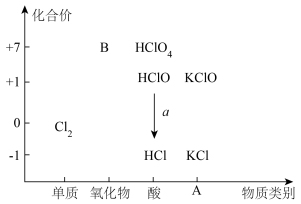
请回答下列问题:
(1)缺失的类别A为___________ ,物质B为___________ (填化学式),能够实现图中a转化的反应方程式为___________ (写一个即可)
(2)已知: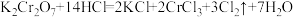 ,按要求完成下列问题。
,按要求完成下列问题。
①用双线桥标明电子转移方向和数目:___________ 。
②该反应中,氧化剂是___________ ,还原剂是___________ ,还原性
___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
③ 完全反应,产生的
完全反应,产生的 在标准状况下的体积为
在标准状况下的体积为___________ L,
(3)写出 在强碱性介质中与
在强碱性介质中与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。

请回答下列问题:
(1)缺失的类别A为
(2)已知:
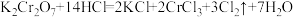 ,按要求完成下列问题。
,按要求完成下列问题。①用双线桥标明电子转移方向和数目:
②该反应中,氧化剂是

 (填“大于”或“小于”)。
(填“大于”或“小于”)。③
 完全反应,产生的
完全反应,产生的 在标准状况下的体积为
在标准状况下的体积为(3)写出
 在强碱性介质中与
在强碱性介质中与 反应生成
反应生成 的离子方程式为
的离子方程式为
您最近半年使用:0次



