锡酸钠 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为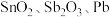 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体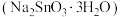 的工艺流程如下:
的工艺流程如下:
②锡酸钠晶体易溶于水,难溶于乙醇。
回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ 。
(2)“高温真空蒸发”控制温度在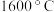 左右,目的是
左右,目的是___________ 。
(3)“高温碱熔”时,单质 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(4)已知“溶浸”后溶液中的阴离子主要为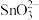 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为___________ 。
(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、___________ (填试剂名称)洗涤、___________ (填“低温”或“高温”)干燥。
(6)利用焦炭在 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为___________  。
。
 在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为
在电镀、印染、纺织、陶瓷等工业中具有重要作用。一种以含铅、锑、锡的复合渣(主要成分为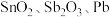 及
及 等)为原料制备锡酸钠晶体
等)为原料制备锡酸钠晶体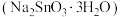 的工艺流程如下:
的工艺流程如下: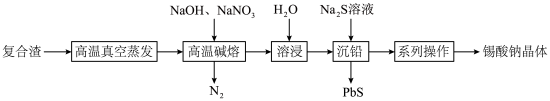
| 物质 |  |  |  |  |
沸点 | 1800 | 2260 | 1550 | 1740 |
回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)“高温真空蒸发”控制温度在
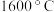 左右,目的是
左右,目的是(3)“高温碱熔”时,单质
 与
与 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(4)已知“溶浸”后溶液中的阴离子主要为
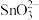 和少量
和少量 ,“沉铅”时发生反应的离子方程式为
,“沉铅”时发生反应的离子方程式为(5)获得锡酸钠晶体的“系列操作”是蒸发浓缩、冷却结晶、过滤、
(6)利用焦炭在
 高温下还原
高温下还原 可制得单质
可制得单质 。
。 存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为
存在白锡、灰锡和脆锡三种同素异形体,其中灰锡的晶体结构与金刚石相似。若晶胞参数为 ,则最近的两个锡原子间的距离为
,则最近的两个锡原子间的距离为 。
。
更新时间:2024-04-19 11:26:26
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂排出的废水中含有大量的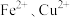 和
和 。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
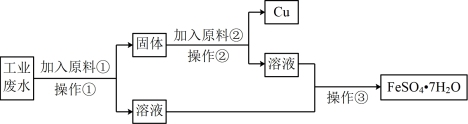
(1)原料①为金属___________ (填元素符号)。
(2)加入原料②是为了溶解过量的①,加入原料②反应的离子方程式___________ 。
(3)操作②要用到的玻璃仪器的名称是漏斗、___________ 、玻璃棒。
(4)操作③要用到蒸发皿,操作③的实验名称是___________ 。
(5)硫酸亚铁分解生成铁红,将反应补充完整: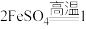
________ 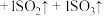 。
。
(6)硫酸亚铁溶液吸收氯气的离子方程式为___________ 。
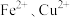 和
和 。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
(1)原料①为金属
(2)加入原料②是为了溶解过量的①,加入原料②反应的离子方程式
(3)操作②要用到的玻璃仪器的名称是漏斗、
(4)操作③要用到蒸发皿,操作③的实验名称是
(5)硫酸亚铁分解生成铁红,将反应补充完整:
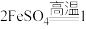
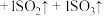 。
。(6)硫酸亚铁溶液吸收氯气的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】二硫化钨(WS2,WS2中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其主要成分是FeWO4,还含少量Al2O3)制备二硫化钨的工艺流程如下:
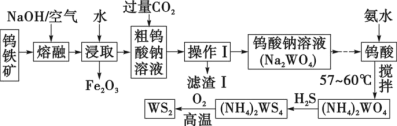
(1)写出FeWO4在碱熔过程中发生反应的化学方程式:___________ 。
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为___________ 。

(1)写出FeWO4在碱熔过程中发生反应的化学方程式:
(2)滤渣Ⅰ中主要成分的形成可用离子方程式表示为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如图:
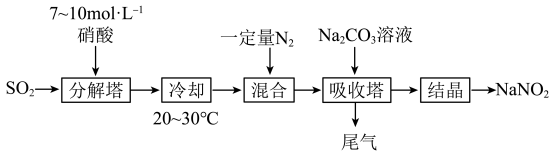
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)“分解塔”中SO2从塔底进入,硝酸从塔顶喷淋,其目的是___________ 。
(2)“分解塔”中的温度不宜过高,其原因是___________ 。
(3)按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则“分解塔”中发生反应的化学方程式为___________ 。
(4)为提高氮氧化物的转化率,可向“尾气”中通入一定量的___________ 气体,再通入“吸收塔”中,实现循环吸收。
(5)“吸收塔”所得溶液中除含有NaNO2、NaNO3和少量Na2CO3外,还含有的溶质为___________ (填化学式)。
(6)工业废气中NO2可用NaOH溶液吸收生成NaNO2和NaNO3,反应的离子方程式为______ 。

已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)“分解塔”中SO2从塔底进入,硝酸从塔顶喷淋,其目的是
(2)“分解塔”中的温度不宜过高,其原因是
(3)按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则“分解塔”中发生反应的化学方程式为
(4)为提高氮氧化物的转化率,可向“尾气”中通入一定量的
(5)“吸收塔”所得溶液中除含有NaNO2、NaNO3和少量Na2CO3外,还含有的溶质为
(6)工业废气中NO2可用NaOH溶液吸收生成NaNO2和NaNO3,反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】广泛用于纺织工业的连二亚硫酸钠(Na2S2O4),俗称保险粉,是一种强还原剂,可溶于水,但不溶于乙醇,在碱性介质中较稳定。
Ⅰ.工业上制备保险粉的流程如下:

(1)步骤①中发生反应的化学方程式为_____ 。
(2)步骤②中生成的沉淀为_____ (填化学式)。
(3)步骤③中加入NaCl固体的作用是_____ ,分离出保险粉的方法为_____ 、洗涤、干燥,洗涤所用试剂是_____ 。
Ⅱ.探究Na2S2O4的性质:某课题小组常温下测得0.050mol·L-1Na2S2O4溶液的pH随时间变化的关系如图所示。
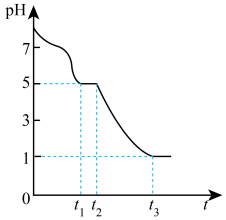
(4)0~t1主要生成HSO ,写出0~t1发生反应的离子方程式:
,写出0~t1发生反应的离子方程式:_____ 。
Ⅰ.工业上制备保险粉的流程如下:

(1)步骤①中发生反应的化学方程式为
(2)步骤②中生成的沉淀为
(3)步骤③中加入NaCl固体的作用是
Ⅱ.探究Na2S2O4的性质:某课题小组常温下测得0.050mol·L-1Na2S2O4溶液的pH随时间变化的关系如图所示。

(4)0~t1主要生成HSO
 ,写出0~t1发生反应的离子方程式:
,写出0~t1发生反应的离子方程式:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
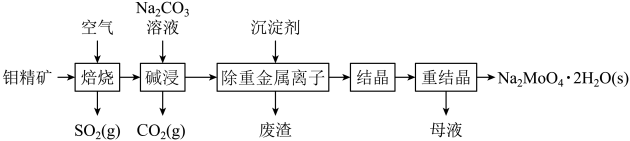
(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是___ ,焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ)。
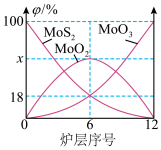
①x=___ 。
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:___ 。
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是___ 。
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是___ %[已知:Ksp(BaCO3)=1×10-9,Ksp(BaMoO4)=4.0×10-8,溶液体积变化忽略不计]。
(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是___ 。
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是___ (填选项字母)。
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸

(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是

①x=
②“焙烧”时MoS2最终转化为MoO3,写出该反应的化学方程式:
(2)沉淀剂通常用Na2S,使用时若溶液pH较小,Pb2+沉淀不完全,原因是
(3)“结晶”前需向滤液中加入Ba(OH)2固体以除去CO
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol•L-1,c(CO
)=0.40mol•L-1,c(CO )=0.10mol•L-1,当BaMoO4开始沉淀时,CO
)=0.10mol•L-1,当BaMoO4开始沉淀时,CO 的去除率是
的去除率是(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备Na2MoO4,同时生成硫酸盐,该反应的离子方程式是
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是:在空气中钼酸盐能在钢铁表面形成FeMoO4——Fe2O3保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外还需加入的物质是
A.NaNO2 B.通入适量N2 C.油脂 D.盐酸
您最近半年使用:0次
【推荐3】钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如下:

回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是_______________ 。
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是__________ ;再向滤液加入氨水调节pH=6,滤液中Sc3+的浓度为_____________ 。(已知:Ksp[Mn(OH)2]=1.9×10-13、Ksp[Fe(OH)3]=2.6×10-39,Ksp[Sc(OH)3]=9.0×10-31)
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中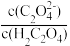 =
=__________ (保留两位有效数字)。写出“沉钪”得到草酸钪的离子方程式________________________ 。【已知Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5】
(4)草酸钪“灼烧”氧化的化学方程式为________________ 。

回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是
(2)先加入氨水调节pH=3,过滤,滤渣主要成分是
(3)用草酸“沉钪”。25 ℃时pH=2的草酸溶液中
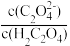 =
=(4)草酸钪“灼烧”氧化的化学方程式为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C, B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是___________ 。
(2) H2A比H2D熔沸点高得多的原因是___________ 。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH 溶液反应可生成Na[C(OH)4]
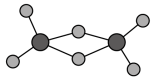
①C2Cl6属于___________ 晶体(填晶体类型),其中C原子的杂化轨道类型为___________ 杂化。
②[C(OH)4]-中存在的化学键有___________ 。
(4)B的氯化物、C的氟化物晶格能分别是2957KJ/mol、5492KJ/mol,二者相差很大的原因是___________ 。
(5)D与E所形成化合物晶体的晶胞如图所示。

①原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2),c为(1/2,1/2,0)。则d原子的坐标为___________ 。
②已知该晶胞的密度为ρg/cm3,则其中两个D,原子之间的距离为___________ pm(列出计算式即可)。
(1)B、C中第一电离能较大的是
(2) H2A比H2D熔沸点高得多的原因是
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH 溶液反应可生成Na[C(OH)4]

①C2Cl6属于
②[C(OH)4]-中存在的化学键有
(4)B的氯化物、C的氟化物晶格能分别是2957KJ/mol、5492KJ/mol,二者相差很大的原因是
(5)D与E所形成化合物晶体的晶胞如图所示。

①原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2),c为(1/2,1/2,0)。则d原子的坐标为
②已知该晶胞的密度为ρg/cm3,则其中两个D,原子之间的距离为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的价电子排布式为_______ ,有_______ 个未成对电子。
(2)Ge与C是同主族元素,第一电离能Ge_______ C(填“大于”或“小于”)。
(3)比较下列锗卤化物的熔点和沸点,分析锗卤化物变化原因_______ 。
GeCl4水解可获得高纯GeO2,经H2还原成金属Ge。GeCl4的空间结构为_______ 。
(4)Ge单晶具有金刚石型结构,Ge单晶的熔点比金刚石_______ (填“高”或“低”)。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。

②已知Ge单晶的晶胞参数 a pm,其密度为_______ g∙cm-3(列出计算式即可)。
(1)基态Ge原子的价电子排布式为
(2)Ge与C是同主族元素,第一电离能Ge
(3)比较下列锗卤化物的熔点和沸点,分析锗卤化物变化原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,Ge单晶的熔点比金刚石
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②已知Ge单晶的晶胞参数 a pm,其密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】国内外学者近年来对金属-有机框架(MOFs)作为催化剂光解制氢和还原CO2等方面的研究取得了丰硕的成果。其中Masaya等人利用Ti-MOF-NH2、H2PtCl6、DMF等原料制备了催化剂Pt/F-MOF-NH2。回答下列问题:
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是_______ ,处于_______ 区。
(2)DMF的结构是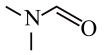 ,σ键与π键的数目比是
,σ键与π键的数目比是________ ,其中N原子的杂化方式是________ 。
(3)已知pKa=-lgKa,CCl3CH2OH的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因________ 。
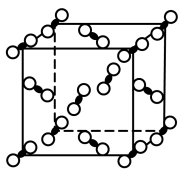
(4)一定条件下,CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有________ 个。若阿伏加德罗常数为NA,干冰的密度为ρg•cm-3,则晶胞体对角线长度是________ cm。
(1)Pt的电子排布式为[Xe]4f145d96s1,则Pt在元素周期表中的位置是
(2)DMF的结构是
 ,σ键与π键的数目比是
,σ键与π键的数目比是(3)已知pKa=-lgKa,CCl3CH2OH的pKa小于CBr3CH2OH,从分子组成与性质之间的关系解释原因
(4)一定条件下,CO2分子可形成干冰晶体,干冰的晶胞模型如图所示。在干冰中,与一个CO2分子紧邻的分子共有

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
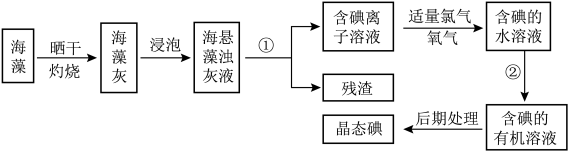
【推荐1】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的过程如下:
(1)灼烧海藻时,除需要三脚架.玻璃棒外,还需要用到的实验仪器是________________ 。(从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.瓷坩埚 C.表面皿 D.泥三角 E.酒精灯 F.坩埚钳
(2)指出提取碘的过程中有关的实验操作名称:①________ 、②________
(3)提取碘的过程②中,通常在________________ (仪器名称)中进行,若得到的是含碘的四氯化碳溶液,静置后分层,下层为________________ 色。
(4)氧化过程请用离子方程式表示__________________________ 。
(1)灼烧海藻时,除需要三脚架.玻璃棒外,还需要用到的实验仪器是
A.烧杯 B.瓷坩埚 C.表面皿 D.泥三角 E.酒精灯 F.坩埚钳
(2)指出提取碘的过程中有关的实验操作名称:①
(3)提取碘的过程②中,通常在
(4)氧化过程请用离子方程式表示
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钴(Co)及其化合物在工业上广泛应用于磁性材料、电池材料及超硬材料等领域。某学习小组欲从某工业废料中回收钴,设计工艺流程如下:(废料中含有Al、Co2O3和Fe2O3等物质)。
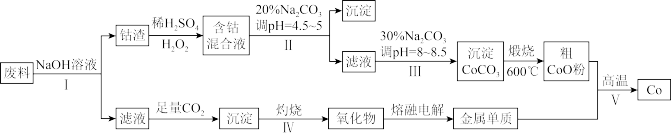
请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是____________ 。
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式___________ 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________ 。
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式__________________________________ 。
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在__________________ (填仪器名称)中灼烧;写出在过程Ⅴ中发生反应的化学方程式__________________________________ 。
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________ mol/L。(已知:CoCO3的溶度积为:Ksp=1.0×10-13)
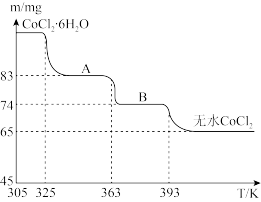
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是____________________ 。

请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】从固体混合物A出发可以发生如下框图所示的一系列变化.
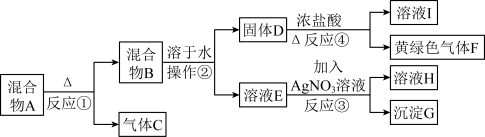
G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察).
回答下列问题:
(1)在实验室中收集气体C,可选择下图装置中的________ 。
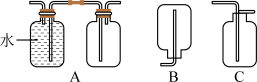
(2)操作②的名称是________ .在操作②中所使用的玻璃仪器的名称是_____ 。
(3)写出反应④的离子方程式:________________________________________ 。
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如图中的装置,其中瓶Ⅰ中盛放的是_________ ,瓶Ⅱ中盛放的是_________________ 。

(5)实验中必须吸收多余的气体F,以免污染空气.下图是实验室用NaOH溶液吸收气体F的装置,为防止产生倒吸现象,合理的装置是____________ .


G为不溶于稀硝酸的白色固体;溶液H的焰色反应呈紫色(透过蓝色的钴玻璃观察).
回答下列问题:
(1)在实验室中收集气体C,可选择下图装置中的

(2)操作②的名称是
(3)写出反应④的离子方程式:
(4)在实验室中,要获得干燥纯净的黄绿色气体F,可以将它通过如图中的装置,其中瓶Ⅰ中盛放的是

(5)实验中必须吸收多余的气体F,以免污染空气.下图是实验室用NaOH溶液吸收气体F的装置,为防止产生倒吸现象,合理的装置是

您最近半年使用:0次



