铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:___________ 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式
更新时间:2024-04-23 19:01:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】Fe(OH)2很不稳定,露置在空气中容易被氧化,Fe(OH)2被氧化的化学方程为:________________ 。为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时你觉得还需加入_________________ 。
(2)除去蒸馏水中溶解的O2常采用_______________________________ 的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__________________________ 。
(4)检验Fe3+存在的最佳试剂是______ ,现象是_______________________ 。
(5)写出Fe与H20在一定条件下反应的化学方程式_________________ 。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时你觉得还需加入
(2)除去蒸馏水中溶解的O2常采用
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是
(4)检验Fe3+存在的最佳试剂是
(5)写出Fe与H20在一定条件下反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得Fe(OH)2白色沉淀。若用下图所示实验装置,则可制得纯净的Fe(OH)2白色沉淀。已知两极材料分别为石墨和铁:
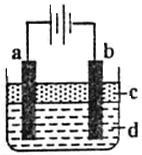
(1)a极材料为______ ,a电极反应式为______ 。
(2)电解液d可以是______ ,则白色沉淀在电极上生成;电解液d也可以是______ ,则白色沉淀在两极间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是______ ,在加苯之前对d溶液进行加热煮沸处理,目的是______ 。
(4)为了在短时间内看到白色沉淀,可以采取的措施是______ 。
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极上看到的气泡外,另一明显的现象为______ 。

(1)a极材料为
(2)电解液d可以是
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是
(4)为了在短时间内看到白色沉淀,可以采取的措施是
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极上看到的气泡外,另一明显的现象为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请按要求完成下列各题:
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为___ 。
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为___ ,反应过程分两步,其中第2步反应的化学方程式为___ 。
(3)写出溶液中硫酸氢钠的电离方程式___ 。
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是___ mL。
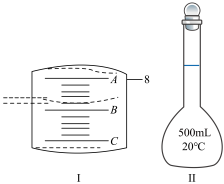
(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O___ g(读到小数点后两位)
(6)图Ⅱ所示仪器的名称是___ 。
(1)将一小块钠投入到盛CuSO4溶液的烧杯中,剧烈反应,放出气体并生成蓝色沉淀,其反应的离子方程式为
(2)将FeSO4溶液与过量NaOH溶液混合并在空气中放置一段时间,整个过程中的现象为
(3)写出溶液中硫酸氢钠的电离方程式
(4)配制某浓度的稀硫酸,用10mL量筒量取浓硫酸的体积如图Ⅰ所示,A与B,B与C刻度间相差1mL,如果刻度A为8,量筒中浓硫酸的体积是

(5)要用CuSO4·5H2O晶体配制500mL0.01mol/LCuSO4溶液,应该用托盘天平称取CuSO4·5H2O
(6)图Ⅱ所示仪器的名称是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】金属材料对于促进生产发展、改善人类生活发挥了巨大作用。请回答下列关于金属及其化合物的问题:
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
(2)实验室里保存 溶液时,常在溶液中加入
溶液时,常在溶液中加入_______ ,其目的为_______ 。
(3)实验室配制 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制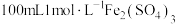 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量_______ g 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要_______ ;如果配制时俯视定容,那么所配溶液的浓度_______ (填“偏大”、“小”或“无影响”)。
(4)除杂:(括号内为杂质)
①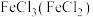 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ ;
②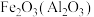 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ 。
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
A.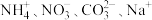 | B.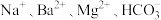 |
C.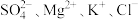 | D.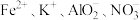 |
 溶液时,常在溶液中加入
溶液时,常在溶液中加入(3)实验室配制
 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制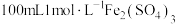 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要(4)除杂:(括号内为杂质)
①
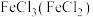 除杂试剂为
除杂试剂为②
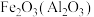 除杂试剂为
除杂试剂为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)一个体重50 kg的健康人身体中含铁2 g。铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的Fe3+转化为Fe2+,利于铁的吸收。人体中经常进行Fe2+和Fe3+的转化,反应中,Fe2+作______ 剂,Fe3+作______ 剂。服用维生素C,可使食物中的Fe3+转化为Fe2+,说明维生素C在反应中作______ 剂,具有_______ 性。
(2)在热的稀硫酸溶液中溶解了11.4 g FeSO4。当加入50 mL 0.5 mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。
___ FeSO4+___ KNO3+___ H2SO4=__ K2SO4+___ Fe2(SO4)3+___ NxOy+___ H2O
①配平该化学方程式,用单线桥标出电子转移的方向和数目__________________ 。
②反应中氧化剂为_________ ,x=_______ ,y=_________ ,
(3)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是___________ 。
(2)在热的稀硫酸溶液中溶解了11.4 g FeSO4。当加入50 mL 0.5 mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出。
①配平该化学方程式,用单线桥标出电子转移的方向和数目
②反应中氧化剂为
(3)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁器时代是人类发展史中⼀个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾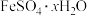 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入________ ,其原因是______________________ (用离子方程式表示)。
(2)利用部分变质的 溶液制备
溶液制备 :
:
部分变质的 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

① 溶液作用的离子方程式为
溶液作用的离子方程式为_____________________________________ 。
②写出由“溶液I”到“沉淀II”反应的离子方程式:_______________________________ 。
(3)电子工业中,常用 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为________________________ 。
(1)长期放置的
 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾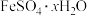 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(2)利用部分变质的
 溶液制备
溶液制备 :
:部分变质的
 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

①
 溶液作用的离子方程式为
溶液作用的离子方程式为②写出由“溶液I”到“沉淀II”反应的离子方程式:
(3)电子工业中,常用
 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。

请回答以下问题:
(1)K2FeO4中Fe的化合价为_____ 。
(2) 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 ,发生相应反应的离子方程式为
,发生相应反应的离子方程式为_____ ,当有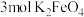 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为_____  。
。
(3)Fe2O3是否为碱性氧化物_____ (填是或否),理由:_____ 。
(4)制备氢氧化亚铁时,观察到白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释该现象:_____ ,其中检验溶液中Fe3+的试剂是KSCN溶液,该反应的离子方程式为:_____ 。

请回答以下问题:
(1)K2FeO4中Fe的化合价为
(2)
 是一种新型水处理剂,将
是一种新型水处理剂,将 溶液、
溶液、 溶液与
溶液与 溶液混合可得到
溶液混合可得到 ,发生相应反应的离子方程式为
,发生相应反应的离子方程式为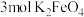 生成时,反应中转移的电子数目为
生成时,反应中转移的电子数目为 。
。(3)Fe2O3是否为碱性氧化物
(4)制备氢氧化亚铁时,观察到白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释该现象:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学基本概念是学习化学的基石,请正确回答下列问题。
(1)用足量的澄清石灰水检验二氧化碳,请写出其反应的离子方程式:_______ 。
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是_______ ,生成1 mol O2转移电子的物质的量为_______ 。
(3)Fe与Cl2在一定条件下恰好完全反应。将产物溶于水,置于两支试管中。
①向第一支试管中滴加KSCN溶液,溶液呈_______ 色;
②向第二支试管中加入足量铁粉,振荡,反应的离子方程式是_______ ;静置后,取上层清液于另一支试管中,滴加NaOH溶液,可以观察到的现象是_______ ,反应的化学方程式是_______ 。
(1)用足量的澄清石灰水检验二氧化碳,请写出其反应的离子方程式:
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是
(3)Fe与Cl2在一定条件下恰好完全反应。将产物溶于水,置于两支试管中。
①向第一支试管中滴加KSCN溶液,溶液呈
②向第二支试管中加入足量铁粉,振荡,反应的离子方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁、铜及其化合物在日常生活中应用广泛,根据下列事实回答问题。
(1)钢铁在空气中容易发生锈蚀,形成铁锈,铁锈的主要成分是_____________________ 。
(2)取一定量氯化亚铁固体,制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是___________________________ 。
(3)取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,现象是____________________ 。
(4)取KI溶液于试管中,加入FeCl3溶液混合,再加入适量CCl4充分振荡、静置,CCl4层呈紫色;写出此反应的离子方程式为_________________________ 。
(5)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是_____________________ 。
(6)磁铁矿是工业上冶炼铁的原料之一,其原理是______________________________________ ,若有1.5mol Fe3O4参加反应,转移电子的物质的量是_____________ mol。
(7)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式_______________________________________ 。
(1)钢铁在空气中容易发生锈蚀,形成铁锈,铁锈的主要成分是
(2)取一定量氯化亚铁固体,制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(3)取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,现象是
(4)取KI溶液于试管中,加入FeCl3溶液混合,再加入适量CCl4充分振荡、静置,CCl4层呈紫色;写出此反应的离子方程式为
(5)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是
(6)磁铁矿是工业上冶炼铁的原料之一,其原理是
(7)Cu不活泼,通常情况下不与稀硫酸反应,但向Cu和稀硫酸的混合物中滴入H2O2溶液后,溶液很快变蓝色,试写出该反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、 、
、 作用产生的,化学式为
作用产生的,化学式为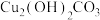 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。
(1)物质分类标准看,“铜绿”属于___________(填字母)。
(2)铜器表面有时会生成铜绿,这层铜绿可用化学方法除去,试写出用盐酸除去铜绿而不损伤器物的反应的离子方程式___________ 。
(3)古代人们高温灼孔雀石[ ]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为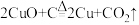 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。
(4)氧化亚铜( )是—种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应,与硫酸反应如下:
)是—种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应,与硫酸反应如下: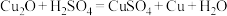 ,该反应中氧化产物为
,该反应中氧化产物为___________ 。
(5)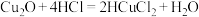 该反应
该反应___________ (填“是”或“不是”)氧化还原反应。
(6)氧化还原反应中实际上包含氧化和还原两个过程,下面是一个发生还原过程的反应式: ,将少量
,将少量 放入稀硝酸中能使上述还原过程发生。
放入稀硝酸中能使上述还原过程发生。
①上述反应中生成3个NO分子的同时,转移电子数目为___________ 个。
②已知 被氧化为
被氧化为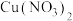 ,写出
,写出 与稀硝酸反应的化学方程式,并标出电子转移的方向和数目:
与稀硝酸反应的化学方程式,并标出电子转移的方向和数目:___________ 。
 、
、 作用产生的,化学式为
作用产生的,化学式为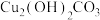 ,“铜绿”能跟酸反应生成铜盐、
,“铜绿”能跟酸反应生成铜盐、 和
和 。
。(1)物质分类标准看,“铜绿”属于___________(填字母)。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)古代人们高温灼孔雀石[
 ]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为
]和木炭的混合物得到一种紫红色的金属铜,其化学反应式为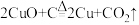 ,该反应属于___________(填序号)。
,该反应属于___________(填序号)。| A.化合反应 | B.置换反应 | C.氧化还原反应 | D.非氧化还原反应 |
 )是—种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应,与硫酸反应如下:
)是—种鲜红色粉末状固体,几乎不溶于水,可在酸性溶液中发生反应,与硫酸反应如下: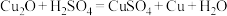 ,该反应中氧化产物为
,该反应中氧化产物为(5)
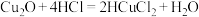 该反应
该反应(6)氧化还原反应中实际上包含氧化和还原两个过程,下面是一个发生还原过程的反应式:
 ,将少量
,将少量 放入稀硝酸中能使上述还原过程发生。
放入稀硝酸中能使上述还原过程发生。①上述反应中生成3个NO分子的同时,转移电子数目为
②已知
 被氧化为
被氧化为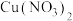 ,写出
,写出 与稀硝酸反应的化学方程式,并标出电子转移的方向和数目:
与稀硝酸反应的化学方程式,并标出电子转移的方向和数目:
您最近半年使用:0次
【推荐2】氧化还原反应在生产、生活中有广泛的用途。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是_______ (填化学式,下同),还原剂是_______ ,氧化产物和还原产物的个数比是_______ 。
Ⅱ.工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O
(2)在该反应中,被氧化的是_______ (填离子符号,下同),还原产物是_______ ,此反应可以推断物质还原性强弱顺序是_______ 。
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2 +_______+ 5H2O
+_______+ 5H2O
(3)请完成该化学方程式并配平_______ 。
(4)该反应中生成2个 转移的电子数为
转移的电子数为_______ 。
Ⅰ.为防治碘缺乏病,通常在食盐中添加少量的碘酸钾(KIO3),碘酸钾和碘化钾在酸性溶液中能发生下列反应:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O。回答下列问题:
(1)该反应中,氧化剂是
Ⅱ.工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ +
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4•7H2O)做处理剂,反应的离子方程式6Fe2+ + + 14H+ = 6Fe3+ + 2Cr3++ 7H2O
+ 14H+ = 6Fe3+ + 2Cr3++ 7H2O(2)在该反应中,被氧化的是
Ⅲ.高铁酸钠是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可用离子方程式表示为:3ClO- +2Fe3+ + 10OH- = 2
 +_______+ 5H2O
+_______+ 5H2O(3)请完成该化学方程式并配平
(4)该反应中生成2个
 转移的电子数为
转移的电子数为
您最近半年使用:0次

 来消毒、杀菌。实验室可用
来消毒、杀菌。实验室可用 固体与浓盐酸制得
固体与浓盐酸制得 ,每生成6个
,每生成6个 分子,转移电子的数目是
分子,转移电子的数目是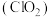 是一种在水处理等方面有广泛应用的高效安全消毒剂。工业上制
是一种在水处理等方面有广泛应用的高效安全消毒剂。工业上制 方法如下:
方法如下: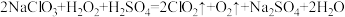 。该反应中被还原的物质为
。该反应中被还原的物质为

