15. FeCl
2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下方法来制备无水FeCl
2。有关物质的性质如下:
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 |
| 溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯;易溶于乙醇,易吸水 |
| 熔点/℃ | -45 | 53 | 100℃时升华 | 672 |
| 沸点/℃ | 132 | 173 | >1000 |
方法一:用H
2还原无水FeCl
3制取FeCl
2。有关装置如下:
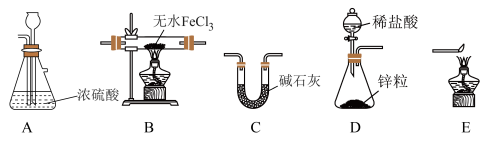
(1)用H
2还原无水FeCl
3制取FeCl
2的化学方程式为
____________。
(2)按气流由左到右的方向,上述仪器的连接顺序为____________。
| A.D→C→B→A→E | B.D→A→B→C→E |
| C.D→B→A→C→E | D.D→C→A→B→E |
(3)该制备装置的缺点为
____________。
方法二:利用反应
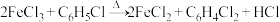
制取无水FeCl
2,并通过测定HCl的量来计算FeCl
3的转化率。按下图装置,在三颈烧瓶中放入32.50g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却并持续通N
2一段时间,分离提纯得到粗产品。

(4)仪器a的名称是
_____________。
(5)仪器b中干燥剂可以选择_____________。
(6)反应结束后恢复至室温,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用最佳试剂是
___________。
(7)回收滤液中C
6H
6Cl的操作方法是_____________。
(8)反应后将c中溶液稀释至250mL。量取25.00mL所配溶液,用0.400mol·L
-1标准NaOH溶液滴定,终点时消耗标准液19.60mL。则氯化铁的转化率为
___________。
(9)若反应后通入N
2时间不足,则测得氯化铁的转化率
______________。
A.偏低
B.偏高
C.不影响
(10)制备无水FeCl
2需要用到无水FeCl
3,某同学提出利用
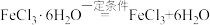
制备无水FeCl
3。你认为该设想是否可行。若不可行,请说明理由;若可行,请简要叙述实验方
_______________。