解题方法
1 . 明矾 是工业上重要的铝盐,可作为净水剂等。
是工业上重要的铝盐,可作为净水剂等。
实验室以铝屑(含少量Fe、Cu)、NaOH溶液、 溶液、
溶液、 溶液为原料制取明矾。
溶液为原料制取明矾。
实验步骤如下:
Ⅰ. 的制取
的制取
取60mL NaOH溶液,置于250mL烧杯中。再称取2.0g铝屑,分次加入NaOH溶液中,水浴加热,并在烧杯口上扣表面皿。反应至无气泡时,向溶液中加少量蒸馏水,趁热过滤。将滤液加热至沸腾,边搅拌边滴加
NaOH溶液,置于250mL烧杯中。再称取2.0g铝屑,分次加入NaOH溶液中,水浴加热,并在烧杯口上扣表面皿。反应至无气泡时,向溶液中加少量蒸馏水,趁热过滤。将滤液加热至沸腾,边搅拌边滴加 稀硫酸,控制溶液的pH为8~9。
稀硫酸,控制溶液的pH为8~9。
继续加热几分钟,抽滤,并用沸水洗涤沉淀。
Ⅱ. 的制备
的制备
将制得的 沉淀转移至烧杯中,加入稀硫酸,并不断搅拌,使沉淀溶解。
沉淀转移至烧杯中,加入稀硫酸,并不断搅拌,使沉淀溶解。
Ⅲ.明矾的制备
将 溶液与
溶液与 溶液混合,搅拌均匀,经过一系列操作,再过滤,干燥,制得粗产品。
溶液混合,搅拌均匀,经过一系列操作,再过滤,干燥,制得粗产品。
Ⅳ.产品纯度测定
取1.0g粗产品,加适量水溶解后,定容至250mL容量瓶中,移取25.00mL该溶液于锥形瓶中,加入20.00mL 的EDTA溶液,过量的EDTA用
的EDTA溶液,过量的EDTA用 的
的 标准溶液滴定,用二甲酚橙作指示剂,进行三次平行实验,消耗
标准溶液滴定,用二甲酚橙作指示剂,进行三次平行实验,消耗 标准溶液的平均体积为15.00mL(EDTA与
标准溶液的平均体积为15.00mL(EDTA与 、
、 均按1∶1反应)。
均按1∶1反应)。
已知:不同温度下明矾溶解度(100g水)如下表:
回答下列问题:
(1)写出NaOH溶液溶解铝屑的离子方程式:___________ 。
(2)步骤Ⅰ中在烧杯口上扣表面皿的作用是___________ ;在趁热过滤之前加少量蒸馏水的目的是___________ ;控制溶液的pH为8~9的目的是___________ 。
(3)用浓硫酸配制 的稀硫酸,下列实验操作会使所配溶液浓度偏高的是___________(填标号)。
的稀硫酸,下列实验操作会使所配溶液浓度偏高的是___________(填标号)。
(4)步骤Ⅲ中“一系列操作”是___________ (填操作名称),该实验操作所用仪器除了铁架台(带铁圈)、酒精灯外,还需要___________ (填仪器名称)。
(5)本实验制得的产品纯度为___________ (保留3位有效数字)。
 是工业上重要的铝盐,可作为净水剂等。
是工业上重要的铝盐,可作为净水剂等。实验室以铝屑(含少量Fe、Cu)、NaOH溶液、
 溶液、
溶液、 溶液为原料制取明矾。
溶液为原料制取明矾。实验步骤如下:
Ⅰ.
 的制取
的制取取60mL
 NaOH溶液,置于250mL烧杯中。再称取2.0g铝屑,分次加入NaOH溶液中,水浴加热,并在烧杯口上扣表面皿。反应至无气泡时,向溶液中加少量蒸馏水,趁热过滤。将滤液加热至沸腾,边搅拌边滴加
NaOH溶液,置于250mL烧杯中。再称取2.0g铝屑,分次加入NaOH溶液中,水浴加热,并在烧杯口上扣表面皿。反应至无气泡时,向溶液中加少量蒸馏水,趁热过滤。将滤液加热至沸腾,边搅拌边滴加 稀硫酸,控制溶液的pH为8~9。
稀硫酸,控制溶液的pH为8~9。继续加热几分钟,抽滤,并用沸水洗涤沉淀。
Ⅱ.
 的制备
的制备将制得的
 沉淀转移至烧杯中,加入稀硫酸,并不断搅拌,使沉淀溶解。
沉淀转移至烧杯中,加入稀硫酸,并不断搅拌,使沉淀溶解。Ⅲ.明矾的制备
将
 溶液与
溶液与 溶液混合,搅拌均匀,经过一系列操作,再过滤,干燥,制得粗产品。
溶液混合,搅拌均匀,经过一系列操作,再过滤,干燥,制得粗产品。Ⅳ.产品纯度测定
取1.0g粗产品,加适量水溶解后,定容至250mL容量瓶中,移取25.00mL该溶液于锥形瓶中,加入20.00mL
 的EDTA溶液,过量的EDTA用
的EDTA溶液,过量的EDTA用 的
的 标准溶液滴定,用二甲酚橙作指示剂,进行三次平行实验,消耗
标准溶液滴定,用二甲酚橙作指示剂,进行三次平行实验,消耗 标准溶液的平均体积为15.00mL(EDTA与
标准溶液的平均体积为15.00mL(EDTA与 、
、 均按1∶1反应)。
均按1∶1反应)。已知:不同温度下明矾溶解度(100g水)如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 溶解度/g | 3.0 | 4.0 | 5.9 | 8.4 | 11.7 | 24.8 | 71.0 | 109.1 |
(1)写出NaOH溶液溶解铝屑的离子方程式:
(2)步骤Ⅰ中在烧杯口上扣表面皿的作用是
(3)用浓硫酸配制
 的稀硫酸,下列实验操作会使所配溶液浓度偏高的是___________(填标号)。
的稀硫酸,下列实验操作会使所配溶液浓度偏高的是___________(填标号)。| A.洗涤量取浓硫酸后的量筒,并将洗涤液倒入烧杯中 |
| B.浓硫酸稀释后立即转移至容量瓶 |
| C.定容时仰视容量瓶刻度线 |
| D.摇匀后发现液面低于刻度线,再补加蒸馏水至刻度线 |
(5)本实验制得的产品纯度为
您最近半年使用:0次
2 . 下列由废易拉罐制取 的实验原理与装置不能达到实验目的的是
的实验原理与装置不能达到实验目的的是
 的实验原理与装置不能达到实验目的的是
的实验原理与装置不能达到实验目的的是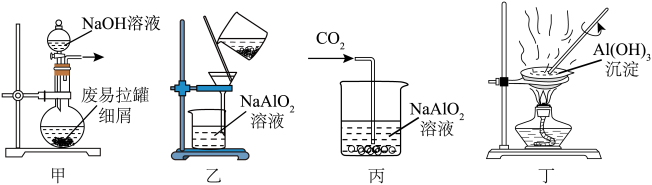
| A.用装置甲溶解废易拉罐细屑 | B.用装置乙过滤得到Na[Al(OH)4]溶液 |
C.用装置丙制取 沉淀 沉淀 | D.用装置丁灼烧 制取 制取 |
您最近半年使用:0次
昨日更新
|
192次组卷
|
2卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
解题方法
3 . 下列各组粒子在指定的溶液中一定能大量共存的是
A.碱性溶液中: | B.与 生成 生成 的溶液: 的溶液: |
C.酸性溶液中: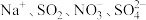 | D.澄清透明溶液中: |
您最近半年使用:0次
名校
解题方法
4 . 在元素周期表中,某些主族元素与右下方的主族元素的某些性质是相似的。如: 和
和 均为两性氢氧化物,
均为两性氢氧化物, 溶于强碱形成
溶于强碱形成 ;BeO和
;BeO和 都具有难溶于水、高熔点等性质。
都具有难溶于水、高熔点等性质。 和
和 在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和
在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和 。工业上用焦炭和
。工业上用焦炭和 在高温下反应制粗硅。硼酸(
在高温下反应制粗硅。硼酸( )和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列化学反应表示不正确的是
)和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列化学反应表示不正确的是
 和
和 均为两性氢氧化物,
均为两性氢氧化物, 溶于强碱形成
溶于强碱形成 ;BeO和
;BeO和 都具有难溶于水、高熔点等性质。
都具有难溶于水、高熔点等性质。 和
和 在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和
在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和 。工业上用焦炭和
。工业上用焦炭和 在高温下反应制粗硅。硼酸(
在高温下反应制粗硅。硼酸( )和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列化学反应表示不正确的是
)和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作润滑剂。下列化学反应表示不正确的是A.焦炭与石英砂反应: |
B.盛放碱液的试剂瓶不能用玻璃塞的原因: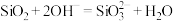 |
C.氯化铍溶液中滴加过量NaOH溶液: |
D.硅与氢氧化钠溶液反应: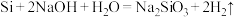 |
您最近半年使用:0次
5 . 下列关于元素及其化合物的性质说法不正确的是
| A.浓硫酸与蔗糖反应,观察到蔗糖变黑,体现了浓硫酸的吸水性 |
| B.硝酸见光受热易分解,一般保存在棕色试剂瓶中,放置在阴凉处 |
C.燃油发动机产生的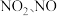 与 与 反应能生成 反应能生成 和 和 ,因此可直接排放 ,因此可直接排放 |
| D.铝制餐具不宜用来蒸煮或长时间存放酸性或者碱性食物 |
您最近半年使用:0次
名校
6 . 化学中广泛存在哲学中“世变引起质变”规律。下列变化过程不符合这一规律的是
| A.铁粉和硝酸反应 | B.Al和NaOH溶液反应 |
C.石灰乳吸收废气中 | D.向 溶液中滴加氨水 溶液中滴加氨水 |
您最近半年使用:0次
7日内更新
|
87次组卷
|
2卷引用:湖北省T8联盟2024届高三下学期压轴考试(二模)化学试题
名校
解题方法
7 . 下列各组离子在给定条件的溶液中一定能大量共存的是
A.在强酸性溶液中:Fe2+ 、K+ 、 Cl-、 |
B.加入铝粉有大量氢气产生的溶液中:Na+ 、Ca2+ 、Br- 、 |
C.在无色溶液中: 、 、 、K+、Cl-、Na+ 、K+、Cl-、Na+ |
D.滴入酚酞显红色的溶液中:K+、 Na+ 、 、 、 |
您最近半年使用:0次
名校
解题方法
8 . 下列说法正确的是
①Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色;
②足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等;
③质量相等的NaHCO3与Na2CO3分别与足量的相同浓度盐酸完全反应时,产生CO2的物质的量相等;
④取a g Al分别与等物质的量的稀盐酸或氢氧化钠溶液充分反应,生成的氢气一样多。
⑤鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液;
⑥NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑦制取氧化铝可以向用四羟基合铝酸钠溶液中通入过量的CO2,再过滤得到氢氧化铝固体,灼烧氢氧化铝得到氧化铝。
①Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色;
②足量O2和质量相等的Na在常温和加热条件下反应,转移的电子数相等;
③质量相等的NaHCO3与Na2CO3分别与足量的相同浓度盐酸完全反应时,产生CO2的物质的量相等;
④取a g Al分别与等物质的量的稀盐酸或氢氧化钠溶液充分反应,生成的氢气一样多。
⑤鉴别NaHCO3与Na2CO3溶液,可用Ca(OH)2溶液;
⑥NaHCO3固体可以做干粉灭火剂,金属钠起火可以用它来灭火;
⑦制取氧化铝可以向用四羟基合铝酸钠溶液中通入过量的CO2,再过滤得到氢氧化铝固体,灼烧氢氧化铝得到氧化铝。
| A.②③④ | B.②⑤⑦ | C.①②⑦ | D.③④⑥ |
您最近半年使用:0次
9 . 已知A、B、C、D、E五种元素的原子序数依次增大,其中A、B、C、D为短周期元素,且只有A、D为非金属元素。A的氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族,且原子序数相差8。
(1)E在元素周期表中的位置:___________ ,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________ 。
(2)A的氢化物溶于水后的电离方程式为___________ ;实验室制备A的氢化物的化学方程式为___________ 。
(3)B单质在空气中燃烧后的产物为___________ ,写出该产物和水反应的离子方程式:___________ 。
(1)E在元素周期表中的位置:
(2)A的氢化物溶于水后的电离方程式为
(3)B单质在空气中燃烧后的产物为
您最近半年使用:0次
解题方法
10 . 某废旧三元锂离子电池正极材料的主要成分是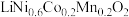 和
和 ,下图是处理电池正极材料回收锂、钴、镍、锰、铝的一种流程。已知:常温下,碳酸锂微溶于水,碳酸氢锂易溶于水。焙烧时
,下图是处理电池正极材料回收锂、钴、镍、锰、铝的一种流程。已知:常温下,碳酸锂微溶于水,碳酸氢锂易溶于水。焙烧时 元素转化为
元素转化为
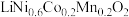 和
和 ,下图是处理电池正极材料回收锂、钴、镍、锰、铝的一种流程。已知:常温下,碳酸锂微溶于水,碳酸氢锂易溶于水。焙烧时
,下图是处理电池正极材料回收锂、钴、镍、锰、铝的一种流程。已知:常温下,碳酸锂微溶于水,碳酸氢锂易溶于水。焙烧时 元素转化为
元素转化为
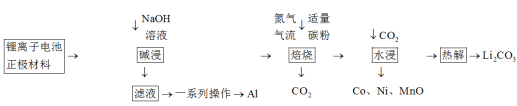
A.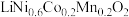 中 中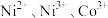 个数比为 个数比为 ,则 ,则 的化合价为 的化合价为 |
| B.该流程中除“焙烧”外均不涉及氧化还原反应 |
| C.冶炼金属锂和金属铝均可用电解其熔融氯化物的方法 |
| D.“水浸”步骤反应温度不宜过高 |
您最近半年使用:0次



