1 . 按要求填空:
(1)将80克NaOH溶解于水中,配成5L溶液,则NaOH的物质的量浓度是
(2)在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为
(3)某些化学反应可以表示为A+B→C+D+H2O,若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式:
(4)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(5)某+3价阳离子(M3+)含有24个电子,它的质量数为56,该离子核内中子数为
您最近一年使用:0次
解题方法
2 . 选择相应的试剂或操作方法除去下列各物质的杂质(括号内为杂质),并按要求写出化学或离子方程式。
(1)Fe(Al):试剂___________ ,化学方程式为___________ 。
(2)FeCl3(FeCl2):试剂___________ ,离子方程式为___________ 。
(3)Na2CO3固体(NaHCO3固体):方法___________ ,化学方程式为___________ 。
(1)Fe(Al):试剂
(2)FeCl3(FeCl2):试剂
(3)Na2CO3固体(NaHCO3固体):方法
您最近一年使用:0次
3 . 在甲、乙两个烧杯中分别装有等体积等物质的量浓度的盐酸与NaOH溶液,向两个烧杯中分别加入等质量的铝粉,反应结束后测得同温同压下生成气体的体积之比为1:2,则两烧杯中反应的情况可能是
| A.甲中酸过量,乙中碱过量 | B.甲、乙都是铝过量 |
| C.甲中铝过量,乙中碱过量 | D.甲中酸过量,乙中铝过量 |
您最近一年使用:0次
解题方法
4 . 甲、乙两烧杯中分别盛有200mL浓度均为2mol/L的盐酸与NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得同温同压下生成气体的体积之比为2:5
| A.2.7g | B.3.6g | C.5.4g | D.9.0g |
您最近一年使用:0次
解题方法
5 . 下列反应的离子方程式书写正确的是
A.铜片插入浓硝酸中: |
B.实验室制氯气: |
C.用氯化铁溶液腐蚀铜箔刻制印刷电路板: |
D.铝和氢氧化钠溶液反应: |
您最近一年使用:0次
6 . 称取两份铝粉,第一份加足量的 溶液,第二份加足量的盐酸,若放出等物质的量的气体,则两份铝粉的质量比
溶液,第二份加足量的盐酸,若放出等物质的量的气体,则两份铝粉的质量比
 溶液,第二份加足量的盐酸,若放出等物质的量的气体,则两份铝粉的质量比
溶液,第二份加足量的盐酸,若放出等物质的量的气体,则两份铝粉的质量比A. | B. | C. | D. |
您最近一年使用:0次
7 . 镁铝合金质优体轻,不易锈蚀,被大量用于航空、造船、日用化工等领域,下列有关说法中正确的是
| A.该合金属于化合物 | B.该合金能全部溶于盐酸溶液中 |
| C.该合金的熔点比镁和铝的都高 | D.该合金的硬度比镁和铝的都小 |
您最近一年使用:0次
2023-06-26更新
|
78次组卷
|
2卷引用:广东惠州珠海深圳汕头四校2020-2021学年高一下学期联考化学试题
名校
8 . 下表是元素周期表的一部分,回答有关问题。
(1)在元素①~⑧中,金属性最强的元素的离子结构示意图是_______ 。
(2)前三周期所有元素中,原子最外层电子数是元素所处周期数2倍的元素有_______ 种。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为_______ 。
(4)在②、③、④这些元素形成的最简单离子中,离子半径由大到小的顺序为_______ (填离子符号)。
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有_______ 。
(6)⑥、⑦和⑧三种元素的最低价气态氢化物的热稳定性由弱到强的依次为_______ (填化学式)。
(7)写出元素⑤的单质与元素③最高价氧化物的水化物反应的离子方程式_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)前三周期所有元素中,原子最外层电子数是元素所处周期数2倍的元素有
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为
(4)在②、③、④这些元素形成的最简单离子中,离子半径由大到小的顺序为
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有
(6)⑥、⑦和⑧三种元素的最低价气态氢化物的热稳定性由弱到强的依次为
(7)写出元素⑤的单质与元素③最高价氧化物的水化物反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式书写正确的是
A.稀硝酸与过量的铁屑反应: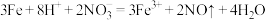 |
B. 和氢氧化钠溶液反应: 和氢氧化钠溶液反应: |
C. 和水反应: 和水反应: |
D.向 溶液中通入 溶液中通入 气体: 气体: |
您最近一年使用:0次
2023-03-12更新
|
500次组卷
|
3卷引用:陕西省汉中市2020-2021学年高二下学期期中联考化学试题
解题方法
10 . 常见金属和非金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)实验室制取氢氧化铝时,常用铝盐溶液和_______ (填“氨水”或“氢氧化钠溶液”)作为原料。
(2)铝制餐具不宜长时间存放酸性、碱性食物,但铝制容器可以盛装浓硝酸的原因是_______ 。
(3)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是_______ (用离子方程式表示)。
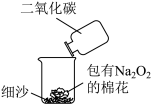
(4)如图实验可用来验证Na2O2与CO2的反应,实验过程中可观察到包有Na2O2的棉花燃烧。写出该反应的化学方程式_______ ,棉花燃烧说明该反应具有的特点是_______ 。
(5)铁红是一种红色颜料,其成分是_______ (填化学式)。将一定量的铁红溶于160 mL5 mol/L的盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24 L (标准状况下),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为_______ g。
(1)实验室制取氢氧化铝时,常用铝盐溶液和
(2)铝制餐具不宜长时间存放酸性、碱性食物,但铝制容器可以盛装浓硝酸的原因是
(3)实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是
(4)如图实验可用来验证Na2O2与CO2的反应,实验过程中可观察到包有Na2O2的棉花燃烧。写出该反应的化学方程式

(5)铁红是一种红色颜料,其成分是
您最近一年使用:0次



