陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
陕西
高一
期末
2024-03-19
59次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学与STSE、化学实验基础、化学反应原理、有机化学基础
陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
陕西
高一
期末
2024-03-19
59次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学与STSE、化学实验基础、化学反应原理、有机化学基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
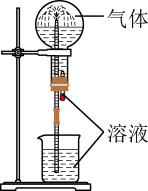
1. 在2020年初抗击新冠病毒感染的肺炎(Covid-19)疫情中,化学品发挥了重要的作用。下列说法正确的是
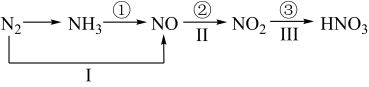
| A.制备“84消毒液”时的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O |
| B.“84消毒液”的有效成分是NaClO |
| C.Cl2、ClO2和O3均可用于自来水消毒 |
| D.将氯气通入澄清的石灰水中可制得漂白粉,漂白粉的有效成分是Ca(ClO)2,可作纸张的漂白剂 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
2. 设NA代表阿伏加德罗常数的值,下列说法正确的是
| A.6.4g铜与足量稀硫酸反应生成氢气转移的电子数为0.2NA |
| B.0.5molNO2与11.2LO3所含的分子数均为0.5NA |
| C.1molNa与足量O2反应,生成Na2O和Na2O2混合物,钠得到电子总数为NA |
| D.101kPa、4℃时,18mL水和202kPa、27℃时32gO2所含分子数均为NA |
您最近一年使用:0次
2021-08-21更新
|
352次组卷
|
4卷引用:四川省绵阳中学2020-2021学年高一上学期期中考试化学试题
单选题
|
适中(0.65)
解题方法
3. 室温下,下列各组离子在指定溶液中能大量共存的是
A.澄清透明的溶液中:Cu2+、Fe3+、Cl-、SO |
| B.pH=2的溶液中:Ca2+、Fe2+、ClO-、Br- |
C.0.1mol•L-1的HI溶液中:Na+、K+、MnO 、CO 、CO |
D.含有大量CO 的溶液中:NH 的溶液中:NH 、H+、NO 、H+、NO 、ClO 、ClO |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
4. 某无色、澄清溶液中可能含有①Na+、②SO 、③Cl-、④HCO
、③Cl-、④HCO 、⑤CO
、⑤CO 、⑥H+、⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
、⑥H+、⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是
 、③Cl-、④HCO
、③Cl-、④HCO 、⑤CO
、⑤CO 、⑥H+、⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
、⑥H+、⑦Cu2+中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:| 步骤 | 操作 | 现象 |
| (1) | 用紫色石蕊试液检验 | 溶液变红 |
| (2) | 向溶液中滴加BaCl2和稀HCl | 有白色沉淀生成 |
| (3) | 将(2)中所得混合物过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀生成 |
| A.肯定含有的离子是②③⑥ | B.该实验无法确定是否含有③ |
| C.可能含有的离子是①③⑦ | D.肯定没有的离子是④⑤,可能含有的离子是② |
您最近一年使用:0次
2021-11-16更新
|
971次组卷
|
20卷引用:河南郑州新密市第六高级中学2020-2021学年高一12月月考化学试题
河南郑州新密市第六高级中学2020-2021学年高一12月月考化学试题(已下线)2.2.2 离子方程式的书写-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)四川省成都市树德中学2021-2022学年高一上学期10月阶段性测试化学试题四川省成都外国语学校2021-2022学年高一上学期期中化学试题四川省仁寿县第二中学2021-2022学年高一11月质量检测化学试题河北省石家庄市藁城区第一中学2021-2022学年高一上学期第一次月考化学试题河北省张家口市宣化第一中学2021-2022学年高一下学期3月月考化学试题(已下线)第一章 物质及其变化(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)江苏省泰州中学2022-2023学年高一上学期第一次月考化学试题广东省江门市第一中学2022-2023学年高一上学期第一次月考化学试题山东省莒南第一中学2022-2023学年高一上学期期中考试化学试题浙江省温州新力量联盟2022-2023学年高一上学期期中联考 化学试题【2022】【高一上】【杭师大附中】【期中考】【高中化学】【徐外兰收集】【2022】【高一上】【杭四下沙】【期中考】【高中化学】【陈光收集】江西省宜丰中学2022-2023学年高一下学期第3次月考化学试题贵州省“三新”改革联盟校2022-2023学年高一上学期联考(三)化学试题(已下线)专题02 离子反应【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)河南省实验中学2023-2024学年高一上学期期中考试 化学试题河南省新乡市原阳县第一高级中学2023-2024学年高一上学期12月月考化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
解题方法
5. 已知有如下反应:①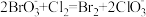 ②
② +5Cl—+6H+=3Cl2+3H2O③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )
+5Cl—+6H+=3Cl2+3H2O③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )
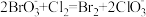 ②
② +5Cl—+6H+=3Cl2+3H2O③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )
+5Cl—+6H+=3Cl2+3H2O③2FeCl2+Cl2=2FeCl3 。根据上述反应,判断下列结论中错误的是( )| A.Cl2在反应②中既是氧化产物又是还原产物 |
| B.Cl2在①、③反应中均作氧化剂 |
C.氧化性强弱的顺序为: > > > Cl2 >Fe3+ > Cl2 >Fe3+ |
D.溶液中可发生: +6Fe2++6H+=Cl—+6Fe3++3H2O +6Fe2++6H+=Cl—+6Fe3++3H2O |
您最近一年使用:0次
2020-10-17更新
|
779次组卷
|
41卷引用:2016-2017学年江西省南昌市第十中学高一上学期期末考试化学试卷
2016-2017学年江西省南昌市第十中学高一上学期期末考试化学试卷安徽省六安市第一中学2018届高三9月月考化学试题云南省曲靖市第一中学2018届高三上学期第三次月考化学试题江西省临川实验学校2017-2018学年高一上学期期末质量检测化学试题重庆一中2017-2018学年高一上学期期末化学试题重庆一中2017-2018学年高一上学期期末考试化学试题四川省广安友谊中学2018-2019学年高一上学期期末模拟化学试题【市级联考】北京市2018 -2019学年高一上学期期末质量检测模拟化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高一上学期期末考试化学试题湖南省醴陵市第一中学2018-2019学年高一上学期期末考试化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高一下学期开学考试化学试题黑龙江省大庆市铁人中学2019-2020学年高一上学期期中考试化学试题四川省成都市双流棠湖中学2019-2020学年高一下学期第一次在线月考化学试题广东省珠海市2019-2020学年高一上学期期末考试化学试题四川省乐山市第四中学高一下学期第一次月考化学试题四川省阆中中学2019-2020学年高一下学期开学考试化学试题山西省临猗县临晋中学2020-2021学年高一9月月考化学试题吉林省(长春市)榆树市第一高级中学2021届高三10月月考化学试题江苏省盐城市一中、射阳中学等五校2020-2021学年高一上学期期中联考化学试题山东省日照市莒县2020-2021学年高一11月模块考试化学试题(已下线)【苏州新东方】01 吴江区 震泽 杨班河北省石家庄市第一中学2021-2022学年高一上学期第一次学情反馈化学试题广东省广州市禺山高级中学2021-2022学年高一上学期期中考试化学试题云南省丘北县第一中学2021-2022学年高一下学期3月份考试 化学试题云南省玉溪市通海县第三中学2021-2022学年高一上学期期末考试化学试题山西省晋城市第一中学校2022-2023学年高一上学期第二次调研考试化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期期中线上考试化学试题广东省广州市第七中学2022-2023学年高一上学期期中考试化学试题甘肃省兰州西北师范大学附属中学2022-2023学年高一上学期期中考试化学试题内蒙古包头市第九中学2022-2023学年高一上学期10月月考化学试题湖北省襄阳市第五中学2022-2023学年高一上学期12月月考化学试题山东省济宁市第一中学2022-2023学年高一上学期期末教学质量线上测试化学试题甘肃省民勤县第一中学2022-2023学年 高一下学期开学考试化学试题江西省宜丰中学2022-2023学年高一下学期第3次月考化学试题广东省广州市第七中学2022-2023学年高一上学期期中考试化学试题甘肃省西北师范大学附属中学2022-2023学年高一上学期第一次月考化学试题广东省广州市禺山高级中学2023-2024学年高一上学期期中考试化学试题四川省遂宁市射洪中学校2023-2024学年高一上学期10月月考化学试题河北省石家庄市新乐市第一中学2023-2024学年高一上学期期中考试化学试题四川省眉山市东坡区部分学校2023-2024学年高一上学期11月期中联考化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
6. 下列说法正确的是
| A.氯气有毒,所以不能用于制造农药、染料和药品等 |
| B.钢铁的密度大,强度高,具有较强的抗腐蚀能力 |
| C.液态钠可用作核反应堆的传热介质 |
| D.二氧化硅可直接用于制造计算机芯片 |
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
7. 甲、乙两烧杯中分别盛有200mL浓度均为2mol/L的盐酸与NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得同温同压下生成气体的体积之比为2:5
| A.2.7g | B.3.6g | C.5.4g | D.9.0g |
您最近一年使用:0次
单选题
|
较易(0.85)
8. 下列反应中有+3价铁元素生成的是
①铁丝在空气中生锈
②向FeCl2溶液中通入足量氯气
③将铁片置于CuSO4溶液中
④Fe(OH)2暴露在空气中
⑤FeSO4溶液中滴加过氧化氢
⑥高温下铁与水蒸气反应
①铁丝在空气中生锈
②向FeCl2溶液中通入足量氯气
③将铁片置于CuSO4溶液中
④Fe(OH)2暴露在空气中
⑤FeSO4溶液中滴加过氧化氢
⑥高温下铁与水蒸气反应
| A.①②③④⑤ | B.②③④⑤ | C.①②④⑤⑥ | D.①②③④⑤⑥ |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
9. 向氧化铁、氧化铜、铁、铜的混合粉末中加入过量的稀盐酸,充分反应后,仍有红色粉末存在
| A.只有Fe2+和Cu2+ |
| B.一定有Fe2+、Cu2+,可能有Fe3+ |
| C.一定有Fe2+,可能有Cu2+ |
| D.只有Fe2+ |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
10. 下列有关物质的性质与用途的描述错误的是
| A.Al具有良好的延展性,故铝可用于制作铝金属制品 |
| B.镁铝合金的密度大、强度高,是制造飞机和宇宙飞船的理想材料 |
| C.Al、Al2O3均能与酸、碱反应,因此铝制炊具不宜用来蒸煮酸性或碱性食物 |
| D.“蛟龙号”载人潜水器的耐压球壳是用钛合金制造的,合金具有硬度大等优点 |
您最近一年使用:0次
2021-12-17更新
|
1623次组卷
|
12卷引用:河北省百所学校大联考2021-2022学年高一12月联考化学试题
河北省百所学校大联考2021-2022学年高一12月联考化学试题(已下线)第三章 铁 金属材料(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)辽宁省渤海大学附属高级中学2021-2022学年高一上学期期末质量检测化学试题河北省保定市唐县第一中学2022-2023学年高一上学期第三次考试化学试题河北省定州市第二中学2022-2023学年高一上学期12月月考化学试题甘肃省兰州第一中学2022-2023学年高一上学期期末考试化学试题甘肃省兰州第一中学2022-2023学年高一上学期期末考试化学试题广东省深圳市光明区2022-2023学年高一下学期开学考试化学试题(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)安徽省马鞍山市第二十二中学2022-2023学年高一下学期2月月考化学试题新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
11. 某化学教师为“氯气与金属钠反应”设计了如图装置的实验(夹持、加热装置已略),实验操作:先给钠预热,等钠熔融成圆球时,通入氯气,即可见钠着火燃烧
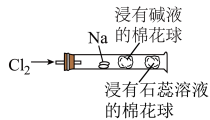

| A.反应生成大量白烟是因为生成氯化钠 |
| B.塞一团浸有碱液的棉球是用于吸收过量的氯气,以免其污染空气 |
| C.钠熔点高,所以先预热再反应 |
| D.可据浸有石蕊溶液的棉花球的颜色变化判断氯气是否被碱液完全吸收 |
您最近一年使用:0次
单选题
|
较易(0.85)
12. 维生素C又称“抗坏血酸”,能将食物中摄取的不易吸收的Fe3+转化为易吸收的Fe2+,下列有关分析错误的是
| A.维生素C具有还原性 |
| B.Fe3+转化为Fe2+发生了还原反应 |
| C.K3[Fe(CN)6]溶液可用于检验Fe3+ |
| D.向Fe3+的溶液中加入Fe或Cu,也能将Fe3+转化为Fe2+ |
您最近一年使用:0次
2021-07-15更新
|
397次组卷
|
3卷引用:四川省成都市2020-2021学年高二下学期期末考试(2022届零诊)化学试题
单选题
|
适中(0.65)
13. 将4.3gNa、Na2O、Na2O2的混合物与足量水反应,在标准状况下得到672ml混合气体,将该混合气体通过放电恰好反应,则原混合物中Na、Na2O、Na2O2的物质的量之比为
| A.1:2:1 | B.1:1:1 | C..1:3:1 | D.4:3:2 |
【知识点】 化学方程式中物质的量的运用解读 过氧化钠 过氧化钠与水的反应解读
您最近一年使用:0次
2016-12-09更新
|
331次组卷
|
4卷引用:2017届辽宁省铁岭市高三上学期第一次联考化学试卷
14. 某废催化剂含SiO2、ZnS、CuS及少量的Fe3O4.某实验小组以该废催化剂为原料,回收锌和铜,设计实验流程如图:
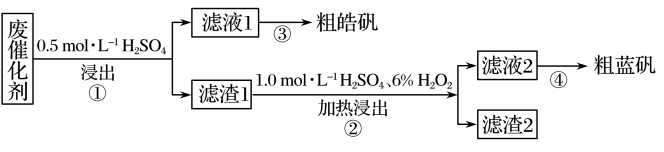
下列说法正确的是

下列说法正确的是
| A.步骤①操作中,生成的气体可用CuSO4溶液吸收 |
| B.检验滤液1中是否含有Fe2+,可以选用KSCN和新制的氯水 |
| C.步骤②操作中,应先加6% H2O2,然后加入1.0mol·L -1H2SO4 |
| D.滤渣1和滤渣2均含有H2SiO3胶体,进一步加工可获得硅胶 |
【知识点】 二氧化硅 铁盐与亚铁盐鉴别试剂的选择解读 物质分离、提纯综合应用解读
您最近一年使用:0次
2021-08-13更新
|
780次组卷
|
10卷引用:广东省华附、省实、广雅、深中2021届高三四校联考化学试题
广东省华附、省实、广雅、深中2021届高三四校联考化学试题(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点30 物质的分离、提纯和检验-备战2022年高考化学一轮复习考点帮(浙江专用)广州大学附属东江中学2021届高三一模考试模拟测试化学试题广东省普宁二中实验学校2021-2022学年高三上学期第一次月考化学试题广东省梅州市东山中学2021-2022学年高三上学期期中考试化学试题山东省济宁市兖州区2021-2022学年高三上学期期中考试化学试题(已下线)押广东卷化学第10题 元素及其化合物-备战2022年高考化学临考题号押题(广东卷)(已下线)专题06 物质的转化-备战2023年高考化学母题题源解密(广东卷)陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
较易(0.85)
15. 下列物质性质与用途对应关系正确的是
| 性质 | 用途 | |
| A |  具有氧化性 具有氧化性 | 漂白纸浆 |
| B |  溶液呈弱碱性 溶液呈弱碱性 | 防火材料 |
| C |  溶液具有氧化性 溶液具有氧化性 | 蚀刻铜制电路板时作为“腐蚀液” |
| D |  具有弱酸性 具有弱酸性 | 蚀刻玻璃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-16更新
|
78次组卷
|
2卷引用:湖南省郴州市2020-2021学年高二下学期期末考试化学试题
16. 化学无处不在,与人类生产、生活联系密切。下列与化学有关的说法错误的是
A.王安石诗:雷蟠电掣云滔滔,夜半载雨输亭皋,涉及反应:N2+O2 2NO 2NO |
| B.北科大参与研发的“超级钢”(含Mn10%、C0.47%、V0.7%等)是一种新型合金 |
| C.生活中制作油条的口诀是“一碱、二矾、三钱盐”,其中的“碱”是纯碱 |
| D.中国古代常用竹简、丝帛记载文字,二者的主要成分均为蛋白质 |
【知识点】 自然界氮的固定解读 盐类水解的应用 蛋白质 金属材料的性质及利用
您最近一年使用:0次
2021-04-20更新
|
443次组卷
|
3卷引用:河北省保定市2021届高三第一次模拟考试化学试题
河北省保定市2021届高三第一次模拟考试化学试题(已下线)考向08 金属材料 金属的冶炼-备战2022年高考化学一轮复习考点微专题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
解题方法
17. 下列物品使用了SiO2的是
①陶瓷餐具②玛瑙手镯③太阳能电池帆板④石英钟⑤手机芯片⑥钻石项链
①陶瓷餐具②玛瑙手镯③太阳能电池帆板④石英钟⑤手机芯片⑥钻石项链
| A.③⑤ | B.①⑥ | C.②④ | D.①②③ |
您最近一年使用:0次
2024-03-08更新
|
293次组卷
|
2卷引用:陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
解题方法
18. 下列说法不正确的是
| A.玻璃、水泥、陶瓷是三大传统的无机非金属材料 |
B.工业上用焦炭还原石英砂制取粗硅原理:SiO2+2C Si+2CO↑ Si+2CO↑ |
| C.海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等 |
| D.绿色化学的核心思想就是先污染后用化学方法治理 |
【知识点】 硅的制备解读 含硅的无机非金属材料解读 绿色化学与可持续发展解读 海水淡化解读
您最近一年使用:0次
单选题
|
较易(0.85)
解题方法
19. 已知常温下,浓盐酸与高锰酸钾反应可以生成氯气。如图甲、乙、丙三处分别是沾有NaBr溶液的棉花、润湿的淀粉-KI试纸、润湿的品红试纸,下列说法正确的是
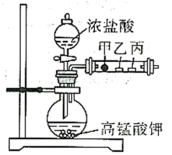

A.该实验通过现象可以证明氧化性: |
| B.沾有品红溶液的试纸会褪色,若再对丙微热则恢复红色 |
C.甲的现象也可以证明 的还原性强于 的还原性强于 |
D. 与NaBr溶液反应的实质与 与NaBr溶液反应的实质与 与NaBr溶液反应类似 与NaBr溶液反应类似 |
您最近一年使用:0次
2021-07-13更新
|
512次组卷
|
4卷引用:河南省信阳市2020-2021学年高一下学期期末教学质量检测化学试题
河南省信阳市2020-2021学年高一下学期期末教学质量检测化学试题专题八 原子结构与元素周期表(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)第四章 物质结构 元素周期律(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
适中(0.65)
名校
20. 下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
①氯气 ②液氯 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸 ⑥盐酸酸化的漂白粉溶液
①氯气 ②液氯 ③新制氯水 ④氯气的酒精溶液 ⑤盐酸 ⑥盐酸酸化的漂白粉溶液
| A.①②③ | B.①②③⑥ | C.③⑥ | D.③④⑥ |
您最近一年使用:0次
2018-04-09更新
|
737次组卷
|
15卷引用:2012届福建省福州市罗源一中高三上学期第一次月考化学试卷
(已下线)2012届福建省福州市罗源一中高三上学期第一次月考化学试卷河北省鸡泽县第一中学2017-2018学年高一上学期期中考试化学试题山东省桓台第二中学2017-2018学年高一4月月考化学试题【全国百强校】山东省新泰市新泰一中2018-2019学年高一上学期第一次质量检测化学试题北京清华附中2019-2020高一化学上学期期中试题天津市耀华中学2019-2020学年高一下学期第一次月考化学试题苏教版(2020)高一必修第一册专题3第一单元课时2 氯气的性质及应用人教版(2019)高一必修第一册 第二章 第二节课时1 氯气的性质鲁科版(2019)高一必修第一册第1章 认识化学科学 第2节 研究物质性质的方法 课时2 研究物质性质的基本程序黑龙江省哈尔滨师范大学附属中学2020-2021学年高一上学期期中考试化学试题湖南省/(常德市芷兰实验中学2020-2021学年高一上学期第二次月考化学试题云南省昭通市昭阳区第一中学2020-2021学年高一上学期第三次月考化学试题(已下线)第6讲 海水中的氯-2020-2021学年秋季班高一上学期教材知识点精讲练(沪科版)(已下线)专题05 氯及其化合物【考点清单】(讲+练)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
单选题
|
容易(0.94)
真题
名校
21. 化学与环境密切相关,下列有关说法正确的是
| A.CO2属于大气污染物 |
| B.酸雨是pH小于7的雨水 |
| C.CO2、NO2或SO2都会导致酸雨的形成 |
| D.大气中CO2含量的增加会导致温室效应加剧 |
您最近一年使用:0次
2016-12-09更新
|
4453次组卷
|
36卷引用:2014届福建省厦门一中高三上学期期中考试化学试卷
(已下线)2014届福建省厦门一中高三上学期期中考试化学试卷2012年普通高等学校招生全国统一考试化学(海南卷)云南省彝良县一中2018-2019学年高一上学期12月考试化学试题【全国百强校】北京四中2018-2019学年高一下学期期中测试化学试题备战2020高考化学二轮专项训练:化学与生活云南省普洱市澜沧县第一中学2019-2020学年高一上学期期末考试化学试题黑龙江省哈尔滨市第三十二中学2019-2020学年高一下学期期中考试化学试题山西省朔州市怀仁市第一中学2019—2020学年高一下学期第一次月考化学试题云南省昆明市官渡区第一中学2019-2020学年高二下学期开学考试化学试题湖南省益阳市桃江县2019-2020学年高一下学期期末考试化学试题四川省射洪中学校2020-2021学年高二上学期开学考试化学试题人教版2019必修第二册 第五章 本章达标检测甘肃省天水市第一中学2020-2021学年高一下学期第一阶段考试化学(理)试题湖南省常德市一中2020-2021学年高一下学期期中考试化学试题山西省大同市浑源县第七中学2020-2021学年高一下学期第一次月考化学试题福建省莆田第二中学2019~2020学年高一下学期4月线上月考化学试题吉林省长春市第二十中学2020-2021学年高一下学期期末考试化学试题河北省张家口市第一中学2021-2022学年高二上学期开学检测化学试题广东省惠州市第一中学2021-2022学年高二上学期第二次考试化学试题广东省惠州市第一中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2020-2021学年高二上学期期中考试化学(文)试题(已下线)课后-8.3 环境保护与绿色化学-人教2019必修第二册海南省儋州川绵中学2021-2022学年高一下学期期中考试(合格考)化学试题甘肃省兰州市教育局第四片区2021-2022学年高一下学期期中考试化学试题湖南省邵阳市新邵县2021-2022学年高一下学期期末质量检测化学试题(已下线)第23练 环境保护与绿色化学-2023年高考化学一轮复习小题多维练(全国通用)海南省儋州川绵中学2021-2022学年高一下学期第一次月考化学试题安徽省合肥市肥东县综合高中2021-2022学年高一下学期期中考试化学试题河南省许昌市鄢陵县职业教育中心2021-2022学年高一下学期期中考试(普高)化学试题河南省灵宝市第五高级中学2021-2022学年高一下学期第一次月考化学试题广东省汕尾市华大实验学校2022-2023学年高一下学期3月月考化学试题上海市第三女子中学2023-2024学年高二上学期期末化学合格考试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题内蒙古赤峰市元宝山区第一中学、新红旗中学联考2023-2024学年高一下学期4月月考化学试题湖北省仙桃市汉江中学2023-2024学年高一下学期期中考试化学试题四川省泸州市龙马潭区2023-2024学年高一下学期5月期中考试化学试题
单选题
|
适中(0.65)
22. 利用下图所示方法可防治含硫煤燃烧产生的污染,同时可得到化工产品。下列说法错误的是


| A.该方法可得到化工产品H2SO4 |
| B.该过程中每吸收11.2LSO2,同时产生2molFe2+ |
| C.该过程中化合价发生改变的元素有Fe、O和S |
D.图中涉及到的反应之一为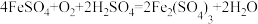 |
【知识点】 二氧化硫与氧气的反应解读 化学反应原理综合考查解读
您最近一年使用:0次
2021-07-12更新
|
436次组卷
|
2卷引用:山东省日照市2020-2021学年高一下学期期末校际联合考试化学试题
单选题
|
适中(0.65)
解题方法
23. 将SO2分别通入下列四种溶液,根据实验现象所得结论正确的是
| 选项 | 溶液 | 现象 | 结论 |
| A | 溴水溶液 | 溴水褪色 | SO2具有漂白性 |
| B | H2S溶液 | 出现淡黄色浑浊 | SO2具有氧化性 |
| C | BaCl2溶液 | 无明显变化 | BaSO4能溶于水 |
| D | H2O2溶液 | 无明显变化 | SO2和H2O2溶液不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易(0.85)
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
26. 某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
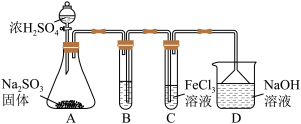
(1)通入足量SO2时C中观察到的现象为____ 。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式___ ;
②C装置中所盛装的FeCl3溶液为5mL,物质的量浓度为2.0mol·L-1,欲使其完全被SO2还原,则至少需要Na2SO3固体___ g;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO 。该做法
。该做法___ (填“合理”或“不合理”),理由是___ 。
(3)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有___(填序号)。

(1)通入足量SO2时C中观察到的现象为
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式
②C装置中所盛装的FeCl3溶液为5mL,物质的量浓度为2.0mol·L-1,欲使其完全被SO2还原,则至少需要Na2SO3固体
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO
 。该做法
。该做法(3)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有___(填序号)。
| A.浓硫酸 | B.酸性KMnO4溶液 | C.碘水 | D.NaCl溶液 |
您最近一年使用:0次
2020-06-21更新
|
218次组卷
|
3卷引用:吉林省长春市实验中学2019-2020学年高一下学期期中考试化学试题
(已下线)吉林省长春市实验中学2019-2020学年高一下学期期中考试化学试题吉林省长春市实验中学2019-2020学年高一下期中考试化学试题陕西省延安市新区高级中学2021-2022学年高一上学期期末考试化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
27. 亚硝酸钠(NaNO2)有毒、有咸味,外形与食盐相似,人若误食会引起中毒。某兴趣小组欲研究亚硝酸钠,查阅资料得到如表信息。试根据信息回答下列问题:
(1)已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,则该反应中氧化剂是 _______ ;若有0.75mol电子发生转移,则被氧化的还原剂的粒子数为 _______ (用NA表示阿伏加德罗常数的值)。
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
(3)下列方法中,可用来区分NaNO2和NaCl的是 _______ (填序号)。
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式_______ 。
| 药品 | NaNO2(亚硝酸钠) |
| 性质 | 在酸性溶液中有较强氧化性,能将Fe2+氧化成Fe3+。 |
(2)人若误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,可服用维生素C解毒。下列说法错误的是 _______(填序号)。
| A.NaNO2被还原 |
| B.维生素C具有还原性 |
| C.还原性:维生素C>Fe2+ |
| D.NaNO2是还原剂 |
A.焰色反应
B.滴加酸化的FeSO4溶液和KSCN溶液
C.在酸性条件下加入淀粉KI溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-无机推断题
|
适中(0.65)
28. 已知常温下B、D、E、L为密度比空气大的气体,D、E为单质,其他为化合物。A是一种淡黄色固体,F、G均能与L的水溶液反应放出B.据如图反应框图填空。

(1)F的俗名是_______ ,B分子式为 _______ ,工业上利用反应③生产 _______ 。(填名称)
(2)反应④的离子方程式为_______ 。
(3)有一种单质能与H反应生成E,该反应的化学方程式为_______ 。
(4)某酸性氧化物气体M溶于水具有漂白作用,既有氧化性,又有还原性,与D在溶液中反应的离子方程式为_______ 。

(1)F的俗名是
(2)反应④的离子方程式为
(3)有一种单质能与H反应生成E,该反应的化学方程式为
(4)某酸性氧化物气体M溶于水具有漂白作用,既有氧化性,又有还原性,与D在溶液中反应的离子方程式为
您最近一年使用:0次
五、计算题 添加题型下试题
计算题
|
适中(0.65)
29. 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为_______ 。
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为_______ 克。
(3)此时,被氧化HCl的物质的量为_______ 。
(1)质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为
(2)若要制取2.24L Cl2(标准状况),理论上需要消耗MnO2质量为
(3)此时,被氧化HCl的物质的量为
【知识点】 物质的量有关计算 物质的量浓度的基础计算解读 氯气的实验室制法解读
您最近一年使用:0次
计算题
|
适中(0.65)
解题方法
30. 将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
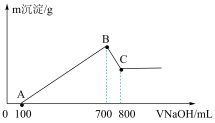
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、认识化学科学、化学与STSE、化学实验基础、化学反应原理、有机化学基础
试卷题型(共 30题)
题型
数量
单选题
25
解答题
2
填空题
1
计算题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 次氯酸及其性质 漂白粉和漂粉精 氯气与碱溶液反应 漂白粉和漂粉精的制备原理 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 气体物质与NA相关的推算 氧化还原反应与NA相关推算 | |
| 3 | 0.65 | 限定条件下的离子共存 氧化还原反应的规律 次氯酸及其性质 卤素离子 | |
| 4 | 0.65 | 离子反应的实际应用 限定条件下的离子共存 离子反应在化合物组成的分析、鉴定的应用 | |
| 5 | 0.65 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 6 | 0.85 | 氯气的化学性质 硅的物理性质与用途 二氧化硅的用途 金属与合金性能比较 | |
| 7 | 0.85 | 化学方程式中物质的量的运用 铝与酸溶液反应 铝与强碱溶液反应 | |
| 8 | 0.85 | 氢氧化亚铁 铁与非金属单质反应 铁与水蒸气的反应 Fe2+的还原性 | |
| 9 | 0.65 | 氧化性、还原性强弱的比较 Fe、Cu及相关离子的反应 | |
| 10 | 0.85 | 铝与酸溶液反应 铝与强碱溶液反应 氧化铝与酸反应 氧化铝与碱溶液反应 | |
| 11 | 0.65 | 氯气与金属单质的反应 氯气与碱溶液反应 氯水的性质 钠的物理性质 | |
| 12 | 0.85 | 氧化还原反应的应用 氧化还原反应在生活、生产中的应用 铁盐 Fe3+与其他物质氧化性强弱关系 | |
| 13 | 0.65 | 化学方程式中物质的量的运用 过氧化钠 过氧化钠与水的反应 | |
| 14 | 0.65 | 二氧化硅 铁盐与亚铁盐鉴别试剂的选择 物质分离、提纯综合应用 | |
| 15 | 0.85 | 二氧化硫 二氧化硅 硅酸与硅酸盐 印刷电路板 | |
| 16 | 0.85 | 自然界氮的固定 盐类水解的应用 蛋白质 金属材料的性质及利用 | |
| 17 | 0.94 | 硅的物理性质与用途 二氧化硅的用途 硅酸盐工业 | |
| 18 | 0.65 | 硅的制备 含硅的无机非金属材料 绿色化学与可持续发展 海水淡化 | |
| 19 | 0.85 | 氧化性、还原性强弱的比较 次氯酸及其性质 溴、碘的性质 物质性质的探究 | |
| 20 | 0.65 | 氯气的化学性质 氯水的性质 | |
| 21 | 0.94 | 硫的氧化物对人体、环境的危害 酸雨 大气污染的治理原理及方法 | |
| 22 | 0.65 | 二氧化硫与氧气的反应 化学反应原理综合考查 | |
| 23 | 0.65 | 二氧化硫的漂白性 二氧化硫的弱氧化性 二氧化硫与其他强氧化剂的反应 | |
| 24 | 0.85 | 氨的喷泉实验 | |
| 25 | 0.65 | 物质的转化 氨气 硝酸 自然界氮的固定 | |
| 二、解答题 | |||
| 26 | 0.65 | 二氧化硫的化学性质 二氧化硫的制备 硫酸根离子的检验 | 实验探究题 |
| 28 | 0.65 | 无机综合推断 次氯酸及其性质 二氧化硫 过氧化钠与水的反应 | 无机推断题 |
| 三、填空题 | |||
| 27 | 0.65 | 氧化还原反应的几组概念 氧化性、还原性强弱的比较 氧化还原反应方程式的书写与配平 焰色试验 | |
| 四、计算题 | |||
| 29 | 0.65 | 物质的量有关计算 物质的量浓度的基础计算 氯气的实验室制法 | |
| 30 | 0.65 | 物质的量浓度的计算 化学方程式中物质的量的运用 氢氧化铝与强碱反应 | |