下列各组离子在给定条件的溶液中一定能大量共存的是
A.在强酸性溶液中:Fe2+ 、K+ 、 Cl-、 |
B.加入铝粉有大量氢气产生的溶液中:Na+ 、Ca2+ 、Br- 、 |
C.在无色溶液中: 、 、 、K+、Cl-、Na+ 、K+、Cl-、Na+ |
D.滴入酚酞显红色的溶液中:K+、 Na+ 、 、 、 |
更新时间:2024-05-11 10:06:26
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是
A.滴加石蕊试液显红色的溶液:Fe3+、NH 、Cl-、SCN- 、Cl-、SCN- |
B.pH为1的溶液:Cu2+、Na+、Mg2+、NO |
C.pH为13的溶液:K+、HCO 、Br-、Ba2+ 、Br-、Ba2+ |
D.所含溶质为Na2SO4的溶液:K+、AlO 、NO 、NO 、Al3+ 、Al3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是( )
| A.常温下,向pH为2的盐酸中加入等体积的pH=12的氨水恰好完全中和 |
| B.Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 |
| C.0.2 mol•L-1与0.1 mol•L-1醋酸中c(H+)之比为2:1 |
| D.pH=1的溶液中NH4+、Cl-、Cu2+、SO42-一定能大量共存 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有一瓶Na2SO3溶液,可能部分被氧化,某同学进行如下实验:取少量此溶液,滴入Ba(NO3)2溶液产生白色沉淀,再加入足量稀盐酸,充分振荡后仍有白色沉淀,对此实验下列结论正确的是
| A.加入盐酸后的不溶沉淀可能有BaSO3 |
| B.此实验不能确定Na2SO3是否部分被氧化 |
| C.实验中将Ba(NO3)2换成BaCl2,不影响实验结论 |
| D.实验中若先加稀盐酸酸化,再滴加Ba(NO3)2溶液,可确定Na2SO3是否部分被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列离子方程式书写正确的是
A.向氨水中通入过量二氧化硫: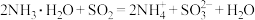 |
B.氢氧化钠溶液与铝反应: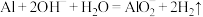 |
C.铁与少量稀硝酸反应: |
D.向亚硫酸钠溶液中通入氯气: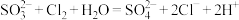 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】现有一块铝铁合金,欲测定其铝的质量分数,切下Wg合金,溶于盐酸中,再加入过量NaOH溶液,滤出沉淀,已知沉淀成分为氢氧化铁,把沉淀在空气中充分灼烧,最后得到Wg红棕色粉末。则此合金中铝的质量分数约为
| A.20% | B.30% | C.70% | D.80% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用相同的铝片、6 mol·L-1稀盐酸、3 mol·L-1稀硫酸、6 mol·L-1氢氧化钠溶液、试管等分别进行表中实验:
对上述实验的相关说法不正确 的是
| 实验方案 | 实验现象 | 实验原理(化学方程式) |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 | Al2O3+6HCl=2AlCl3+3H2O 2Al+6HCl=2AlCl3+3H2↑ |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,铝片表面有少量气泡产生 | Al2O3+3H2SO4=2Al2(SO4)3+3H2O 2Al+3H2SO4=2Al2(SO4)3+3H2↑ |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后铝片逐渐溶解,并有大量气泡产生 | Al2O3+2NaOH=2NaAlO2+H2O 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| A.对比(1)、(2)、(3)中Al2O3参与的反应可得出:Al2O3既有碱性氧化物的某些性质,又有酸性氧化物的某些性质 |
| B.对比(1)、(2)、(3)中气体产生现象和酸碱挥发性可得出:实验(3)最适宜于实验室制备H2 |
| C.对比实验(1)、(2)后来产生气泡的现象,可得出:c(H+)浓度对气泡产生的多少无影响 |
D.对比实验(1)、(2)后来产生气泡的现象,可得出: 对Al与H+的反应可能有阻碍作 对Al与H+的反应可能有阻碍作 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】把铝粉和氧化铁粉配成铝热剂,分成两等份.一份在高温下恰好完全反应后,再与足量盐酸起反应;另一份放入足量的烧碱溶液中充分反应.前后两种情况下生成的气体的质量比是
| A.1:1 | B.2:3 | C.3:2 | D.28:9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列各组离子一定能在指定溶液中大量共存的是
A.使酚酞变红的溶液: |
B.水电离的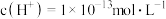 的溶液: 的溶液: |
C.与 反应能放出 反应能放出 的溶液: 的溶液: |
D. 的溶液: 的溶液: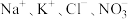 |
您最近一年使用:0次

 、
、 、
、
 、
、 、
、 、
、
 、
、
 、
、
 溶液中滴加少量稀氨水:
溶液中滴加少量稀氨水:
 加入
加入

 溶液中:
溶液中:
 、ClO-、Cl-
、ClO-、Cl- 、Na+、S2O
、Na+、S2O



