黑龙江省齐齐市拜泉县第一中学2021-2022学年高一上学期期中考试化学试题
黑龙江
高一
期中
2022-09-28
113次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用
一、单选题 添加题型下试题
①鸡蛋白溶液 ②水 ③淀粉溶液 ④硫酸溶液 ⑤沸水中滴入饱和FeCl3溶液
| A.②④ | B.③④ | C.②⑤ | D.④ |
| A.液态氧——化合物 | B.食盐水——纯净物 |
| C.Na2O——碱性氧化物 | D.NaHSO4——含氧酸 |
| A.明矾净水时使悬浮颗粒沉淀 |
| B.向煮熟的豆浆中加入卤水可生产出豆腐 |
| C.雾霾天气打手电能看到明显的光柱 |
| D.澄清的石灰水中通入CO2气体,有白色的沉淀产生 |
【知识点】 胶体的性质和应用解读 明矾的净水作用及原理解读
①AgNO3→HNO3 ②Fe2O3→FeCl2 ③Cu→CuCl2 ④Cu(OH)2→CuCl2 ⑤Fe→FeCl3
| A.①② | B.②④ | C.①④ | D.③⑤ |
【知识点】 物质的转化
| A.分散系的稳定性:溶液>胶体>浊液 |
| B.分散质粒子的大小:溶液>胶体>浊液 |
| C.分散质粒子的直径为10-9~10-7 m的分散系是胶体 |
| D.可以用过滤的方法将悬浊液中的分散质从分散剂中分离出来 |
| A.Ca(ClO)2 | B.CaCl2 | C.Ca(ClO)2和CaCl2 | D.HClO |
【知识点】 漂白粉和漂粉精 漂白粉和漂粉精的用途解读
| A.电解质本身不一定能导电 |
| B.溶液中离子数目越多,导电性就越强 |
| C.溶于水后能电离出H+的化合物都是酸 |
| D.电解质在水溶液里或熔融状态下能够导电,说明电解质本身必须含有阴、阳离子 |
【知识点】 非电解质、电解质物质类别判断解读 物质水溶液的导电性解读
| A.C→CO2 | B.CO2→CO |
| C.CuO→Cu | D.H2SO4→BaSO4 |
【知识点】 氧化还原反应的几组概念解读 常见氧化剂与还原剂解读
| A.钠放入水中:Na+2H2O=Na++2OH-+H2↑ |
| B.过量CO2通入澄清石灰水中:CO2+Ca2++2OH-=CaCO3↓+H2O |
| C.盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
| D.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
【知识点】 离子方程式的正误判断解读 钠的化学性质
A.使酚酞变红的溶液中: 、 、 、K+、Na+ 、K+、Na+ |
B.无色透明的溶液中:K+、Fe3+、S2-、 |
C.与铁反应生成氢气的溶液中: 、Cl﹣、K+、Na+ 、Cl﹣、K+、Na+ |
D.使紫色石蕊变红的溶液中:Cl-、Na+、Fe2+、 |
【知识点】 离子共存 限定条件下的离子共存解读
| A.实验后剩余少量钠粒可放回原试剂瓶中 | B.用一般的化学方法不能制取金属钠 |
| C.自然界中无游离态的钠存在 | D.钠在空气中燃烧生成氧化钠 |
【知识点】 钠的化学性质 钠单质的保存与用途解读 钠与氧气等非金属的反应解读
| A.加热,观察是否有气体放出 |
| B.溶于水后加BaCl2,看有无沉淀 |
| C.溶于水后加石灰水,看有无沉淀 |
| D.取固体试样加盐酸,看是否有气泡产生 |
【知识点】 碳酸钠与碳酸氢钠鉴别的实验解读
| A.氢气和氯气混合光照制氯化氢 | B.金属钠在氯气中燃烧制氯化钠 |
| C.氯气通入澄清石灰水中制漂白粉 | D.高温分解石灰石制生石灰 |
【知识点】 氯气的化学性质 氯气的用途解读 漂白粉和漂粉精的制备原理解读
| A.将NaHCO3固体加入新制氯水,有气泡产生(H+) |
| B.使红色布条褪色(HCl) |
| C.向FeCl2溶液中滴加氯水,溶液变黄色(Cl2) |
| D.滴加AgNO3溶液生成白色沉淀(Cl-) |
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应
②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应
④氢氧化钡溶液与稀硫酸反应
| A.①② | B.①②④ | C.②③ | D.①②③ |
【知识点】 离子反应的发生条件解读 离子方程式的正误判断解读
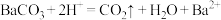 中的
中的 能代表的物质是
能代表的物质是①
 ②
② ③
③ ④
④ ⑤
⑤
| A.①③ | B.①④⑤ | C.②④⑤ | D.①⑤ |
【知识点】 离子反应的发生及书写 离子方程式的正误判断解读
| A.只有① | B.只有② | C.①和② | D.②和③ |
【知识点】 氧化性、还原性强弱的比较解读
A. |
B.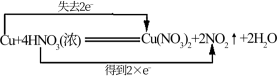 |
C.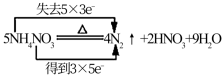 |
D.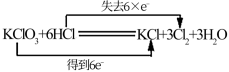 |
【知识点】 单线桥、双线桥分析氧化还原反应解读
| A.钠与氧气反应时,产物是由氧气的用量决定的 |
| B.在饱和Na2CO3溶液中通入足量CO2有沉淀析出 |
| C.用洁净的铂丝蘸取溶液放在酒精灯火焰上灼烧,焰色为黄色,则该溶液为钠盐溶液 |
| D.7.8gNa2O2和6.2gNa2O分别溶于100g水中,所得溶液中溶质的质量分数:前者大于后者 |
| A.42% | B.58% | C.29% | D.50% |
【知识点】 碳酸钠、碳酸氢钠混合物的有关求算解读
二、填空题 添加题型下试题
【知识点】 氧化还原反应的几组概念解读 氧化还原反应的规律解读
 、④干冰、⑤液氯、⑥
、④干冰、⑤液氯、⑥ 粉末、⑦稀硫酸、⑧
粉末、⑦稀硫酸、⑧ 胶体、⑨
胶体、⑨ 固体⑩乙醇。回答下列问题:
固体⑩乙醇。回答下列问题:(1)属于电解质的是
(2)属于混合物的是
(3)写出⑨在水中的电离方程式:
(4)
 胶体中分散质粒子直径的范围是
胶体中分散质粒子直径的范围是(1)在3S+6KOH = 2K2S+K2SO3+3H2O中还原剂和氧化剂的质量比
(2)向Ca(HCO3)2溶液中滴加少量的NaOH溶液的离子方程式
【知识点】 离子方程式的书写解读 与氧化剂、还原剂有关的计算解读
 、SO
、SO ,取该溶液进行以下实验:
,取该溶液进行以下实验:①取pH试纸检验,表明溶液呈强酸性
②另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生
③取上述碱性溶液滴加Na2CO3溶液,有白色沉淀生成
请回答下列问题:
(1)原溶液中一定有的离子是
(2)写出③中发生的离子反应
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
三、解答题 添加题型下试题
 5X-+
5X-+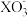 +3H2O”。
+3H2O”。
回答下列问题:
(1)装置中的圆底烧瓶内发生反应的化学方程式为
(2)装置中能否省去盛饱和NaCl溶液的洗气瓶?
(3)装置中能否省去盛浓硫酸的洗气瓶?
(4)装置中能否省去盛冰水的烧杯?
四、填空题 添加题型下试题
【知识点】 氧化还原反应有关计算 与氧化剂、还原剂有关的计算解读
试卷分析
试卷题型(共 27题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 胶体 胶体的定义及分类 胶体的性质和应用 | |
| 2 | 0.94 | 分类方法的应用 无机物质的分类 酸、碱、盐、氧化物的概念及其相互联系 | |
| 3 | 0.85 | 胶体的性质和应用 明矾的净水作用及原理 | |
| 4 | 0.85 | 物质的转化 | |
| 5 | 0.85 | 胶体 分散系概念及其分类 | |
| 6 | 0.94 | 漂白粉和漂粉精 漂白粉和漂粉精的用途 | |
| 7 | 0.85 | 非电解质、电解质物质类别判断 物质水溶液的导电性 | |
| 8 | 0.65 | 氧化还原反应的几组概念 常见氧化剂与还原剂 | |
| 9 | 0.94 | 离子方程式的正误判断 钠的化学性质 | |
| 10 | 0.65 | 离子共存 限定条件下的离子共存 | |
| 11 | 0.94 | 钠的化学性质 钠单质的保存与用途 钠与氧气等非金属的反应 | |
| 12 | 0.65 | 碳酸钠与碳酸氢钠鉴别的实验 | |
| 13 | 0.65 | 氯气的化学性质 氯气的用途 漂白粉和漂粉精的制备原理 | |
| 14 | 0.65 | 氯水的成分及检验 氯水的性质 氯水性质实验探究 | |
| 15 | 0.65 | 离子反应的发生条件 离子方程式的正误判断 | |
| 16 | 0.65 | 离子反应的发生及书写 离子方程式的正误判断 | |
| 17 | 0.65 | 氧化性、还原性强弱的比较 | |
| 18 | 0.65 | 单线桥、双线桥分析氧化还原反应 | |
| 19 | 0.65 | 焰色试验 钠与氧气等非金属的反应 过氧化钠 碳酸钠与碳酸氢钠的相互转化 | |
| 20 | 0.65 | 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 二、填空题 | |||
| 21 | 0.94 | 离子方程式的书写 钠与盐溶液的反应 | |
| 22 | 0.85 | 氧化还原反应的几组概念 氧化还原反应的规律 | |
| 23 | 0.65 | 胶体的定义及分类 胶体的性质和应用 非电解质、电解质物质类别判断 电离方程式 | |
| 24 | 0.65 | 离子方程式的书写 与氧化剂、还原剂有关的计算 | |
| 25 | 0.85 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 27 | 0.65 | 氧化还原反应有关计算 与氧化剂、还原剂有关的计算 | |
| 三、解答题 | |||
| 26 | 0.85 | 氯气的实验室制法 氯气与碱溶液反应 | 实验探究题 |



