解题方法
1 . I.通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:______ (填名称)。
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是______ (填仪器名称),
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为______ (填化学式),装置Ⅰ中反应的化学方程式为____________ ;
(5)该流程中可循环利用的物质是______ (填化学式)
 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
A.① ② ② ③NaOH ③NaOH | B.① ②NaOH③ ②NaOH③ |
C.①NaOH② ③ ③ | D.① ② ② ③NaOH ③NaOH |
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:

| 物质 | NaCl |  |  |  |
| 溶解度 | 36.0 | 21.7 | 9.6 | 37.2 |
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为
(5)该流程中可循环利用的物质是
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案、现象、结论的对应关系错误的是
| 选项 | 操作 | 现象 | 解释 |
| A | 用毛皮摩擦过的带电橡胶棒靠近 液流 液流 |  液流方向不变 液流方向不变 |  分子无极性 分子无极性 |
| B | 将含有稀硫酸的蔗糖溶液水浴加热后,加入新制氢氧化铜悬浊液并加热 | 未产生砖红色沉淀 | 蔗糖未水解 |
| C | 向苯酚悬浊液中加入 溶液 溶液 | 溶液变澄清 | 苯环对羟基有影响 |
| D | 向饱和碳酸钠溶液里通入过量的 | 有晶体析出 |  溶解度小 溶解度小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 用下列各组气体和溶液,能完成喷泉实验的是
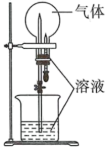
| 选项 | 气体 | 溶液 |
| A |  | 饱和NaCl溶液 |
| B | NO | 稀NaOH溶液 |
| C |  | 饱和 溶液 溶液 |
| D | HCl | 氨水溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式书写正确的是
A.将 滴入酸性 滴入酸性 溶液中: 溶液中: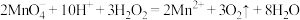 |
B.将少量氯气通入 溶液中: 溶液中: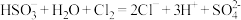 |
C.向 溶液中加入足量稀硝酸: 溶液中加入足量稀硝酸: |
D.过量 通入饱和碳酸钠溶液: 通入饱和碳酸钠溶液: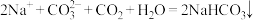 |
您最近一年使用:0次
5 . 侯氏制碱法将氨碱法制取碳酸钠和合成氨相互联合。下列说法不正确的是
A.合成氨工业可为制取碳酸钠提供 |
B.氨碱法将 通入氨的饱和氯化钠溶液 通入氨的饱和氯化钠溶液 |
| C.碳酸钠固体溶于水吸热 |
D. 比 比 热稳定性好 热稳定性好 |
您最近一年使用:0次
6 . 下列表述对应的离子方程式书写正确的是
A.将二氧化硫通入酸性高锰酸钾溶液中: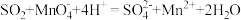 |
B.酸性碘化钾溶液中滴加适量双氧水: |
C.将二氧化碳通入碳酸钠溶液中: |
D.向 溶液中加入足量的NaOH溶液: 溶液中加入足量的NaOH溶液: |
您最近一年使用:0次
7 . 某化学兴趣小组模拟侯氏制碱法制取Na2CO3产品并回收NH4Cl,设计如下实验方案。
Ⅰ.NaHCO3的制备,实验装置如图甲:
②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是_____ 。
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为_____ 。
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体_____ g(保留1位小数)。
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
(5)①回收NH4Cl时加入氨水的目的是_____ 。
②结合图乙,简单说明操作b的过程_____ 。
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量_____ (填“大于”、“小于”或“等于”)理论上生成Na2CO3的质量。
Ⅰ.NaHCO3的制备,实验装置如图甲:

②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
| A.308K | B.373K | C.421K | D.573K |
(5)①回收NH4Cl时加入氨水的目的是
②结合图乙,简单说明操作b的过程
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量
您最近一年使用:0次
名校
解题方法
8 . 下列除杂试剂的选择和除杂操作均正确的是
| 选项 | 括号内为杂质 | 除杂试剂 | 除杂操作 |
| A | CO2(SO2) | Na2CO3 | 将气体通过足量的Na2CO3溶液 |
| B | Cl2(HCl) | 饱和食盐水 | 将气体通过足量的饱和食盐水 |
| C | FeCl3溶液 (FeCl2) | KMnO4溶液 | 加入适量KMnO4溶液 |
| D | NaHCO3溶液(Na2CO3) | 氯化钡溶液 | 加入适量氯化钡溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列实验方案中,不能测定出Na2CO3和 NaHCO3的混合物中Na2CO3质量分数的是
| A.取ag混合物充分加热,质量减少bg |
| B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| C.取ag混合物与足量稀硫酸充分反应,排饱和碳酸钠溶液收集到气体VL |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加bg |
您最近一年使用:0次
解题方法
10 . 下列各组物质之间可以按:物质A→物质B→物质C→物质D的关系不能直接转化的是
| A.Fe→Fe3O4→Fe(OH)3→Fe2(SO4)3 |
| B.Cl2→NaClO→HClO→HCl |
| C.Cu→CuCl2→Cu(OH)2→CuSO4 |
| D.Na→NaOH→NaCl→NaHCO3 |
您最近一年使用:0次



