2015-2016学年河北省景县中学高一下学期升级考试化学试卷
河北
高一
期末
2017-07-27
388次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、物质结构与性质、化学反应原理、有机化学基础、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
| A.燃料燃烧产物CO2是温室气体之一 |
| B.化石燃料完全燃烧不会造成大气污染 |
| C.以液化石油气代替燃油可减少大气污染 |
| D.燃料不完全燃烧排放的CO是大气污染物之一 |
A.8个中子的碳原子的符号: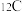 | B. 的电子式: 的电子式: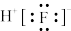 |
C. 的结构示意图: 的结构示意图: | D. 分子的空间填充模型: 分子的空间填充模型: |
| A.离子半径:S2->Na+ | B.热稳定性:HCl>HF |
| C.酸性:H3BO3>H2CO3 | D.碱性:Al(OH)3>Ca(OH)2 |
【知识点】 元素周期表 元素周期律
| A.为放热反应 | B.为吸热反应 |
| C.过程中热能转化为化学能 | D.反应物的总能量低于生成物的总能量 |
| A.①褪色,②不褪色 | B.①不褪色,②褪色 |
| C.①②均褪色 | D.①②均不褪色 |
【知识点】 乙烯与强氧化性物质的反应解读 苯的化学性质
 2P(g)达到平衡时,下列说法正确的是
2P(g)达到平衡时,下列说法正确的是| A.M、N全部变成了P |
| B.反应已经停止 |
| C.反应混合物中各组分的浓度不再改变 |
| D.反应混合物中c(M)∶c(N)∶c(P)一定等于2∶1∶2 |
| A.同主族元素从上到下,其氢化物的稳定性逐渐增强 |
| B.同周期元素(0族除外) 从左到右,原子半径逐渐减小 |
| C.将SO2通入Ca(ClO)2溶液可生成CaSO3沉淀 |
| D.Na、Al、Fe金属单质在一定条件下与水反应都生成H2和对应的碱 |
【知识点】 元素周期表 元素周期律
| A.Th元素的质量数是232 | B.Th元素的相对原子质量是231 |
| C.232Th转化成233U是化学变化 | D.230Th和232Th互称为同位素 |
【知识点】 元素周期表 元素周期律
A.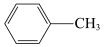 +Cl2 +Cl2 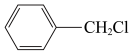 +HCl +HCl |
B.2CH3CH2OH+O2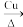 2CH3CHO+2H2O 2CH3CHO+2H2O |
C.ClCH2CH=CH2+NaOH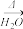 HOCH2CH=CH2+NaCl HOCH2CH=CH2+NaCl |
D.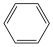 +HNO3 +HNO3 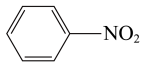 +H2O +H2O |
| A.研制水溶剂涂料替代有机溶剂涂料 |
| B.用可降解塑料生产包装盒或快餐盒 |
C.用反应:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O制备硫酸铜 CuSO4+SO2↑+2H2O制备硫酸铜 |
D. +CH2=CH2→ +CH2=CH2→ |
【知识点】 化学与环境保护
| A.用小苏打治疗胃酸过多:CO3﹣+2H+═CO2↑+H2O |
| B.钠与水反应:Na+2H2O═Na++2OH﹣+H2↑ |
| C.硫酸铜溶液中加入过量铁粉:Cu2++2Fe═2Fe3++Cu |
| D.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH﹣═2AlO2-+H2O |
【知识点】 离子反应的发生及书写
| A.在水中的溶解性:NaHCO3<Na2CO3 |
| B.相同条件下,与等浓度盐酸反应生成CO2的速率:NaHCO3<Na2CO3 |
| C.等质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出CO2更多 |
| D.等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应产生的CO2质量相同 |
【知识点】 碳酸钠与碳酸氢钠性质的比较解读
| A.氧化镁用作耐火材料 |
| B.Na2O常用于潜水艇或呼吸面具的供氧剂 |
| C.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| D.FeCl3溶液可用于刻制印刷铜电路板 |
【知识点】 仪器使用与实验安全
| A.稀盐酸 | B.FeCl3 | C.Fe(NO3)3 | D.BaCl2 |
【知识点】 化学实验基础
| A.铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3 |
| B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜 |
| C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中 |
| D.钠与氧气、水等反应时钠作还原剂,故金属单质参与反应可作还原剂 |
| A.1.0 mol/L | B.2.0 mol/L |
| C.3.0 mol/L | D.4.0 mol/L |
【知识点】 化学方程式计算中物质的量的运用解读 铁与铁离子反应解读
 2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法不正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O 下列说法不正确的是| A.CO2是氧化产物 |
| B.H2C2O4在反应中被氧化 |
| C.1mol KClO3参加反应,转移的电子为1mol |
| D.H2C2O4的氧化性强于ClO2的氧化性 |
【知识点】 氧化还原反应基本概念 氧化还原反应的规律解读
| A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B.在H2O2分解过程中,溶液的酸碱性不变 |
| C.在H2O2分解过程中,Fe2+和Fe3+的总量保持不变 |
| D.H2O2生产过程要严格避免混入Fe2+ |
【知识点】 氧化还原反应基本概念
| 实验 | 操作 | |
| A | 配制稀硫酸 | 先将浓硫酸加入烧杯中,后倒入蒸馏水 |
| B | 排水法收集KMnO4分解产生的O2 | 先熄灭酒精灯,后移出导管 |
| C | 浓盐酸与MnO2反应制备纯净Cl2 | 气体产物先通过浓硫酸,后通过饱和食盐水 |
| D | CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
| A.A | B.B | C.C | D.D |
| A.a与其他三种元素形成的二元化合物中其化合价均为+1 |
| B.b与其他三种元素均可形成至少两种二元化合物 |
| C.c的原子半径是这些元素中最大的 |
| D.d和a形成的化合物的水溶液呈弱酸性 |
| A.14 g乙烯和丙烯混合气体中的氢原子数为2NA |
| B.1 mol N2与4 mol H2反应生成的NH3分子数为2NA |
| C.1 mol Fe溶于过量硝酸,电子转移数为2NA |
| D.标准状况下,2.24 L CCl4含有的共价键数为0.4NA |
 N放出942 kJ热量,根据以上信息和数据,下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,下列说法正确的是
| A.N4属于一种新型的化合物 |
| B.N4与N2互称为同位素 |
| C.N4化学性质比N2稳定 |
| D.1 mol N4气体转变为N2将放出882 kJ热量 |
| A.在18 g 16O2中含有NA个氧原子 |
| B.16O与18O核外电子排布方式相同 |
| C.在标准状况下,1.12 L 16O2和1.12 L 18O2均含有0.1NA个氧原子 |
| D.18O2和16O2化学性质几乎相同 |
【知识点】 化学计量 元素周期表 元素周期律
①粒子半径:K+>Al3+>S2->Cl- ②酸性:H2SO4>H3PO4>H2CO3>HClO
③离子的还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤金属性:Be<Mg<Ca<K ⑥非金属性:O>N>P>Si
⑦氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
| A.②③⑤⑦ | B.②⑥⑦ | C.②④⑤⑥⑦ | D.②④⑥ |
【知识点】 元素周期表 元素周期律
①离子化合物一定含离子键,也可能含极性键或非极性键;
②共价化合物一定含共价键,也可能含离子键;
③含金属元素的化合物不一定是离子化合物;
④由非金属元素组成的化合物一定是共价化合物;
⑤由分子组成的物质中一定存在共价键;
⑥熔融状态能电离的化合物一定是离子化合物。
| A.①③⑤ | B.①③⑥ | C.②③④ | D.②④⑥ |
【知识点】 化学键与物质类别关系的判断解读
| A.煤的干馏产物主要是各类有机物 |
| B.石油的裂解、分馏和煤的干馏都属于化学变化 |
| C.煤焦油经过分馏可得到苯、甲苯等,说明煤中含有苯和甲苯 |
| D.石油的裂化,说明长链烃在高温条件下可以分解为短链烃 |
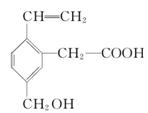
| A.能使酸性KMnO4溶液褪色 |
| B.能发生酯化反应 |
| C.能跟NaOH溶液反应 |
| D.能发生水解反应 |
【知识点】 羧酸化学性质 多官能团有机物的结构与性质解读
| A.只用水就可以鉴别四氯化碳、苯和乙醇 |
| B.C2H4、C3H6、C6H6分子中,所有原子处于同一平面上 |
| C.光照条件下,氯气与乙烷发生化学反应,生成的产物有6种 |
D.有机物 与氯气发生取代反应,生成的一氯代物有5种 与氯气发生取代反应,生成的一氯代物有5种 |
【知识点】 烃
二、填空题 添加题型下试题

(1)元素A在周期表中的位置
(2)写出钙与M原子个数比为1:2化合物的电子式
(3)M2-、D+、G2-离子半径大小顺序是

(4)某同学设计实验证明A、B、F的非金属性强弱关系。
① 溶液a和b分别为
② 溶液c中的离子方程式为
(5)将0.5 mol D2M2投入100 mL 3 mol/L ECl3溶液中,转移电子的物质的量为
【知识点】 元素周期表 元素周期律
 bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:
bM(g)的放热反应,M、N物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中
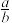 =
=(2)t2时两线交叉点
(3)此反应达到平衡时,反应物的转化率为
(4)下列描述能说明上述反应达到平衡状态的是
①反应中M与N物质的量之比为2∶5 ②混合气体的总物质的量不随时间的变化而变化③M的转化率达到最大 ④如容器为绝热容器,体系内温度不再变化
II.锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiCIO4。溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

回答下列问题:
(1)外电路的电流方向是由
(2)电池正极反应式为
(3)是否可用水代替电池中的混合有机溶剂?
【知识点】 化学平衡
三、解答题 添加题型下试题
 2CH3CH2OH+2CO2↑)
2CH3CH2OH+2CO2↑)已知:实验室制乙烯原理为CH3CH2OH
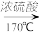 CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
CH2=CH2↑+H2O,产生的气体能使Br2的四氯化碳溶液褪色,甲、乙同学用下列实验验证。(气密性已检验,部分夹持装置略)。
实验操作和现象:

(1)溶液“渐渐变黑”,说明浓硫酸具有
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是
②乙根据现象认为实验中产生的SO2和
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色。
乙:用下列装置按一定顺序与A连接:(尾气处理装置略)

现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色。
请回答下列问题
A.甲设计实验中A、B间洗气瓶中盛放的试剂是
B.能说明确实是SO2使E中溶液褪色的实验是
C.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是
【知识点】 离子反应的发生及书写
四、填空题 添加题型下试题

(1)仪器B的名称是
①Ⅲ中的试剂为
③V的作用为
(3)乙组同学进行同样实验,但装置连接顺序为I-Ⅲ一Ⅳ- II-V-Ⅵ,此时II中现象为
(4)化合物A中含单质M的元素的质量分数为28%,则A的化学式为
【知识点】 元素周期表 元素周期律
试卷分析
试卷题型(共 34题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 大气污染 大气污染来源及危害 化石能源 | |
| 2 | 0.85 | 原子结构示意图、离子结构示意图 有机物的结构式、结构简式、比例模型、球棍模型、最简式 共价型分子结构式、电子式 原子中相关数值及其之间的相互关系 | |
| 3 | 0.64 | 元素周期表 元素周期律 | |
| 4 | 0.85 | 能量的相互转化 吸热反应和放热反应 | |
| 5 | 0.85 | 乙烯与强氧化性物质的反应 苯的化学性质 | |
| 6 | 0.85 | 可逆反应及反应限度 化学平衡状态本质及特征 化学平衡状态的判断方法 | |
| 7 | 0.94 | 元素周期表 元素周期律 | |
| 8 | 0.85 | 元素周期表 元素周期律 | |
| 9 | 0.85 | 有机反应类型 取代反应 | |
| 10 | 0.85 | 化学与环境保护 | |
| 11 | 0.94 | 离子反应的发生及书写 | |
| 12 | 0.65 | 碳酸钠与碳酸氢钠性质的比较 | |
| 13 | 0.85 | 仪器使用与实验安全 | |
| 14 | 0.64 | 化学实验基础 | |
| 15 | 0.65 | 钠 铝 铁 | |
| 16 | 0.64 | 烃 有机物的结构特点 | |
| 17 | 0.85 | 化学方程式计算中物质的量的运用 铁与铁离子反应 | |
| 18 | 0.65 | 氧化还原反应基本概念 氧化还原反应的规律 | |
| 19 | 0.64 | 氧化还原反应基本概念 | |
| 20 | 0.65 | 氯气的实验室制法 化学实验基础操作 萃取和分液 实验方案设计的基本要求 | |
| 21 | 0.65 | 元素周期律、元素周期表的推断 元素周期律的应用 根据原子结构进行元素种类推断 结合物质计算的元素周期律、元素周期表相关推断 | |
| 22 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 23 | 0.65 | 化学反应中能量变化的原因 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 24 | 0.64 | 化学计量 元素周期表 元素周期律 | |
| 25 | 0.64 | 元素周期表 元素周期律 | |
| 26 | 0.85 | 化学键与物质类别关系的判断 | |
| 27 | 0.85 | 化石能源 石油裂化、裂解 煤的干馏 | |
| 28 | 0.65 | 羧酸化学性质 多官能团有机物的结构与性质 | |
| 29 | 0.64 | 烃 | |
| 30 | 0.64 | 烃 烃的衍生物 | |
| 二、填空题 | |||
| 31 | 0.85 | 元素周期表 元素周期律 | |
| 32 | 0.94 | 化学平衡 | |
| 34 | 0.94 | 元素周期表 元素周期律 | |
| 三、解答题 | |||
| 33 | 0.64 | 离子反应的发生及书写 | 实验探究题 |

 的一氯代物可能的结构有(不考虑立体异构)
的一氯代物可能的结构有(不考虑立体异构) 

