甘肃省武威市第十八中学2021届高三上学期第一次月考化学试题
甘肃
高三
阶段练习
2020-11-02
362次
整体难度:
适中
考查范围:
认识化学科学、化学实验基础、常见无机物及其应用、化学反应原理、有机化学基础、物质结构与性质
一、单选题 添加题型下试题
| A.2gH2含有1mol氢分子 |
| B.2mol氧气的摩尔质量为64g·mol-1 |
| C.1mol任何物质都含有6.02×1023个分子 |
| D.质量相等的CO和CO2,物质的量之比为2∶3 |
| A.容量瓶是配制一定物质的量浓度溶液的专用仪器 |
| B.容量瓶可以用来加热 |
| C.能用容量瓶长期贮存配制好的溶液 |
| D.可以用500mL容量瓶配制250mL溶液 |
|
|
|
|
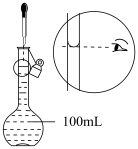
| A.接近称量质量时,轻振手腕,加够药品 | B.溶解时,用量筒控制所加蒸馏水的量 | C.移液时,玻璃棒插在刻度线以上,防止液体洒出 | D.液面接近刻度线1~2cm时,用胶头滴管滴加蒸馏水至刻度线 |
| A.A | B.B | C.C | D. D |
【知识点】 一定物质的量浓度的溶液的配制
| A.NaHSO4溶液与Ba(OH)2溶液混合 | B.NH4Cl溶液与Ca(OH) 2溶液混合 |
| C.HNO3溶液与KOH溶液混合 | D.Na2HPO4溶液与NaOH溶液混合 |
【知识点】 离子反应的发生及书写
A.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| B.硫酸溶液与氢氧化钡溶液混合:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| C.Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
| D.FeCl3溶液与Cu反应:Fe3++Cu═Fe2++Cu2+ |
【知识点】 离子方程式的正误判断解读
A.K+、Na+、NO 、MnO 、MnO | B.Mg2+、Na+、Cl-、SO |
| C.K+、Na+、Br-、Cu2+ | D.Na+、Ba2+、OH-、SO |
【知识点】 限定条件下的离子共存解读
| A.SiO2的摩尔质量为60 |
| B.标准状况下,15 g SiO2的体积为5.6 L |
| C.SiO2中Si与O的质量比为7∶8 |
| D.相同质量的SiO2和CO2中含有的氧原子数相同 |
| A.4N | B.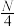 |
| C.2N | D.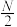 |
【知识点】 阿伏加德罗常数的求算解读
| A.溶液中含有的阴、阳离子总数为0.6mol |
| B.在0.5 L该溶液中,Ba2+的浓度为0.1 mol/L |
| C.在500 mL该溶液中,含有0.2molNO3﹣ |
| D.取1L该溶液稀释到10L时,NO3﹣的浓度为0.02 mol/L |
二、 添加题型下试题
A.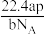 | B.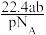 |
C.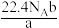 | D.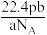 |
三、单选题 添加题型下试题
| A.200 mL2 mol/LMgCl2溶液 | B.1000 mL2.5 mol/LNaCl溶液 |
| C.250 mL1 mol/LAlCl3溶液 | D.300 mL5 mol/LKClO3溶液 |
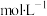 和300mL 0.25
和300mL 0.25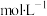 的硫酸注入500mL的容量瓶中,加水稀释至刻度线,则该混合物中
的硫酸注入500mL的容量瓶中,加水稀释至刻度线,则该混合物中 的物质的量浓度为
的物质的量浓度为A.0.21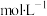 | B.0.26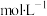 | C.0.42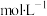 | D.0.56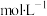 |
【知识点】 物质的量浓度计算-溶液混合的有关计算解读

| A.右边与左边分子数之比为4:1 |
| B.右侧CO的质量为5.6g |
| C.右侧气体密度是相同条件下氢气密度的14倍 |
| D.若改变右边CO的充入量而使隔板处于容器正中间保持温度不变,则应充入0.2 mol CO |
【知识点】 阿伏加德罗定律及其推论解读
| A.1:1 | B.1:4 | C.2:1 | D.2:3 |
【知识点】 气体摩尔体积 物质的量有关计算 根据n=m/M进行相关计算解读
| A.14 g乙烯和丙烯混合气体中的氢原子数为2NA |
| B.1 mol N2与4 mol H2反应生成的NH3分子数为2NA |
| C.1 mol Fe溶于过量硝酸,电子转移数为2NA |
| D.标准状况下,2.24 L CCl4含有的共价键数为0.4NA |

| A.a的溶解度大于b的溶解度 |
| B.在t℃时,a、b的饱和溶液中溶质的物质的量浓度相同 |
| C.当a中含有少量b时,可以用冷却结晶法提纯a |
| D.在t℃时,将a、b的饱和溶液升温后,溶质的质量分数:a﹥b |
【知识点】 溶液 溶解度、饱和溶液的概念解读 物质的量浓度概念、含义解读
四、计算题 添加题型下试题
(1)所得盐酸的质量分数和物质的量浓度分别是
(2)取这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是
(3)在40.0 mL 0.065 mol·L-1Na2CO3溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过
(4)将不纯的NaOH样品1g(样品含少量Na2CO3和水),放入50mL2mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到
五、填空题 添加题型下试题
| 实验步骤 | 实验现象 |
| ①用玻璃棒蘸取少量该溶液,点在pH试纸中部 | 试纸变为红色 |
| ②取少量该溶液放入洁净的试管中,加入Cu片和浓硫酸,加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| ③取少量该溶液放入洁净的试管中,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中反应后的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断:
(1)溶液中一定存在的离子是
(2)写出实验步骤②中所发生反应的离子方程式:
(3)为了进一步确定其他离子,应该补充的实验及对应欲检验离子的名称
六、解答题 添加题型下试题
Ⅰ.配制酸性KMnO4标准溶液:如图是配制50mL酸性KMnO4标准溶液的过程示意图。


(1)下列关于容量瓶的叙述正确的是
①主要用于配制准确物质的量浓度的溶液
②不宜长时间贮存溶液
③能用来加热
④使用前要检查是否漏水
(2)请你观察图示并判断其中不正确的操作有
(3)其中确定50mL溶液体积的容器是
(4)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将
Ⅱ.测定血液样品中Ca2+的浓度:取血液样品20.00mL,经过上述处理后得到草酸,再用0.020mol·L-1酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL酸性KMnO4溶液。
(4)已知草酸与酸性KMnO4溶液反应的离子方程式为5H2C2O4+2MnO
 +6H+=2Mnx++10CO2↑+8H2O,则式中的x=
+6H+=2Mnx++10CO2↑+8H2O,则式中的x=(5)滴定时,根据现象
(6)经过计算,血液样品中Ca2+的浓度为
七、填空题 添加题型下试题
 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)指出反应的类型:A→C:
(2)在A~E五种物质中,互为同分异构体的是
(3)A中所含有的官能团名称为
A→B:
A→D:
(4)C能形成高聚物,该高聚物的结构简式为
(5)写出D与NaOH溶液共热反应的化学方程式为
八、解答题 添加题型下试题
 ;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。
;Y是元素周期表中电负性最大的元素;Y、Z位于同一主族;Q基态原子核外的M能层中有两个未成对电子和三个空轨道;R位于第四周期ⅥB族。请回答下列问题:
 元素基态原子的电子排布式为
元素基态原子的电子排布式为 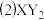 分子的立体构型是
分子的立体构型是 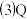 与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为
与氮元素形成的一种化合物晶胞如图所示,该化合物的化学式为 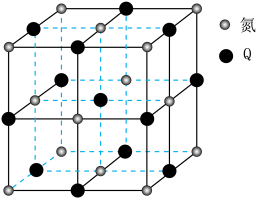
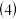 化合物
化合物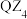 熔点为
熔点为 ,沸点为
,沸点为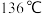 ,熔融态不导电,可知
,熔融态不导电,可知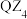 的晶体类型是
的晶体类型是 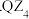 与热水反应的化学方程式为
与热水反应的化学方程式为 【知识点】 物质结构与性质综合考查解读 电子排布式解读 杂化轨道理论
试卷分析
试卷题型(共 21题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 物质的量的含义 摩尔质量的概念 | |
| 2 | 0.94 | 仪器使用与实验安全 配制一定物质的量浓度的溶液实验的仪器 | |
| 3 | 0.85 | 一定物质的量浓度的溶液的配制 | |
| 4 | 0.65 | 离子反应的发生及书写 | |
| 5 | 0.65 | 离子方程式的正误判断 | |
| 6 | 0.85 | 限定条件下的离子共存 | |
| 7 | 0.85 | 摩尔质量 物质的量有关计算 | |
| 8 | 0.85 | 阿伏加德罗常数的求算 | |
| 9 | 0.94 | 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 11 | 0.65 | 物质的量浓度的计算 物质的量浓度计算-与溶质成分有关的计算 | |
| 12 | 0.65 | 物质的量浓度计算-溶液混合的有关计算 | |
| 13 | 0.4 | 阿伏加德罗定律及其推论 | |
| 14 | 0.65 | 气体摩尔体积 物质的量有关计算 根据n=m/M进行相关计算 | |
| 15 | 0.65 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合氧化还原反应知识与NA相关推算 结合物质结构基础知识与NA相关推算 | |
| 16 | 0.65 | 溶液 溶解度、饱和溶液的概念 物质的量浓度概念、含义 | |
| 二、 | |||
| 10 | 0.65 | 气体摩尔体积 根据n=N/NA的相关计算 气体物质与NA相关的推算 根据n=m/M的相关计算 | |
| 三、计算题 | |||
| 17 | 0.65 | 物质的量浓度 化学方程式计算中物质的量的运用 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 四、填空题 | |||
| 18 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 硝酸的强氧化性 铝三角转化 离子的检验 | |
| 20 | 0.65 | 有机官能团的性质及结构 酯化反应 烯烃的加聚反应 醇类的化学性质 | |
| 五、解答题 | |||
| 19 | 0.65 | 氧化还原反应方程式的配平 酸碱中和滴定原理的应用 一定物质的量浓度的溶液的配制 | 实验探究题 |
| 21 | 0.65 | 物质结构与性质综合考查 电子排布式 杂化轨道理论 | 无机推断题 |