湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题
湖南
高三
阶段练习
2020-10-20
748次
整体难度:
容易
考查范围:
常见无机物及其应用、化学实验基础、有机化学基础、认识化学科学、化学反应原理、化学与STSE
一、单选题 添加题型下试题
| A.用冷水贮存白磷 | B.用浓硫酸干燥二氧化硫 |
| C.用酒精灯直接加热蒸发皿 | D.用二氧化碳灭火器扑灭金属钾的燃烧 |
| A.谷物发酵酿造食醋 | B.小苏打用作食品膨松剂 |
| C.含氯消毒剂用于环境消毒 | D.大气中NO2参与酸雨形成 |
| A.33.3% | B.40% | C.36% | D.54.5% |
| 加入溶液 | ①适量铋酸钠溶液 | ②过量的双氧水 | ③适量KI淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A.I2,H2O2,KMnO4,NaBiO3 |
| B.H2O2,I2,NaBiO3,KMnO4 |
| C.NaBiO3,KMnO4,H2O2,I2 |
| D.KMnO4,NaBiO3,I2,H2O2 |
【知识点】 氧化性、还原性强弱的比较解读 氧化还原反应的规律解读
| A.常温常压下,124gP4中所含P—P键数目为4NA |
| B.100mL1mol·L−1FeCl3溶液中所含Fe3+的数目为0.1NA |
| C.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA |
| D.密闭容器中,2molSO2和1molO2催化反应后分子总数为2NA |
| A.称量物错放在托盘天平右盘 | B.定容时观察液面俯视 |
| C.有少量NaOH溶液残留在烧杯中 | D.容量瓶中原来有少量蒸馏水 |
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
①澄清石灰水②H2S溶液③KMnO4酸性溶液④氯水⑤品红溶液
| A.①②③ | B.②③④ | C.除①以外 | D.全部 |
【知识点】 二氧化硫与二氧化碳的性质区别解读
 、SO
、SO 、Al3+、I-、Mg2+、Na+七种离子中的某几种。现取该溶液进行实验,得到如下现象:
、Al3+、I-、Mg2+、Na+七种离子中的某几种。现取该溶液进行实验,得到如下现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
已知:5Cl2+I2+6H2O=10HCl+2HIO3
据此可以判断,该溶液中肯定不存在的离子组是( )
A.Al3+、Mg2+、SO |
B.Mg2+、CO 、I- 、I- |
C.Al3+、SO 、I- 、I- |
D.Al3+、Br-、SO |
| A.Na2SO4是钠盐、硫酸盐、正盐 |
| B.HNO3是一元酸、强酸、挥发性酸 |
| C.Mg(OH)2是二元碱、难溶性碱、中强碱 |
| D.Al2O3是两性氧化物、金属氧化物、最高价氧化物 |

A.a反应: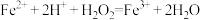 |
B.b反应: |
C.c反应: |
D.d反应: |
【知识点】 离子方程式的正误判断解读
| 化学性质 | 实际应用 | |
| A. | Al2(SO4)3和小苏打反应 | 泡沫灭火器灭火 |
| B. | 铁比铜金属性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| C. | 次氯酸盐具有氧化性 | 漂白粉漂白织物 |
| D. | HF与SiO2反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| A.A | B.B | C.C | D.D |
A.用醋酸除去水垢:2H++CaCO3 Ca2++CO2↑+H2O Ca2++CO2↑+H2O |
B.硫化亚铁与浓硫酸混合加热:2H++FeS H2S↑+ Fe2+ H2S↑+ Fe2+ |
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3  Al2(CO3)3↓ Al2(CO3)3↓ |
D.用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-  +NO2-+ H2O +NO2-+ H2O |
【知识点】 离子反应的发生及书写
| A.钠与水反应:Na +2H2O=Na++2OH–+H2↑ |
B.电解饱和食盐水获取烧碱和氯气:2Cl–+2H2O H2↑+Cl2↑+2OH– H2↑+Cl2↑+2OH– |
| C.向氢氧化钡溶液中加入稀硫酸:Ba2++OH–+H++SO42-=BaSO4↓+H2O |
| D.向碳酸氢铵溶液中加入足量石灰水:Ca2++HCO3-+OH–=CaCO3↓+H2O |
【知识点】 离子反应的发生及书写
A.无色溶液中:Na+、 、Cu2+、 、Cu2+、 |
B.0.1 mol·L-1的NH4HCO3溶液中:K+、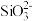 、 、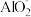 、Cl- 、Cl- |
C.25 ℃时,Kw/c(H+)=1×10-12mol·L-1的溶液中:K+、 、S2-、ClO- 、S2-、ClO- |
D.使甲基橙呈红色的溶液: 、Ba2+、Al3+、Cl- 、Ba2+、Al3+、Cl- |
【知识点】 物质共存解读 限定条件下的离子共存解读
二、多选题 添加题型下试题

| A.对比①和②可以说明还原性:Br->Cl- |
| B.①和③相比可说明氧化性:Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明酸性:H2SO4>HCl |
| D.③中的反应是非氧化还原反应 |
三、单选题 添加题型下试题
| A.向溶液中滴入KSCN溶液呈红色,说明不含Fe2+ |
| B.向溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+ |
| C.向溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+ |
| D.向溶液中加入NaOH溶液得白色沉淀,逐渐变为红褐色,说明溶液中不含有Mg2+ |
【知识点】 铁盐与亚铁盐鉴别试剂的选择解读 常见阳离子的检验解读
四、多选题 添加题型下试题
| A.氧气转化为臭氧是化学变化 | B.臭氧(O3)的摩尔质量为48g |
| C.氮氧化合物会导致臭氧层空洞 | D.臭氧对人的身体健康不利,应该拒绝使用臭氧 |
五、单选题 添加题型下试题
A.0.1 mol·L-1 NaOH溶液: Na+、K+、 、 、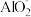 |
B.0.1 mol·L-1 FeCl2溶液: K+、Mg2+、 、 、 |
| C.0.1 mol·L-1 KHCO3溶液:Na+、Ba2+、Cl-、OH- |
D.0.1 mol·L-1 氯水中: K+、 、 、 、 、 |
【知识点】 物质共存解读 限定条件下的离子共存解读
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化硫的化学性质 物质性质实验方案的设计解读
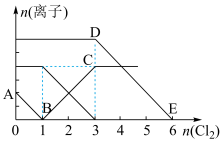
| A.线段BC代表Fe3+的物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)=6 mol/L |
| C.当通入 2mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
【知识点】 氧化还原反应有关计算 氧化还原反应的规律解读
六、多选题 添加题型下试题
| A.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能 |
B.因为CaCO3+SiO2 CaSiO3+CO2↑,所以硅酸的酸性比碳酸强 CaSiO3+CO2↑,所以硅酸的酸性比碳酸强 |
| C.CO2和SiO2都能与碳反应,且都作氧化剂 |
| D.SiO2既能和NaOH反应,又能和氢氟酸反应,但SiO2不属于两性氧化物 |
七、单选题 添加题型下试题
| A.NaClO溶液的消毒原理是使蛋白质变性 |
| B.1molCl2与足量NaOH溶液反应转移2mol电子 |
| C.NaClO溶液的漂白原理与Na2O2、SO2相同 |
| D.“84”消毒液与“洁厕灵”(盐酸)共同使用,可达到既清洁又消毒的双重效果 |
八、计算题 添加题型下试题
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比4∶5,其中Fe2+与Fe3+物质的量之比为
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水)
(4)为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量为
九、解答题 添加题型下试题
| 阳离子 | K+、Ba2+、Ag+、Mg2+、 |
| 阴离子 | Cl-、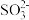 、 、 、 、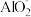 、 、 |
(1)取该固体混合物,加水后固体完全溶解得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12。则混合物组成中肯定不存在的离子是
(2)向(1)所得溶液中滴加盐酸,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。则肯定存在的离子是
(3)取以上实验的上层澄清液,滴加AgNO3溶液,有白色沉淀生成。你认为还有哪些离子尚待检验:
十、计算题 添加题型下试题

(1)在A情况下,溶质是(填化学式)
(2)在B情况下,溶质是(填化学式)
(3)原氢氧化钠溶液的物质的量浓度
(1)所得盐酸的质量分数和物质的量浓度分别是
(2)取这种盐酸100 mL,稀释至1.18L,所得稀盐酸的物质的量浓度是
(3)在40.0 mL 0.065 mol·L-1Na2CO3溶液中,逐滴加入上述稀释后的稀盐酸,边加边振荡。若使反应不产生CO2气体,加入稀盐酸的体积最多不超过
(4)将不纯的NaOH样品1g(样品含少量Na2CO3和水),放入50mL2mol·L-1的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1mol·L-1的NaOH溶液。蒸发中和后的溶液,最终得到
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 浓硫酸的吸水性 碱金属发生火灾的处理方法 仪器使用与实验安全 常用仪器及使用 | |
| 2 | 0.94 | 二氧化氮与水反应 硫的氧化物对人体、环境的危害 酸雨 碳酸氢钠的不稳定性 乙醇与强氧化剂的反应 | |
| 3 | 0.4 | 过氧化钠与水的反应 过氧化钠和二氧化碳反应 过氧化钠的相关计算 | |
| 4 | 0.65 | 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 5 | 0.65 | 阿伏加德罗常数的应用 可逆反应及反应限度 盐类水解规律 甲烷的组成与结构 | |
| 6 | 0.85 | 配制一定物质的量浓度的溶液实验的误差分析 | |
| 7 | 0.94 | 二氧化硫与二氧化碳的性质区别 | |
| 8 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 盐类双水解反应 常见阳离子的检验 常见阴离子的检验 | |
| 9 | 0.85 | 分类方法的应用 酸、碱、盐、氧化物的概念及其相互联系 | |
| 10 | 0.85 | 离子方程式的正误判断 | |
| 11 | 0.65 | 漂白粉和漂粉精的用途 二氧化硅的化学性质 印刷电路板 盐类水解在生活、生产中的应用 | |
| 12 | 0.65 | 离子反应的发生及书写 | |
| 13 | 0.65 | 离子反应的发生及书写 | |
| 14 | 0.85 | 物质共存 限定条件下的离子共存 | |
| 16 | 0.85 | 铁盐与亚铁盐鉴别试剂的选择 常见阳离子的检验 | |
| 18 | 0.85 | 物质共存 限定条件下的离子共存 | |
| 19 | 0.65 | 二氧化硫的化学性质 物质性质实验方案的设计 | |
| 20 | 0.65 | 氧化还原反应有关计算 氧化还原反应的规律 | |
| 22 | 0.65 | 次氯酸及其性质 漂白粉和漂粉精 氯气与碱溶液反应 电子转移计算 | |
| 二、多选题 | |||
| 15 | 0.85 | 二氧化硫的制备 化学实验探究 物质性质的探究 物质性质实验方案的设计 | |
| 17 | 0.85 | 物理变化与化学变化 摩尔质量与相对原子质量区别与联系 大气污染来源及危害 | |
| 21 | 0.85 | 硅单质 二氧化硅 硅的化学性质 二氧化硅与二氧化碳结构与性质的比较 | |
| 三、计算题 | |||
| 23 | 0.65 | 铁的氧化物 物质含量的测定 | |
| 25 | 0.65 | 氢氧化钠、碳酸钠混合溶液与盐酸反应相关考查 碳酸钠、碳酸氢钠混合物的有关求算 | |
| 26 | 0.65 | 物质的量浓度 化学方程式计算中物质的量的运用 依据物质的量浓度公式的基础计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 四、解答题 | |||
| 24 | 0.65 | 离子反应的实际应用 离子反应在化合物组成的分析、鉴定的应用 | 无机推断题 |



