河北省安平中学2016-2017学年高二下学期期末考试化学试题
河北
高二
期末
2017-07-10
353次
整体难度:
适中
考查范围:
有机化学基础、认识化学科学、化学与STSE、物质结构与性质、化学反应原理、化学实验基础、常见无机物及其应用
一、单选题 添加题型下试题
①研究有机化合物组成、结构、性质和应用
②根据需要对有机化合物分子进行设计和合成
③从天然的动植物中提取、分离出一些纯净物。
这是有机化学发展的必经之路。下列按先后顺序排列的是
| A.①②③ | B.③②① | C.③①② | D.②①③ |
| A.用石灰、碳酸钠等碱性物质处理废水中的酸 |
| B.用氯气处理水中的Cu2+、Hg+等重金属离子 |
| C.用可溶性的铝盐和铁盐处理水中的悬浮物 |
D.用烧碱处理含高浓度 的废水并回收利用氨 的废水并回收利用氨 |
【知识点】 离子反应在生活、生产中的应用解读
| A.PM2.5是指粒径不大于2.5 μm的可吸入悬浮颗粒物 |
| B.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 |
| C.绿色化学要求从源头上消除或减少生产活动对环境的污染 |
| D.天然气和液化石油气是我国目前推广使用的清洁燃料 |
| A.水可以用来分离溴苯和苯的混合物 | B.淀粉和纤维素互为同分异构体 |
| C.环己烷与苯可用酸性KMnO4溶液鉴别 | D.植物油氢化过程中发生了加成反应 |
【知识点】 油脂的基本组成与结构解读
A.凡是分子组成相差一个或 个 个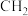 原子团的物质,彼此一定是同系物 原子团的物质,彼此一定是同系物 |
| B.两种有机物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体 |
| C.相对分子质量相同的几种化合物,互称为同分异构体 |
| D.组成元素的质量分数相同,且相对分子质量也相同的不同有机物,一定互为同分异构体 |
【知识点】 同系物的概念解读 同分异构现象、同分异构体的概念解读
| A.X的简单氢化物的热稳定性比W的强 |
| B.Y与X的简单离子具有相同的电子层结构 |
| C.Y与Z形成的化合物的水溶液可使蓝色石蕊试纸变红 |
| D.Z与X属于同一主族,与Y属于同一周期 |
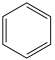 (b)、
(b)、 (c)、
(c)、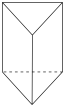 (d)的分子式均为C6H6,下列说法正确的是
(d)的分子式均为C6H6,下列说法正确的是| A.b的同分异构体只有c和d两种 |
| B.b、c、d的二氯代物均只有三种 |
| C.b、c、d均可与酸性高锰酸钾溶液反应 |
| D.b、c、d中只有b的所有原子处于同一平面 |
 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A.0.1 mol 的 中,含有 中,含有 个中子 个中子 |
B.pH=1的H3PO4溶液中,含有 个 个 |
C.2.24L(标准状况)苯在O2中完全燃烧,得到 个CO2分子 个CO2分子 |
D.密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加 个P-Cl键 个P-Cl键 |
| 选项 | 物质 | 使用的试剂 | 主要操作 |
| A | 乙醇(水) | 氧化钙 | 蒸馏 |
| B | 乙酸乙酯(乙酸) | 饱和氢氧化钠溶液 | 分液. |
| C | 苯(苯酚) | 浓溴水 | 过滤 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
【知识点】 物质分离、提纯的常见化学方法解读

下列有关说法正确的是
| A.该高分子由 4 种单体(聚合成高分子的简单小分子)缩聚而成 |
| B.构成该分子的几种羧酸单体互为同系物 |
| C.上述单体中的乙二醇,可被O2催化氧化生成单体之一的草酸 |
| D.该高分子有固定熔、沸点,1mol上述链节完全水解需要氢氧化钠物质的量为5mol |
 ,下列有关叙述正确的是
,下列有关叙述正确的是① 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
②X在一定条件下能与FeCl3溶液发生显色反应
③X在一定条件下能发生消去反应和酯化反应
④X的化学式为C10H8O6
| A.①② | B.①③ | C.②④ | D.③④ |
【知识点】 有机物的结构特点
| 目的 | 操作 | |
| A | 取20.00mL盐酸 | 在50mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| B | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C | 测定醋酸钠溶液的pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D | 配制浓度为0.010mol·L-1的KMnO4溶液 | 称取KMnO4固体0.15g放入100mL容量瓶中,加水溶解并稀释至刻度 |
| A.A | B.B | C.C | D.D |
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化硫的化学性质 物质性质实验方案的设计解读

| A.汉黄芩素的分子式为C16H13O5 |
| B.1 mol该物质与溴水反应,最多消耗1 mol Br2 |
| C.该物质遇FeCl3溶液显色 |
| D.与足量H2发生加成反应后,该分子中官能团的种类减少1种 |
【知识点】 多官能团有机物的结构与性质解读
| A.4种 | B.3种 | C.2种 | D.1种 |
【知识点】 根据要求书写同分异构体解读 羧酸酯化反应解读
| A.3种 | B.4种 | C.5种 | D.6种 |
【知识点】 同分异构体的数目的确定解读
| A.硅太阳能电池工作时,光能转化成电能 |
| B.锂离子电池放电时,化学能转化成电能 |
| C.电解质溶液导电时,电能转化成化学能 |
| D.葡萄糖为人类生命活动提供能量时,化学能转化成热能 |
【知识点】 氧化还原反应的应用
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
| B | C4H8Cl2的同分异构体数目(不考虑立体异构) | 共有10种 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | 由乙酸和乙醇制乙酸乙酯,油脂水解 | 均属于取代反应 |
| A.A | B.B | C.C | D.D |
【知识点】 有机反应类型 同分异构体的数目的确定解读
 Ni(CO)4(g)。230 ℃时,该反应的平衡常数K=2×10-5。已知:Ni(CO)4的沸点为 42.2 ℃,固体杂质不参与反应。
Ni(CO)4(g)。230 ℃时,该反应的平衡常数K=2×10-5。已知:Ni(CO)4的沸点为 42.2 ℃,固体杂质不参与反应。第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230 ℃制得高纯镍。下列判断正确的是
| A.增加 c(CO),平衡向正向移动,反应的平衡常数增大 |
| B.该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO) |
| C.第一阶段,在 30 ℃和 50 ℃两者之间选择反应温度,选50 ℃ |
| D.第二阶段,Ni(CO)4分解率较低 |
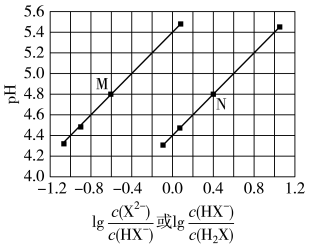
| A.Ka2(H2X)的数量级为10–6 |
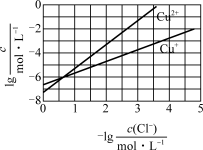
B.曲线N表示pH与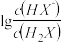 的变化关系 的变化关系 |
| C.NaHX溶液中c(H+)>c(OH-) |
| D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+) |
【知识点】 弱电解质的电离平衡 弱电解质电离平衡的影响因素 盐类水解的应用
| A.电池工作时,正极可发生反应:2Li2S6+2Li++2e−=3Li2S4 |
| B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g |
| C.石墨烯的作用主要是提高电极a的导电性 |
| D.电池充电时间越长,电池中Li2S2的量越多 |
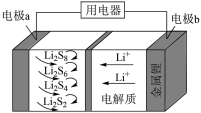
| A.Ksp(CuCl)的数量级为10-7 |
| B.除Cl-反应为Cu+Cu2++2Cl-=2CuCl |
| C.加入Cu越多,Cu+浓度越高,除Cl-效果越好 |
| D.2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 |
【知识点】 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积
二、填空题 添加题型下试题

(1)从左到右依次填写每步所属的反应类型:(a.取代反应,b.加成反应,c.消去反应,只填字母)
(2)A→B反应所需的试剂和条件是
(3)写出的
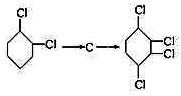 化学反应方程式:
化学反应方程式:三、解答题 添加题型下试题
(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化:

②A中只有一种一氯取代物B。写出由A转化为B的化学方程式
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种,F的结构简式是
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁发生显色反应。“HQ”还能发生的反应是(选填序号)
①加成反应 ②氧化反应 ③加聚反应 ④水解反应
“HQ”的一硝基取代物只有一种,“HQ”的结构简式是
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”,“TBHQ”与NaOH溶液作用得到化学式为C10H12O2Na2的化合物。“TBHQ”的结构简式是
 )的流程:
)的流程: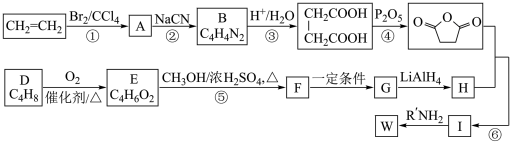
已知:I.
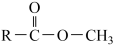
 R-CH2OH
R-CH2OH II.
 +R2-OH
+R2-OH
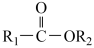 +
+ (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)(1)②是取代反应,其化学方程式是
(2)D的核磁共振氢谱中有两组峰且面积之比是1:3,不存在顺反异构。D的结构简式是
(3)⑤的化学方程式是
(4)G的结构简式是
(5)⑥的化学方程式是
【知识点】 根据要求书写同分异构体解读 羧酸酯化反应解读 有机物的推断
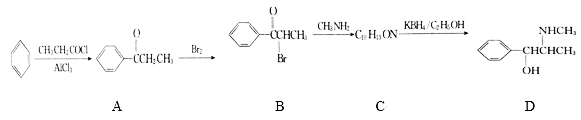
回答下列问题:
(1)伪麻黄碱(D)的分子式为
(2)写出B→C的化学方程式:
(3)B的消去产物可以用于合成高分子化合物E,请写出E的结构简式:
(4)满足下列要求的A的同分异构体有
①能发生银镜反应 ②苯环上的一氯代物有两种结构
其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的是(写出所有有机物的结构简式):
(5)已知:RCOOH
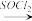 RCOCl。参照上述合成路线,设计一条以苯和乙酸为原料制备
RCOCl。参照上述合成路线,设计一条以苯和乙酸为原料制备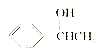 的合成路线。
的合成路线。试卷分析
试卷题型(共 29题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 有机化学发展及应用 | |
| 2 | 0.65 | 化学物质的分类方法 高分子材料 | |
| 3 | 0.65 | 离子反应在生活、生产中的应用 | |
| 4 | 0.65 | 大气污染来源及危害 | |
| 5 | 0.4 | 油脂的基本组成与结构 | |
| 6 | 0.65 | 合理安排饮食 | |
| 7 | 0.85 | 同系物的概念 同分异构现象、同分异构体的概念 | |
| 8 | 0.65 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 9 | 0.85 | 同分异构体的数目的确定 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 | |
| 10 | 0.4 | 物质的量有关计算 物质结构基础与NA相关推算 可逆反应及反应限度 弱电解质的电离平衡 | |
| 11 | 0.65 | 烷烃系统命名法 炔烃系统命名法 醇的系统命名法 | |
| 12 | 0.4 | 物质分离、提纯的常见化学方法 | |
| 13 | 0.65 | 缩聚反应 缩聚物的单体、链节及聚合度的确定 高分子材料的有机推断 | |
| 14 | 0.94 | 有机物的结构特点 | |
| 15 | 0.65 | 测定溶液pH的方法 仪器使用与实验安全 | |
| 16 | 0.65 | 二氧化硫的化学性质 物质性质实验方案的设计 | |
| 17 | 0.65 | 多官能团有机物的结构与性质 | |
| 18 | 0.4 | 根据要求书写同分异构体 羧酸酯化反应 | |
| 19 | 0.4 | 同分异构体的数目的确定 | |
| 20 | 0.65 | 氧化还原反应的应用 | |
| 21 | 0.4 | 有机反应类型 同分异构体的数目的确定 | |
| 22 | 0.65 | 温度对化学平衡移动的影响 化学平衡常数的概念及表达方式 转化率的相关计算及判断 | |
| 23 | 0.15 | 弱电解质的电离平衡 弱电解质电离平衡的影响因素 盐类水解的应用 | |
| 24 | 0.4 | 原电池 新型电池 | |
| 25 | 0.4 | 难溶电解质的溶解平衡 沉淀溶解平衡的应用 溶度积 | |
| 二、填空题 | |||
| 26 | 0.85 | 卤代烃的消去反应 卤代烃的制备 | |
| 三、解答题 | |||
| 27 | 0.65 | 有机官能团的性质及结构 根据要求书写同分异构体 含有酚羟基的物质性质的推断 有机推断综合考查 | 有机推断题 |
| 28 | 0.4 | 根据要求书写同分异构体 羧酸酯化反应 有机物的推断 | 有机推断题 |
| 29 | 0.65 | 同分异构体书写 根据题给物质选择合适合成路线 有机合成综合考查 | 有机推断题 |