2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
北京
高三
高考真题
2017-08-08
13360次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、化学反应原理
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
北京
高三
高考真题
2017-08-08
13360次
整体难度:
适中
考查范围:
认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
容易(0.94)
真题
名校
您最近一年使用:0次
2017-07-01更新
|
2523次组卷
|
45卷引用:四川省广安市2016-2017学年高二下学期期末考试化学试题
四川省广安市2016-2017学年高二下学期期末考试化学试题山东省济南市平阴县玛钢外国语学校2016-2017学年高一下学期期末考试化学试题福建省泉州市泉港区第一中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题01 基本概念类选择题解题方法和策略(已下线)狂刷01 有机化合物的分类—《小题狂刷》2017-2018学年高二化学人教选修5(已下线)《考前20天终极攻略》-5月16日 化学与STSE(已下线)解密01 物质的组成、性质和分类 化学用语——备战2018年高考化学之高频考点解密【全国市级联考】广东省潮州市2017-2018学年高一下学期期末考试化学试题(已下线)学科网2019年高考化学一轮复习讲练测2.1 物质的组成、性质及分类 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化 第1讲 物质的组成、性质和分类 【教学案】云南省玉溪市第一中学2019届高三上学期第二次调研考试化学试题海南省儋州市第一中学2019届高三上学期统测(一)化学试题安徽省黄山市徽州区第一中学2018-2019学年高二上学期开学考试化学试题(已下线)【备战2019年浙江新高考-考点】——考点01 物质的组成、性质及分类湖南省怀化市2018届高三上学期期末统一考试化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第1讲 物质的分类( 教学案)(已下线)2019高考备考二轮复习精品资料-专题1 物质的组成、性质、分类与化学用语(教学案)(已下线)2019年高考总复习巅峰冲刺-专题01 联系生产、科学、生活实际的社会热点问题应试策略(已下线)专题2.1 物质的组成、性质及分类(练)-《2020年高考一轮复习讲练测》(已下线)专题一 化学与STSE(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)广东省深圳中学2020届高三2月份网络教学质量监测理综化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题河北省石家庄市第二中学2020届高中毕业班三月份网络教学质量监测卷理科综合化学部分福建省南平市高级中学2019-2020学年高一下学期期中考试化学试题四川省广安市北京师范大学广安实验学校2019-2020学年高二下学期第三次月考化学试题鲁科版(2019)高一必修第二册 第3章 简单有机化合物 第1节 认识有机化合物 高考帮海南省海口市第四中学2021届高三上学期期中考试化学试题专题1 第一单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第七章 有机化合物 章末综合检测卷吉林省长春市第二十中学2019-2020学年高二下学期期末考试化学试题黑龙江双鸭山市第一中学2021-2022学年高二下学期开学考试化学试题黑龙江省哈尔滨市第九中学2021-2022学年高二上学期开学考试化学试题吉林省抚松县泉阳镇抚松县第六中学2021-2022学年高二上学期化学与生活知识竞赛化学试题(已下线)解密01 物质的组成、分类和转化(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密01 物质的组成、分类和转化(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点01 物质的分类和转化-备战2023年高考化学一轮复习考点帮(全国通用)专题1 有机化学的发展及研究思路 第一~二单元 综合拔高练甘肃省庆阳市第六中学2021-2022学年高一下学期期中考试化学试题 1.1.1有机化学的发展与应用 课后(已下线)考点01 物质的分类和转化(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河南省周口市太康县2022-2023学年高一上学期11月期中考试化学试题北京市第二中学2022-2023学年高一下学期期末考试化学试题
单选题
|
适中(0.65)
2. 2016年IUPAC命名117号元素为Ts(中文名“ ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是
| A.Ts是第七周期第ⅦA族元素 |
| B.Ts的同位素原子具有相同的电子数 |
| C.Ts在同族元素中非金属性最弱 |
D.中子数为176的Ts核素符号是 |
您最近一年使用:0次
2023-09-04更新
|
287次组卷
|
119卷引用:山东省济南市平阴县玛钢外国语学校2016-2017学年高一下学期期末考试化学试题
山东省济南市平阴县玛钢外国语学校2016-2017学年高一下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)安徽省宣城市2016-2017学年高一下学期期末调研测试化学试题新疆生产建设兵团第二中学2016-2017学年高二下学期第四次月考化学试题陕西省西安中学2018届高三上学期第一次摸底考试化学试题辽宁省大连渤海高级中学2018届高三上学期期末考试化学试题2017-2018学年人教版高中化学必修2单元测试题 第1章 物质结构 元素周期律《课时同步君》2017-2018学年高一化学人教必修2-1.1.3 核素(已下线)狂刷03 核素—《小题狂刷》2017-2018学年高一化学人教必修2云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题安徽省蚌埠市第二中学2017-2018学年高一下学期期中考试化学试题【全国百强校】福建省莆田第一中学2017-2018学年高二下学期期中考试化学试题【全国校级联考】安徽省淮北十二中、濉溪二中2017-2018学年高一下学期期中联考化学试题【全国百强校】黑龙江省大庆第一中学2017-2018学年高一下学期第三次阶段检测化学试题(已下线)解密07 物质结构和元素周期律(教师版)——备战2018年高考化学之高频考点解密【全国百强校】陕西省西安市长安区第一中学2017-2018学年高一下学期期末考试(理)化学试题【全国百强校】湖南师范大学附属中学2017-2018学年高一下学期期末考试化学试题黑龙江省伊春市第二中学2017-2018学年高一下学期期末考试(理)化学试题【全国百强校】四川省雅安市雅安中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)(已下线)考点06 原子结构 化学键——备战2019年浙江新高考化学考点江西省宜春市上高二中2018-2019学年高一下学期第一次月考化学试题云南省师范大学附属中学2018~2019学年高一下学期3月考试化学试题重庆市第三十中学2018-2019学年高一下学期期中考试化学试题湖南省醴陵市第一中学2018-2019学年高一下学期期中考试化学试题步步为赢 高一化学暑假作业:作业一 元素周期表四川省广安市广安中学2018-2019学年高一下学期第三次月考化学试题百所名校联考-物质结构 元素周期律2020届高三化学理论复习 元素周期律和元素周期表(专题训练)(已下线)考点13 物质结构 元素周期律 化学键——《备战2020年高考精选考点专项突破题集》贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题人教版高一化学必修2同步练习:第一章第一节第一课时《元素周期表》四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题吉林省吉化第一高级中学校2019-2020学年高一下学期3月线上考试化学试题福建省福州市格致中学2018-2019学年高二下学期期中考试化学试题河北省武邑中学2019-2020学年高一下学期3月线上考试化学试题第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)广东省深圳市红岭中学2019-2020学年高一下学期第一次在线考试化学试题(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训四川省邻水实验学校2019-2020学年高一下学期入学考试化学试题山西省晋中市和诚中学2019-2020学年高一3月月考化学试题吉林省延边市长白山第一高级中学2019-2020学年高一下学期验收考试化学试题陕西省榆林市绥德县绥德中学2019-2020高一下学期第一次阶段性测试化学试题湖北省武汉市华中师范大学第一附属中学2020届高三2月份网络教学质量监测理综化学试题湖北省宜昌市第二中学2019-2020高一下学期4 月线上检测化学试题甘肃省张掖市临泽县第一中学2019-2020学年高一下学期期中考试化学试题安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题山西省运城市高中联合体2019-2020学年高一下学期第一次摸底考试化学试题河南省郑州市中牟县第一高级中学2019-2020高一下学期第二次月考化学试题四川省南充高级中学2019-2020学年高一下学期期中考试化学试题(已下线)专题5.1 原子结构(练)——2020年高考化学一轮复习讲练测(已下线)专题5.1 原子结构(讲)——2020年高考化学一轮复习讲练测山东省滕州市第一中学2019-2020学年高一5月摸底考试化学试题福建省莆田第一中学2019-2020学年高一下学期期中考试化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第三次综合测试化学试题内蒙古自治区呼和浩特市开来中学2019-2020学年高一下学期期末考试化学试题吉林省松原市前郭尔罗斯蒙古族自治县蒙古族中学2019-2020学年高一下学期网课检测化学试题湖南省长沙市长郡中学2019-2020学年高一下学期期末考试化学试题湖南省郴州市2019-2020学年高一下学期期末考试化学试题吉林省长春汽车经济技术开发区第六中学2019-2020学年高一下学期期末考试化学试题安徽省蚌埠第三中学2019-2020学年高一下学期5月月考化学试题(已下线)4.1.3 核素(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.1.3 核素-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)湖南省常德市第一中学2021届高三第四次月水平检测试化学试题(已下线)【浙江新东方】双师107专题5 第二单元综合拔高练-高中化学苏教2019版必修第一册北京市大兴区2020-2021学年高一上学期期末考试化学试题甘肃省兰州市第五十五中学2020-2021学年高一下学期3月月考化学试题北京市第四十三中学2020-2021学年高一下学期第一次月考化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题(已下线)期末检测卷1 -2020-2021学年高一化学必修2章末集训必刷卷(人教版)湖南省长沙市周南中学2020-2021学年高一年级下学期期末考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)4.1.3 原子结构与元素的性质-2021-2022学年高一化学课后培优练(人教版2019必修第一册)上海市复旦大学附属中学青浦分校2022届高三化学测试(一)人教2019版必修第一册第四章第一节 原子结构与元素周期表课后习题北京师范大学附属中学2021-2022学年高一上学期期末考试化学试题云南省玉溪市2021-2022学年高一上学期期末教学质量检测化学试题贵州省黔东南州凯里一中2021-2022学年高一下学期开学考试化学试题宁夏青铜峡市宁朔中学2021-2022学年高一3月月考化学试题广东省佛山市第一中学2021-2022学年高一上学期第二次段考化学试题甘肃省张掖市第二中学2021-2022学年高一上学期期末考试化学试题天津市和平区2021-2022学年高一下学期高中学业水平合格性模拟考试化学试题(已下线)考点07 元素周期律和元素周期表-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古呼伦贝尔市满洲里市第一中学2021-2022学年高一下学期期末考试化学试题专题1 揭示物质结构的奥秘 ★第一~三单元综合拔高练第四章 物质结构 元素周期律 综合拔高练陕西省西安市长安区第一中学2021-2022学年高一下学期期中考试化学试题广西贺州第五高级中学2012-2022学年高一下学期第一次月考化学试题山东省泰安肥城市2021-2022学年高一下学期期中考试化学试题河北省石家庄精英中学2022-2023高二上学期开学考试化学试题四川省自贡市富顺县城关中学2021-2022学年高一下学期期中考试化学试题陕西省黄陵中学2021-2022学年高一下学期期中考试化学试题黑龙江省饶河县高级中学2022-2023学年高一上学期第二次月考化学试题河南省南阳市第六完全学校高级中学2021-2022学年高一下学期第一次考试化学试题陕西省白河高级中学2020-2021学年高一下学期期中考试化学试题北京市第八中学2022-2023学年高一上学期12月月考化学试题吉林市田家炳高级中学2022-2023学年高一上学期期末考试化学试题北京师范大学附属中学2022-2023学年高一上学期期末考试化学试题河南省洛阳市2022-2023学年高一上学期期末考试化学试题(已下线)北京市海淀区2022届高三一模(选择题6-10)山东省枣庄市第八中学南校2022-2023学年高一3月月考化学试题(已下线)【知识图鉴】单元讲练测必修第一册第四单元03巩固练(已下线)【知识图鉴】单元讲练测必修第一册第四单元02基础练(已下线)考点巩固卷05 物质结构 元素周期律(2大考点50题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)T8-元素周期表和元素周期律(已下线)第六章单元测试卷新疆疏勒县第一中学等3校2022-2023学年高一上学期1月期末考试化学试题湖南省长沙市长郡中学2023-2024学年高二上学期入学考试化学试题河北省衡水市武强学校2023-2024学年高三上学期开学考试化学试题(已下线)合格考真题汇编16原子结构与化学键内蒙古赤峰第四中学2020-2021学年高一下学期第一次月考化学试题黑龙江省大庆实验中学实验一部2023-2024学年高一上学期期末考试化学试题湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题云南省保山市腾冲市第八中学2020-2021学年高一下学期期末考试化学试题北京市第二十二中学2023-2024学年高一下学期期中考试化学试题甘肃省兰州新华互联网学校2023-2024学年高一上学期期末考题化学试卷
单选题
|
适中(0.65)
真题
名校
3. 下列变化中,气体被还原的是
| A.二氧化碳使Na2O2固体变白 | B.氯气使KBr溶液变黄 |
| C.乙烯使Br2的四氯化碳溶液褪色 | D.氨气使AlCl3溶液产生白色沉淀 |
您最近一年使用:0次
2017-08-08更新
|
3051次组卷
|
32卷引用:2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)广东省华南师范大学附属中学2018届高三上学期第一次月考理综化学试题北京市一零一中学2018届高三10月月考化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.4 氧化还原反应(已下线)狂刷05 脂肪烃—《小题狂刷》2017-2018学年高二化学人教选修5(已下线)解密03 氧化还原反应——备战2018年高考化学之高频考点解密(已下线)学科网2019年高考化学一轮复习讲练测2.3 氧化还原反应的基本概念 练(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第3讲 氧化还原反应【教学案】云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (教学案)(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)(已下线)考点05 氧化还原反应——备战2019年浙江新高考化学考点(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》吉林省延边市第二中学2020届高三入学考试化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题新疆阿克苏市阿瓦提四中2020届高三上学期第二次月考化学试题(已下线)专题四 氧化还原反应(真题汇编)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题淅江温州新力量联盟2019-2020学年高二下学期期中联考化学试题(已下线)第4单元 氧化还原反应(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷福建师范大学附属中学2021届高三启明级上学期第二次阶段考试化学试题广东省揭阳市揭西县河婆中学2020-2021学年高一下学期期末考试化学试题吉林白城市洮南市第一中学2020-2021学年高二下学期期末考试化学试题河南省实验中学2022届高三9月月考化学试卷云南省昌宁县第一中学2021-2022学年高三下学期3月月考化学试题山西省长治市沁源县第一中学等名校2021-2022学年高二下学期5月联考化学试题陕西省西安市长安区第一中学2021-2022学年高一下学期期中考试化学试题云南省第一民族中学2021-2022学年高三下学期2月份开学测试化学试题北京市第二中学2022-2023学年高一下学期期末考试化学试题上海市洋泾中学2023-2024学年高三上学期期中考试化学试题
4. 我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:
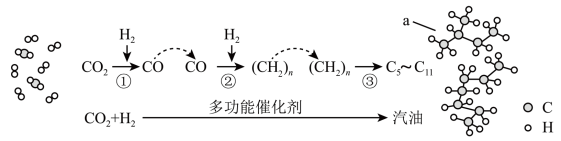
| A.反应①的产物中含有水 |
| B.反应②中只有碳碳键形成 |
| C.汽油主要是C5~C11的烃类混合物 |
| D.图中a的名称是2-甲基丁烷 |
您最近一年使用:0次
2020-08-28更新
|
3954次组卷
|
72卷引用:河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题
河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)湖南省长郡中学2017-2018学年高二上学期第一次模块检测化学试题1江西省等三省十校2018届高三下学期联考理综化学试题(已下线)狂刷03 有机化合物的命名—《小题狂刷》2017-2018学年高二化学人教选修5重庆市第二中学2018届高三3月测试化学试题安徽省师范大学附属中学2017-2018学年高二下学期期中考试化学试题(已下线)《考前20天终极攻略》-5月18日 有机物的结构与性质【全国百强校】北京师范大学附属中学2017-2018学年高二下学期期中考试化学试题【全国百强校】北京市第四中学2017-2018学年高二下学期期中考试化学试题【全国百强校】江苏省海安高级中学2017-2018学年高二6月月考化学试题(已下线)解密14 几种常见的烃——备战2018年高考化学之高频考点解密【区级联考】北京市丰台区2018-2019学年高二第一学期期中考试化学试题【全国百强校】河北省石家庄市第二中学2018-2019学年高二第一学期12月月考化学试题【全国百强校】新疆维吾尔自治区第二师华山中学2018-2019学年高二上学期期末考试化学试题【区级联考】江苏省泰州市姜堰区2018-2019学年高二下学期期中考试化学试题北京师大附中2018-2019学年高二下学期期中考试化学试题广东省佛山一中、石门中学、顺德一中、国华纪中四校2018-2019学年高二下学期期末联考化学试题浙江省温州市十校联合体2018-2019学年高二上学期期末化学试题内蒙古赤峰市赤峰二中2019-2020学年高二上学期第一次月考化学试题(已下线)专题9.1 重要的烃 化石燃料(讲)-《2020年高考一轮复习讲练测》(已下线)专题9.1 重要的烃 化石燃料(练)-《2020年高考一轮复习讲练测》江西省高安中学2019-2020学年高二上学期期中考试化学试题(B卷)上海市民星中学2018—2019学年高三上学期期中考试化学试题人教版高中化学必修2第四章《化学与自然资源的开发利用》检测题(已下线)【新东方】2020-64山东省滕州市第一中学2020届高三3月线上模拟考试化学试题江西省赣州市于都县第二高级中学2019-2020i学年高二下学期线上考试化学试题第二章 烃和卤代烃——C挑战 模拟高考(人教版选修5)江西省上饶市2018-2019学年高二下学期期末教学质量测试化学试题四川省内江市第六中学2019-2020学年高一下学期入学考试化学B试题河北衡水中学2020届高三下学期三月份教学质量监测理科综合化学试题2020届四川省成都市第七中学高三二月份网络教学质量监测卷化学试题2020届湖南省湘潭市高三教学质量监测卷化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题四川隆昌市第二中学2019-2020学年高一下学期4月测试化学试题(已下线)专题4.1 碳、硅及其无机非金属材料 (讲)——2020年高考化学一轮复习讲练测(已下线)专题4.1 碳、硅及其无机非金属材料 (练)——2020年高考化学一轮复习讲练测四川省攀枝花市第十五中学2019-2020学年高二下学期期中考试化学试卷吉林省长春市第二实验中学2019-2020学年高一下学期期末考试化学试卷山西省大同一中2019-2020学年高一下学期6月月考化学试题(已下线)第13讲 碳、硅及无机非金属材料(精讲)——2021年高考化学一轮复习讲练测江苏省盐城市一中、射阳中学等五校2020-2021学年高二上学期期中联考化学(选修)试题第29讲 重要的烃 同分异构体(精练)-2021年高考化学一轮复习讲练测北京市第十二中学2020-2021学年高二上学期期末考试化学试题高二选择性必修3(人教版2019)第一章 有机化合物的结构特点与研究方法 第一章 素养检测河南省洛阳市豫西名校2020-2021学年高二下学期第一次联考化学试题广东省清远市凤霞中学2020-2021学年高二下学期期中质量检测化学试题(已下线)考点27 甲烷、乙烯和苯的性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点26 甲烷、乙烯和苯的性质-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点37 烃-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点37 烃和卤代烃-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)第9讲 无机非金属材料 (讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)课时46 甲烷、乙烯和苯-2022年高考化学一轮复习小题多维练(全国通用)江苏省盐城市上冈高级中学2021-2022学年高二上学期期中考试化学(选修)试题江苏省盱眙中学2021-2022学年上学期高二年级期中考试化学试题云南省宣威市第三中学2021-2022学年高二上学期期末考试化学试题江西省萍乡市上栗中学2021-2022学年高二下学期第二次月考化学试题甘肃省天水市第一中学2021-2022学年高二下学期第一阶段考试化学试题北京师范大学第二附属中学2021-2022学年高二下学期期中考试化学试题广东省佛山市顺德区第一中学 2021-2022学年高二下学期期中考试化学试题湖南省益阳市第一中学2021-2022学年高二下学期期中考试化学试题湖南省株洲市茶陵县第一中学2021-2022学年高二下学期期中考试化学试题浙江省绍兴市柯桥区2021-2022学年高一下学期期末(实验班)化学试题(已下线)第09讲 无机非金属材料(练)-2023年高考化学一轮复习讲练测(新教材新高考)福建省上杭第一中学2022-2023学年高三上学期暑期考试化学试题江苏省宿迁市沭阳县2021-2022学年高二下学期期中调研测试化学试题山西省临汾市尧都区山西师范大学实验中学2021-2022学年高二下学期第二次月考化学试题江苏省江阴市四校2022-2023学年高二上学期期中联考化学试题北京市中国人民大学附属中学2019-2020学年高二上学期期中考试化学试题陕西省西安市长安区第一中学2022-2023学年高二下学期第二次质量检测化学试题北京师范大学第二附属中学2023-2024学年高二下学期期中考试化学试题
单选题
|
适中(0.65)
5. 根据SO2通入不同溶液中的实验现象,所得结论不正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
| B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
| C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
| D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
| A.A | B.B | C.C | D.D |
【知识点】 二氧化硫的化学性质 物质性质实验方案的设计解读
您最近一年使用:0次
2023-06-07更新
|
1558次组卷
|
108卷引用:山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题
山东省淄博市淄川中学2016-2017学年高二下学期学分认定(期末)考试化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省涞水波峰中学2018届高三第一次调研考试化学试题江西省横峰中学、铅山一中、德兴一中2018届高三上学期第一次月考化学试题宁夏六盘山高级中学2018届高三上学期第一次月考化学试题山东省郓城实验中学2018届高三10月月考化学试题江西省铅山县第一中学2018届高三上学期第一次月考化学试题黑龙江省哈尔滨市第六中学2018届高三12月月考化学试题辽宁省大连渤海高级中学2018届高三上学期期末考试化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题内蒙古北方重工业集团有限公司第三中学2017-2018学年高一3月月考化学试题(已下线)《考前20天终极攻略》-5月21日 基础实验(已下线)《考前20天终极攻略》-5月26日 元素及其化合物(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密【全国市级联考】四川省广安市2017-2018学年高一下学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氧及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题【全国百强校】宁夏回族自治区育才中学2019届高三上学期月考(二)化学试题云南省腾冲市第八中学2018-2019学年高二上学期期中考试化学试题【全国百强校】山东省济南市第一中学2019届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第3讲 硫及其化合物 (教学案)【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期12月月考化学试题(已下线)2019高考热点题型和提分秘籍 第四章 常见的非金属及其化合物 第1讲 碳、硅及无机非金属材料 (教学案)山东省德州市夏津县第一中学2019届高三上学期12月月考化学试题(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(教学案)(已下线)2019高考备考二轮复习精品资料-专题6 非金属及其化合物(押题专练)(已下线)2019高考备考二轮复习精品资料-专题5 金属及其化合物(教学案)(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略河南省封丘县第一中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十三 化学实验综合内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题四川省成都石室中学2019-2020学年高二入学考试化学试题北京师范大学实验中学丰台学校2019-2020学年高三上学期期中考试化学试题2020届高三化学一轮复习 化学基础实验(选择题和大题训练)四川省成都市实验中学2020届高三上学期第十四次周考理科综合化学试题(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省黄山市八校联盟2019-2020学年高一下学期期中联考化学试题(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次综合测试化学试题黑龙江省大庆市第十中学2019-2020学年高二下学期期末考试化学试题四川省泸县第二中学2019-2020学年高一下学期期末模拟考试化学试题苏教版(2020)高一必修第一册专题4 总结检测(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测安徽省阜阳市阜南实验中学2020届高三下学期4月月考化学试题山东省济南市章丘区第四中学2021届高三上学期第一次教学质量检测(8月)化学试题黑龙江省哈尔滨市第三中学校2020-2021学年高三上学期第一次验收考试化学试题湖北省宜昌市葛洲坝中学2021届高三9月月考化学试题陕西省西安中学2018-2019学年高一下学期期末考试化学题湖南省邵阳市邵东县创新实验学校2021届高三上学期第一次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测福建省莆田第二十五中学2021届高三上学期期中考试化学试题江西省鹰潭市2019-2020年度高一下学期期末检测化学试题吉林省长春市第二十九中学2021届高三上学期期末考试化学试题专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册辽宁沈阳市第二十八中学2020--2021学年高一上学期期末考试化学试题河北省深州市长江中学2020-2021学年高一下学期3月底月考化学试题新疆维吾尔自治区巴州二中2021届高三第六次月考化学试题重庆市永川景圣中学2020-2021学年高三上学期第二次月考化学试题广东实验中学2020-201学年高一下学期期中考试化学(合格考)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第11讲 硫及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第7周 晚练题-备战2022年高考化学周测与晚练(新高考专用)安徽省马鞍山市含山县第二中学2021-2022学年高三上学期第一次月考化学试题广西河池市高级中学2021-2022学年高三上学期第三次月考化学试题云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)北京市顺义牛栏山第一中学2021-2022学年高一下学期居家学习成果展示化学测试题北京师范大学附属中学2021-2022学年高一下学期期中考试化学试题(已下线)第11讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期第一次验收考试化学试题黑龙江省哈尔滨市第三中学校2022-2023学年高三上学期9月月考化学试题辽宁省本溪满族自治县高级中学2021-2022学年高一下学期开学考试化学试题黑龙江省哈尔滨市第十九中学2021-2022学年高三上学期第一次月考化学试题(已下线)化学(北京A卷)-学易金卷:2023年高考第一次模拟考试卷云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题(已下线)题型48 SO2的制备与性质探究北京市顺义区第一中学2022-2023学年高一下学期3月月考化学试题宁夏银川市第二中学2022-2023学年高一下学期第一次月考化学试题山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试化学试题广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题广东省深圳聚龙科学中学2022-2023学年高一下学期第一次段考(学业水平)化学试题广东省广州市广东实验中学2020-2021学年高一下学期期中考试(合格考)化学试题(已下线)第3讲 硫及其重要化合物北京市第二中学2022-2023学年高一下学期期末考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题江苏省南菁高级中学2023-2024学年高一上学期9月阶段性检测化学(创优班)试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题陕西省咸阳市三原县北城中学2023-2024学年高一下学期第一次月考化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
6. 聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图,(图中虚线表示氢键),下列说法不正确的是
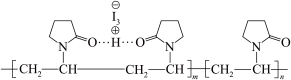

A.聚维酮的单体是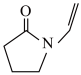 |
| B.聚维酮碘是一种水溶性物质 |
| C.聚维酮在一定条件下能发生水解反应 |
| D.聚维酮分子由(m+n)个单体聚合而成 |
您最近一年使用:0次
2023-06-03更新
|
373次组卷
|
45卷引用:吉林省实验中学2016-2017学年高二下学期期末考试化学试题
吉林省实验中学2016-2017学年高二下学期期末考试化学试题甘肃省兰州市第一中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)黑龙江省大庆中学2016-2017学年高二下学期期末考试化学试题北京市清华大学附属中学2018届高三10月月考化学试题云南省峨山彝族自治县第一中学2018届高三上学期期末考试仿真化学试题甘肃省酒泉市敦煌中学2019届高三一诊化学试题【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题【全国百强校】浙江省嘉兴市第一中学、湖州中学2018-2019学年高二下学期期中考试化学试题(已下线)2019年6月2日 《每日一题》选修5-每周一测河南省周口中英文学校2018-2019学年高二下学期期末考试化学试题辽宁省沈阳铁路实验中学2020届高三上学期开学考试化学试题江西省临川第二中学2020届高三10月月考化学试题江西省景德镇一中2019-2020学年高二上学期期中考试化学试题人教版选修五2019—2020学年高二上学期化学期末复习—选择题专题训练(已下线)考点18 有机高分子化合物——《备战2020年高考精选考点专项突破题集》安徽省太和中学2019-2020学年高二上学期第四次月考(实验班)化学试题上海市民星中学2018—2019学年高三上学期期中考试化学试题江西省高安中学2019-2020学年高二上学期期末考试化学(A卷)试题【省级联考】浙江省2019—2020学年普通高校招生选考科目化学模拟试题浙江省湖州中学2019-2020学年高二下学期3月月考化学试题第五章 进入合成有机高分子化合物的时代—— C 挑战区 模拟高考(人教版选修5)第3章 有机合成及其应用 合成高分子化合物——C挑战区 模拟高考(鲁科版选修5)2020届高三高考化学专题之消毒杀菌练习广东省深圳中学2020年高中毕业班教学质量监测卷理科综合化学试题湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学浙江省温州市平阳县2020届高三高考适应性考试(6月)化学试题山东省青岛市第十七中学2021届高三上学期10月阶段性检测化学试题江西省宜春市高安中学2019-2020学年高二上学期期末考试化学试题(创新班)山东省烟台市中英文学校2021届高三上学期冬学竞赛化学试题青海省湟川中学2019-2020学年高二下学期期中考试化学试题(鲁科版2019)选3第3章 B素养拓展区重庆市七校2020—2021学年高二下学期期末联考化学试题(已下线)考点40 有机合成高分子-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点41 合成高分子 有机合成-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时50 官能团与有机物的性质-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点43 合成高分子-备战2023年高考化学一轮复习考点帮(全国通用)第五章 合成高分子浙江省浙里卷天下2022-2023学年高三8月开学测试化学试题北京汇文中学2022-2023学年高二上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测选择性必修3第5单元03巩固练(已下线)安徽省、云南省、吉林省、黑龙江省2023届高三2月适应性测试变式题(选择题7-10)浙江省宁波效实中学2022-2023学年高二下学期期中考试化学试题北京市清华大学附属中学2020-2021学年高二下学期期中考试化学试题(已下线)第5讲 生物大分子 合成高分子
单选题
|
适中(0.65)
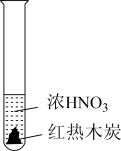
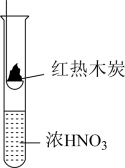
7. 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
| ① | ② | ③ |
| A.由①中的红棕色气体,推断产生的气体一定是混合气体 |
| B.由②中的红棕色气体不能表明木炭与浓硝酸发生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 |
| D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应 |
【知识点】 硝酸的不稳定性解读 化学实验方案的设计与评价 物质性质的探究解读
您最近一年使用:0次
2022-06-29更新
|
3769次组卷
|
81卷引用:河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题
河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省衡水中学2018届高三上学期一调考试化学试题山东省淄博第一中学2018届高三上学期开学考试化学试题四川省德阳市三校2018届高三联合测试化学试题(已下线)黄金30题系列 高一化学 小题好拿分【提升版】北京市清华大学附属中学2018届高三10月月考化学试题广西陆川县中学2018届高三12月月考化学试题北京市一零一中学2018届高三10月月考化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题云南省峨山彝族自治县第一中学2018届高三上学期期末考试仿真化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题河南省三门峡市2017-2018学年高一上学期期末考试化学试题广西陆川县中学2018届高三3月月考化学试题云南省玉溪第一中学2017-2018学年高一下学期4月月考化学试题云南省玉溪市玉溪一中2017-2018学年高一下学期4月月考化学试题(已下线)解密06 非金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】云南省玉溪市峨山一中2019届高三9月月考化学试题江苏省常州市第一中学2019届高三第一学期期初(8月)考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题【全国百强校】山西省山西大学附属中学2018-2019学年高一下学期2月模块诊断化学试题福建省泉州市泉港区第一中学2018-2019学年高一下学期期中考试化学试题百所名校联考-非金属及其化合物内蒙古包头稀土高新区二中2020届高三10月月考理综化学试题四川省绵阳市南山中学2020届高三10月月考化学试题(已下线)2019年12月11日 《每日一题》化学人教版(必修1)——硝酸的强氧化性2020届高三化学二轮冲刺新题专练——硝酸的性质及应用(提升练)贵州省黔南布依族苗族自治州龙里中学2019-2020学年高三上学期期末考试理综化学试题贵州省长顺县二中2019-2020学年高三上学期期末考试理综化学试题贵州省施秉县一中2019-2020学年高三上学期期末考试化学试题(已下线)专题3.5 氮及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》福建省福州市第一中学2020年高一在线自测自评质检化学试题贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题安徽省池州市第一中学2019-2020学年高一下学期期中教学质量检测化学试题云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷安徽省六安市舒城中学2019-2020学年高一下学期第一次月考化学试题(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第12讲 氮及其化合物-2021年高考化学一轮复习名师精讲练2019年上海市高中生化学竞赛初赛试题(“华理一化工杯”)初赛试题鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关高一必修第一册(鲁科2019)第3章 第3节 氮的循环 高考帮(已下线)小题必刷20 氮及其化合物——2021年高考化学一轮复习小题必刷(通用版)湖南省长沙市雅礼中学2021届高三上学期第一次月考化学试题北京一零一中2021届高三上学期第三次统练化学试题(已下线)【浙江新东方】48安徽省滁州市定远县重点中学2021届高三上学期11月质量检测化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】陕西省西安市长安区第一中学2019-2020学年高一上学期期末考试化学试题专题7 第一~二单元 综合拔高练-高中化学必修第二册苏教版2019(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物(已下线)【浙江新东方】高中化学20210304-015黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题浙江省诸暨市2021届高三5月适应性考试化学试题福建省泉州科技中学2020-2021学年高一下学期期中考试化学试题(苏教版2019)必修第二册专题7 氮与社会可持续发展 C 高考挑战区安徽省芜湖市2020-2021学年高一下学期期末质量检测联考化学试题(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第12讲 氮及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)河南部分学校2022届新高三8月份摸底联考化学试题北京市中国农业大学附属中学2020-2021学年高一上学期期末学业水平调研化学试题(已下线)专题07 常见非金属及其化合物-备战2022年高考化学学霸纠错(全国通用)课后-5.2.3 硝酸 酸雨及防治-人教2019必修第二册云南省瑞丽市第一民族中学2021-2022学年高三下学期3月月考化学试题辽宁省沈阳市第二十中学2019-2020学年高一下学期第一次月考化学试题江西省吉安市2021-2022学年高二下学期期末检测化学试题(已下线)考点11 氮及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 氮及其化合物(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第13练 氮及其化合物-2023年高考化学一轮复习小题多维练(全国通用)广东省揭阳华侨高级中学2021-2022学年高一下学期第一次阶段化学试题北京市首师附密云中学2021-2022学年高一下学期等级考化学试题山东省菏泽市单县第二中学2021-2022学年高一上学期(实验班)12月段考化学试题第四章 非金属及其化合物 第23讲 硝酸 含氮化合物的转化关系巩固训练12(已下线)题型61 硝酸、硝酸盐的性质安徽省合肥市第一中学2022-2023学年高一下学期第4次月考化学试题(已下线)考点11 氮及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
二、解答题 添加题型下试题
解答题-有机推断题
|
较难(0.4)
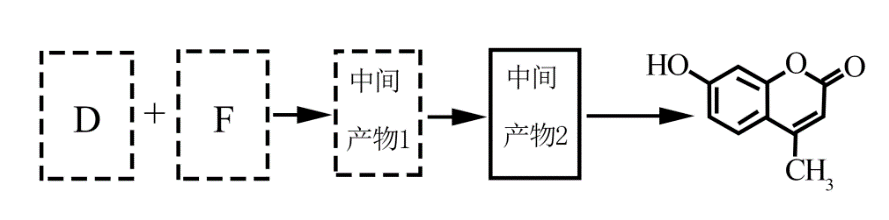
8. 羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
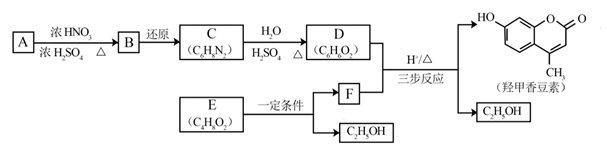
已知: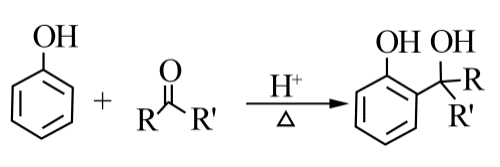
RCOOR'+R''OH RCOOR''+ R'OH(R、R'、R''代表烃基)
RCOOR''+ R'OH(R、R'、R''代表烃基)
(1)A属于芳香烃,其结构简式是______________________ 。B中所含的官能团是________________ 。
(2)C→D的反应类型是___________________ 。
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成E,写出有关化学方程式:__________ 。
(4)已知:2E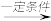 F+C2H5OH。F所含官能团有
F+C2H5OH。F所含官能团有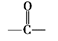 和
和___________ 。
(5)以D和F为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式:_________

已知:

RCOOR'+R''OH
 RCOOR''+ R'OH(R、R'、R''代表烃基)
RCOOR''+ R'OH(R、R'、R''代表烃基)(1)A属于芳香烃,其结构简式是
(2)C→D的反应类型是
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成E,写出有关化学方程式:
(4)已知:2E
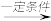 F+C2H5OH。F所含官能团有
F+C2H5OH。F所含官能团有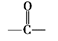 和
和(5)以D和F为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式:

您最近一年使用:0次
2017-08-08更新
|
3512次组卷
|
9卷引用:2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)河北省定州中学2018届高三上学期第一次调研化学试题重庆市第二中学2018届高三3月测试化学试题【全国百强校】北京师范大学附属中学2017-2018学年高二下学期期中考试化学试题(已下线)解密22 有机化学基础(教师版)——备战2018年高考化学之高频考点解密【全国百强校】北京市中央民族大学附属中学(朝阳分校)2019届高三上学期10月月考化学试题(已下线)2019年6月21日 《每日一题》选修5-有机推断综合题云南省屏边县民中2020届高三上学期开学考试化学试题备考突破2020高三化学专题强化集训——化学有机推断题
解答题-原理综合题
|
较难(0.4)
9. TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:_______________________ 。
② 氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的ΔH_____ 0(填“>”“<”或“=”),判断依据:_______________ 。
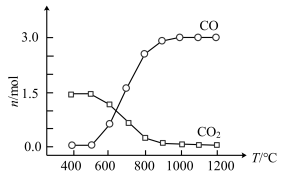
③ 氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是__________________________ 。
④ 氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_____________ 。
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:
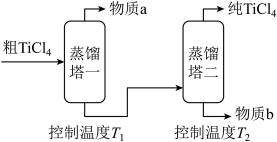
物质a是______________ ,T2应控制在_________ 。

资料:TiCl4及所含杂质氯化物的性质
| 化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
| 熔点/℃ | −69 | −25 | 193 | 304 | 714 |
| 在TiCl4中的溶解性 | 互溶 | —— | 微溶 | 难溶 | |
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:
② 氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的ΔH

③ 氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是
④ 氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:

物质a是
您最近一年使用:0次
2017-08-08更新
|
4035次组卷
|
9卷引用:2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)福建省福州市2018届高三下学期5月模拟考试理综化学试题(已下线)解密19 工艺流程题(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【教学案】湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学湖南省长沙县第九中学2020-2021学年高二上学期第一次月考化学试题北京理工大学附属中学2022-2023学年高三上学期12月月考化学试题(已下线)北京市海淀区2022届高三一模(工业流程题)北京市第十一中学2022-2023学年高二上学期期中考试化学试卷
解答题-原理综合题
|
较难(0.4)
10. SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:___________ 。
② 反应器中NH3还原NO2的化学方程式:___________ 。
③ 当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:___________ 。
④ 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol−1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L−1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L−1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是___________ 。
(2)NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图a所示。___________ 。
② 用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是___________ 。
③ 还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:___________ 
___________ 15NNO+___________ H2O
(1)SCR(选择性催化还原)工作原理:
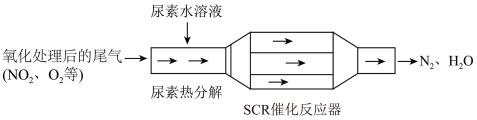
② 反应器中NH3还原NO2的化学方程式:
③ 当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:
④ 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 g·mol−1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L−1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L−1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是
(2)NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图a所示。


② 用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是
③ 还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:

【知识点】 物质的量浓度的计算 基于氧化还原反应守恒规律的计算解读 氨气 一氧化氮
您最近一年使用:0次
2017-08-08更新
|
3694次组卷
|
14卷引用:2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)(已下线)北京四中2018届上学期高三年级期中考试化学试卷(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【教学案】(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】福建省福州市第一中学2020年高一在线自测自评质检化学试题北京市中国人民大学附属中学2020届高三教学质量监测理科综合化学试题河北省衡水中学2020届高三下学期二月份网络教学质量监测理科综合化学试题湖南省衡阳市2020年高中毕业班教学质量监测卷理科综合化学山东省泰安市宁阳一中2021届高三上学期模块考试化学试题北京市北京理工大学附属中学2022届高三十月月考化学试题北京市育才学校2022届高三下学期三模化学试题北京师范大学附属中学2022-2023学年高一下学期期中考试化学试题北京市第三十五中学2023-2024学年高一下学期3月月考化学试卷北京市北京师范大学第二附属中学2023-2024学年高一下学期期中考试化学试题
解答题-实验探究题
|
较难(0.4)
11. 某小组在验证反应“Fe+2Ag+=Fe2++2Ag”的实验中检测到Fe3+,发现和探究过程如下。向硝酸酸化的0.05mol·L-1硝酸银溶液(pH≈2)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取出少量黑色固体,洗涤后,_______ (填操作和现象),证明黑色固体中含有Ag。
②取上层清液,滴加K3Fe(CN)6溶液,产生蓝色沉淀,说明溶液中含有Fe2+。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是___________________ (用离子方程式表示)。针对两种观点继续实验:
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测,同时发现有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
(资料:Ag+与SCN-生成白色沉淀AgSCN)
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于________ (用离子方程式表示),可产生Fe3+;
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据_______ 现象,判断溶液中存在Ag+,可产生Fe3+。
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的________ 溶液(pH≈2)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液,3min时溶液呈浅红色,30min后溶液几乎无色。
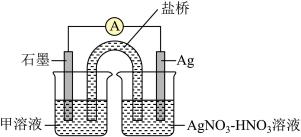
实验Ⅱ:装置如图。其中甲溶液是________ ,操作及现象是________________ 。_______________ 。
(1)检验产物
①取出少量黑色固体,洗涤后,
②取上层清液,滴加K3Fe(CN)6溶液,产生蓝色沉淀,说明溶液中含有Fe2+。
(2)针对“溶液呈黄色”,甲认为溶液中有Fe3+,乙认为铁粉过量时不可能有Fe3+,乙依据的原理是
①取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测,同时发现有白色沉淀生成,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
| 序号 | 取样时间/min | 现象 |
| ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
| ⅱ | 30 | 产生白色沉淀;较3min时量少;溶液红色较3min时加深 |
| ⅲ | 120 | 产生白色沉淀;较30min时量少;溶液红色较30min时变浅 |
②对Fe3+产生的原因作出如下假设:
假设a:可能是铁粉表面有氧化层,能产生Fe3+;
假设b:空气中存在O2,由于
假设c:酸性溶液中NO3-具有氧化性,可产生Fe3+;
假设d:根据
③下列实验Ⅰ可证实假设a、b、c不是产生Fe3+的主要原因。实验Ⅱ可证实假设d成立。
实验Ⅰ:向硝酸酸化的
实验Ⅱ:装置如图。其中甲溶液是
您最近一年使用:0次
2017-08-08更新
|
5135次组卷
|
23卷引用:2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)
2017年全国普通高等学校招生统一考试理综化学(北京卷精编版)贵州省遵义航天高级中学2018届高三第一次模拟考试(9月月考)理科综合化学试题辽宁省实验中学分校2018届高三12月月考理科综合化学试题(已下线)《考前20天终极攻略》-5月27日 综合实验设计、探究和评价(已下线)解密18 物质的制备、实验方案的设计与评价——备战2018年高考化学之高频考点解密(已下线)考点07 元素化合物综合——《备战2020年高考精选考点专项突破题集》湖南长沙长郡中学2020届高三2月份网络教学质量监测卷理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题16 化学实验综合应用-备战2021届高考化学二轮复习题型专练(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题天津市西青区杨柳青第一中学2021--2022 学年高三上学期第一次阶段检测化学试题(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)北京市第四十三中学2021-2022学年高三上学期期中考试化学试题(已下线)题型48 实验原理探究型综合实验北京市中国人民大学附属中学2023-2024学年高三上学期期末考前化学练习 广东省广州市普通高中2024届高三下学期毕业班冲刺训练题(二)化学试题北京市第二十二中学2023-2024学年高一下学期期中考试化学试题北京市丰台区第二中学2024届高三下学期三模化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、有机化学基础、物质结构与性质、化学与STSE、化学实验基础、化学反应原理
试卷题型(共 11题)
题型
数量
单选题
7
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 无机物与有机物 硅酸与硅酸盐 新型有机高分子材料 | |
| 2 | 0.65 | 元素非金属性强弱的比较方法 原子中相关数值及其之间的相互关系 元素、核素、同位素 | |
| 3 | 0.65 | 氯气 溴、碘的性质 氨气 过氧化钠 氧化铝 乙烯 | |
| 4 | 0.65 | 烷烃系统命名法 共价键 能源开发利用新理念 新能源的开发 | |
| 5 | 0.65 | 二氧化硫的化学性质 物质性质实验方案的设计 | |
| 6 | 0.94 | 加聚物的单体、链节及聚合度的确定 氢键对物质性质的影响 | |
| 7 | 0.65 | 硝酸的不稳定性 化学实验方案的设计与评价 物质性质的探究 | |
| 二、解答题 | |||
| 8 | 0.4 | 有机反应类型 芳香烃 酯的化学性质 有机物的合成 | 有机推断题 |
| 9 | 0.4 | 盖斯定律与热化学方程式 化学平衡的移动及其影响因素 物质的分离、提纯 | 原理综合题 |
| 10 | 0.4 | 物质的量浓度的计算 基于氧化还原反应守恒规律的计算 氨气 一氧化氮 | 原理综合题 |
| 11 | 0.4 | Fe3+的检验 原电池原理的应用 化学实验基本操作 化学实验方案的设计与评价 | 实验探究题 |